
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рафінування металу
|
|
|
|
Третьою важливою металургійною операцією, що проходить одночасно з розкисненням і легуванням металу, є його рафінування, тобто очищення від шкідливих домішок — сірки та фосфору.
Джерелами надходження сірки і фосфору в зону зварювання є: а) шлаки, до складу яких входять компоненти, що містять сірку і фосфор; б) розплавлений метал.
Розглянемо вплив шкідливих домішок на наплавлений метал і способи рафінування металу.
Сірка та її видалення із металу шва. Вміст сірки у металі в кількості, що перевищує припустимі норми, негативно позначається на його механічних властивостях, служить причиною червоноламкості металу і появи у ньому кристалізаційних тріщин.
Сірка утворює із залізом сульфід заліза FeS, що має температуру плавлення 1195° С. Сульфід заліза майже не розчиняється у твердому залізі і виділяється у ньому або у виді евтектики, або у виді окремих вкраплень різного виду та форми. Евтектики можуть бути подвійні або потрійні, наприклад, FeS+Fe — Tпл = 985°C; 2FeО×SiО2 + FeS; Fe+FeS+MnS — Tпл = 980° С та ін.
 При кристалізації металу, що проходить в інтервалі температур Т(лікв) — Т(солід), ці сірчисті евтектики відтискуються зростаючими кристалами металу шва до границь між ними і до місця стику кристалів - у центральну частину зварювальної ванни, і є частиною так званих міжкристалітних прошарків (рис. 8.9).
При кристалізації металу, що проходить в інтервалі температур Т(лікв) — Т(солід), ці сірчисті евтектики відтискуються зростаючими кристалами металу шва до границь між ними і до місця стику кристалів - у центральну частину зварювальної ванни, і є частиною так званих міжкристалітних прошарків (рис. 8.9).
До моменту закінчення кристалізації металу шва такі міжкристалітні прошарки можуть ще знаходитися у рідкому стані. Тоді виникнення значних напружень розтягу у шві може викликати появу на цих ділянках кристалізаційних чи гарячих тріщин. Одночасна присутність у металі вуглецю і кремнію збільшує схильність швів до кристалізаційних тріщин.
|
|
|
З усього сказаного неважко зробити висновок, що для більш повного видалення сірки з металу і сприятливого розподілу її частини, що залишилася, необхідно вводити в зварювальну ванну елементи із більшою спорідненістю до сірки, ніж залізо. Утворені сульфіди повинні мати високу температуру плавлення і не створювати евтектик.
По ступеню зростання міцності сульфідів, що утворюються, елементи можна розташувати в ряд (табл. 8.5).
Таблиця 8.5
| Сульфід | Теплота утворення, кал | Сульфід | Теплота утворення, кал |
| NiS FeS MnS MoS2 | MgS Na2S CaS Аl2S3 |
У зварювальній практиці найчастіше зв'язують і видаляють сірку двома способами: за допомогою Мn і МnO, а також СаО.
Сірка утворює з марганцем відносно міцний сульфід MnS із температурою плавлення близько 1620 °С. Сульфід марганцю слабко розчиняється у металі і добре в шлакові; тому він у значній кількості переходить у шлак. Сульфід марганцю, що залишився в металі, розподіляється у дрібнодисперсному вигляді досить рівномірно і не утворює легкоплавких евтектик.
Основною реакцією зв'язування сірки марганцем є
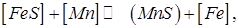 (236) (8.22)
(236) (8.22)
з константою рівноваги  звідки
звідки
 . (237) (8.23)
. (237) (8.23)
Проте ефективність зв'язування сірки у сульфід марганцю по такій реакції мала, бо у напрямку праворуч вона іде помітно лише при знижених температурах, коли швидкості перебігу процесів дуже сповільнюються. У підсумку в металі шва виявляються значні кількості FeS. Тому реакція (8.22) доповнюється другою
 , (238) (8.24)
, (238) (8.24)
для якої константа рівноваги буде 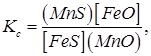 звідкіля
звідкіля
 . (239) (8.25)
. (239) (8.25)
Для реакції (8.24) константа рівноваги Кс зростає зі збільшенням температури, тобто реакція зрушується у бік більшого виходу (MnS) і [ FeO ].
Розглядаючи реакції (8.22) і (8.24) спільно, можна відзначити, що перетворенню FeS у MnS сприяють:
а) краща розкисненість металу;
б) збільшення вмісту марганцю у металі;
в) висока концентрація (MnО) у шлакові.
Звичайно приймають відношення  в металі рівним 20—25, що дозволяє уникнути кристалізаційних тріщин.
в металі рівним 20—25, що дозволяє уникнути кристалізаційних тріщин.
|
|
|
 На рис. 8.10 показано одночасний вплив марганцю, вуглецю і кремнію на схильність до кристалізаційних тріщин, викликаних сіркою. Як видно з рисунка, чим більше відношення
На рис. 8.10 показано одночасний вплив марганцю, вуглецю і кремнію на схильність до кристалізаційних тріщин, викликаних сіркою. Як видно з рисунка, чим більше відношення  , тим більший вміст у металі шва [ Si + С ] можна допускати, не побоюючись утворення тріщин. Виходячи із цього, одержимо, що вмісту сірки у металі шва 0,03% при відношенні
, тим більший вміст у металі шва [ Si + С ] можна допускати, не побоюючись утворення тріщин. Виходячи із цього, одержимо, що вмісту сірки у металі шва 0,03% при відношенні  =25 повинна відповідати концентрація [ Мп ] = 0,75% і [ С + Si ] = 0,5.
=25 повинна відповідати концентрація [ Мп ] = 0,75% і [ С + Si ] = 0,5.
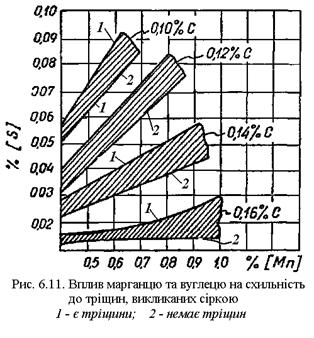
Про те ж свідчать дані, отримані співробітниками Інституту електрозварювання ім. Е. О. Патона і представлені частково на рис. 8.11. Як видно з цих даних, підвищений вміст вуглецю у металі шва збільшує небезпеку появи у ньому кристалізаційних тріщин, викликаних сіркою.
 Зв'язування сірки вапном базується на утворенні досить міцного сульфіду кальцію, практично нерозчинного в металі. Процес іде за реакцією
Зв'язування сірки вапном базується на утворенні досить міцного сульфіду кальцію, практично нерозчинного в металі. Процес іде за реакцією
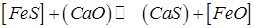 . (240) (8.26)
. (240) (8.26)
Константа рівноваги реакції (8.26) росте зі збільшенням температури, тобто процес інтенсивніше розвивається вправо, убік утворення (CaS). При цьому краще розкиснення металу і введення в шлак окису кальцію буде сприяти зменшенню вмісту в металі [ FeS ].
Збільшення вмісту в шлаку (CaО) приводить до росту константи розподілу 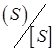 , що забезпечує більш повний перехід сірки із металу в шлак. Поряд з відзначеним установлено, що наявність кремнію й алюмінію в металі значно прискорює процес його десульфурації, причому сірка видаляється одночасно з киснем. Очевидно, це є наслідком як прямого випаровування сірки у видгляді Al2S3 (температура сублімації дорівнює 1550° С), SiS (температура сублімації дорівнює 940° С), так і включення її до складу жужільних часток, що утворяться.
, що забезпечує більш повний перехід сірки із металу в шлак. Поряд з відзначеним установлено, що наявність кремнію й алюмінію в металі значно прискорює процес його десульфурації, причому сірка видаляється одночасно з киснем. Очевидно, це є наслідком як прямого випаровування сірки у видгляді Al2S3 (температура сублімації дорівнює 1550° С), SiS (температура сублімації дорівнює 940° С), так і включення її до складу жужільних часток, що утворяться.
Фосфор і його видалення з металу шва. Фосфор, як і сірка, є шкідливою домішкою, що погіршує механічні властивості сталі і викликає її холодоламкість.
У сталях фосфор утворює частково розчинні у фериті фосфіди двох видів:
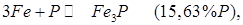
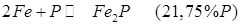 .
.
Фосфор відноситься до числа сильно ліквуючих домішок, тобто таких, котрі дуже нерівномірно розподіляються в металі. Ліквацію фосфору підсилює вуглець. При цьому можливе утворення легкоплавкої евтектики потрійного типу Fe — Р — С, що ще більше знижує міцність металу.
Видалення фосфору зі зварювальної ванни базується на його окиснюванні і наступному зв'язуванні фосфорного ангідриду в міцну комплексну сполуку, що легко видаляється зі шлаком. По зростаючій силі спорідненості до фосфорного ангідриду P2O5 основні й амфотерні оксиди можуть бути розташовані у наступний ряд:
|
|
|
Fе2О3 → Аl2O3 → FeО→ MnО → MgО → CaО.
Як видно, найбільш активними оксидами стосовно фосфорного ангідриду є CaО, MgО і MnО.
Окиснювання фосфору відбувається у зварювальній ванні у відповідності з наступними реакціями:
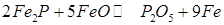 (241) (8.27)
(241) (8.27)
або
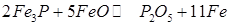 . (242) (8.28)
. (242) (8.28)
Потім йде процес зв'язування фосфорного ангідриду. Найбільш активний процес
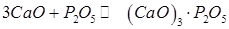 (243) (8.29)
(243) (8.29)
чи
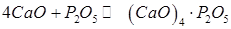 . (244) (8.30)
. (244) (8.30)
Менш активні процеси
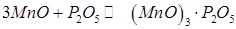 (245) (8.31)
(245) (8.31)
чи
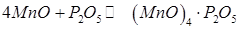 . (246) (8.32)
. (246) (8.32)
У загальному виді, об'єднавши, наприклад, рівняння (241) і (242) з (243) і (244), одержимо
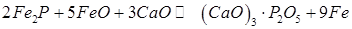 (247) (8.33)
(247) (8.33)
і
 . (248) (8.34)
. (248) (8.34)
Константа рівноваги для реакції (8.33)
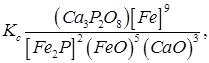
відкіля, припускаючи [Fe] ≈ 1, одержимо
 (249) (8.35)
(249) (8.35)
Аналогічно можна вирішити і рівняння (8.34) відносно [Fе3Р]. Отже, з виразу (8.35) випливає, що при даній концентрації фосфору в зварювальній ванні повнота його видалення в шлак буде залежати від вмісту в шлаку:
а) вільних оксидів (CaО) і (FeО), зі збільшенням вмісту яких реакції (8.33) і (8.34) зрушуються вправо, тобто у напрямку очищення металу від фосфору;
б) комплексної сполуки, що зв'язує фосфор, наприклад, (СаО)3×Р2O5, а також (CaО)4×P2O5; зменшення їхнього вмісту в шлаку сприяє очищенню металу від фосфору. Це досягається розведенням шлаків відповідними нейтральними добавками, наприклад плавиковим шпатом, що одночасно розріджує шлак, а також підвищує його загальну реакційну здатність.
Таким чином, основні шлаки можуть забезпечити необхідне очищення металу шва від фосфору. Кислі шлаки значно гірше видаляють фосфор з металу. Наявні в них основні оксиди СаО і МnО, а також FeО зв'язані в силікати, що викликає зсув реакцій (8.33) і (8.34) уліво. При цьому збільшується вміст фосфору в металі шва і гальмується його видалення в шлак. Константа рівноваги реакцій (8.33) і (8.34) із ростом температури зменшується, що свідчить про інтенсифікацію реакції переходу фосфору зі шлаку в метал. Тому при знижених температурах варто очікувати більш активного переходу фосфору в шлак; у цьому сенсі короткі шлаки є ефективнішими за довгі.
|
|
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1478; Нарушение авторских прав?; Мы поможем в написании вашей работы!