
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Спектры многоэлектронных атомов. Рентгеновские спектры
|
|
|
|
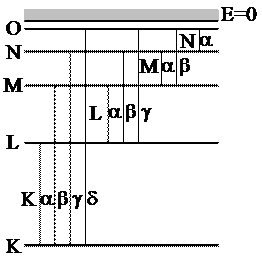 Многоэлектронные атомы имеют вакантные места для электронов только во внешних электронных оболочках. Переходы электронов с ближайших возбужденных уровней энергии на основной уровень дают обычные (оптические) спектры испускания и поглощения (эти спектры обратимы). А что будет, если каким-либо образом вырвать электрон из внутренних оболочек? На образующиеся вакантные места во внутренних слоях переходят электроны из внешних слоев. При этом происходит электромагнитное излучение рентгеновского диапазона. Рентгеновский спектр будет линейчатым (спектр испускания). Рентгеновский спектр в виде совокупности монохроматических линий носит название характеристического излучения, т.к. зависит только от вещества анода (в отличие от тормозного излучения).
Многоэлектронные атомы имеют вакантные места для электронов только во внешних электронных оболочках. Переходы электронов с ближайших возбужденных уровней энергии на основной уровень дают обычные (оптические) спектры испускания и поглощения (эти спектры обратимы). А что будет, если каким-либо образом вырвать электрон из внутренних оболочек? На образующиеся вакантные места во внутренних слоях переходят электроны из внешних слоев. При этом происходит электромагнитное излучение рентгеновского диапазона. Рентгеновский спектр будет линейчатым (спектр испускания). Рентгеновский спектр в виде совокупности монохроматических линий носит название характеристического излучения, т.к. зависит только от вещества анода (в отличие от тормозного излучения).
Подобно оптическим спектрам, это излучение состоит из нескольких серий, резко отличающихся по длине волны: 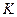 -,
-, 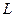 -,
-,  -,
-, 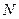 - и
- и 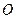 - серии. Каждая серия насчитывает небольшое число линий, обозначаемых буквами
- серии. Каждая серия насчитывает небольшое число линий, обозначаемых буквами  ,
, 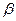 ,
,  и т.д. Название серий отражает их связь с электронными оболочками атомов. В атомах тяжелых элементов, например, в Pt оболочки
и т.д. Название серий отражает их связь с электронными оболочками атомов. В атомах тяжелых элементов, например, в Pt оболочки 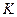 ,
, 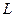 ,
,  ,
, 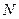 заполнены, электроны внутренних оболочек сильно связаны с ядром, и поэтому для их удаления с оболочки необходимо затрачивать большую энергию (для Pt: K – 78000 эВ).
заполнены, электроны внутренних оболочек сильно связаны с ядром, и поэтому для их удаления с оболочки необходимо затрачивать большую энергию (для Pt: K – 78000 эВ).
Исследование характеристических рентгеновских спектров позволяет непосредственно определить, по каким стационарным состояниям распределены электроны в атомах различных веществ.
В 1913 г. английский физик К.Мозли, проследив, как изменяется длина волны и, соответственно, частота рентгеновских лучей линий  и
и 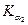 (переходы с
(переходы с 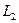 и
и  ) у различных элементов, установил связь между частотой линий рентгеновского спектра и атомным номером элемента
) у различных элементов, установил связь между частотой линий рентгеновского спектра и атомным номером элемента  :
:
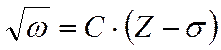 , где
, где 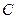 и
и 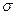 - постоянные,
- постоянные,
т.е. корень квадратный из частоты является линейной функцией атомного номера.
 Очевидно, что структура рентгеновских спектров и закон Мозли отражают закономерности электронных состояний внутренних оболочек многоэлектронных атомов. Анализ рентгеновских спектров позволяет написать:
Очевидно, что структура рентгеновских спектров и закон Мозли отражают закономерности электронных состояний внутренних оболочек многоэлектронных атомов. Анализ рентгеновских спектров позволяет написать:
для 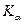 и
и 
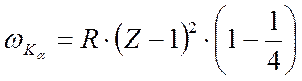 и
и  ,
,
для 
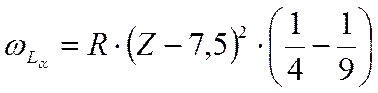 ,
,
где  - постоянная Ридберга.
- постоянная Ридберга.
.
Строгое доказательство закона Мозли дать невозможно. Он носит приближенный характер. Можно дать лишь грубую интерпретацию закона, сведя проблему к одноэлектронной задаче. Такой подход вполне удовлетворительно объясняет результаты для 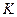 - и
- и 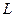 -серий и позволяет установить физический смысл постоянной
-серий и позволяет установить физический смысл постоянной 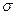 . Экспериментально установлено, что линии с частотами, определяемыми сериальной формулой, совпадают с линиями, испускаемыми при переходе электрона, находящегося в поле заряда
. Экспериментально установлено, что линии с частотами, определяемыми сериальной формулой, совпадают с линиями, испускаемыми при переходе электрона, находящегося в поле заряда 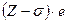 с уровня
с уровня  на уровень
на уровень  . Тогда можно написать:
. Тогда можно написать:
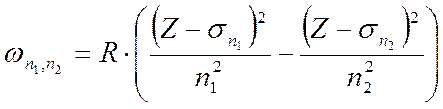 .
.
В этом случае легко понять смысл констант 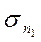 и
и 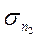 - это поправки на экранирующее действие электронов, ослабляющих притяжение данного электрона ядром. Приближенно можно написать
- это поправки на экранирующее действие электронов, ослабляющих притяжение данного электрона ядром. Приближенно можно написать
 ,
,
где  - постоянная экранирования.
- постоянная экранирования.
Несмотря на приближенность, закон Мозли позволяет установить однозначное соответствие между 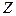 атома и частотой линии соответствующей серии. Это связано дискретностью изменения
атома и частотой линии соответствующей серии. Это связано дискретностью изменения 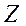 (
(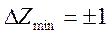 ). Поэтому закон Мозли используется для определения порядкового номера элементов, а также для определения состава сложных веществ по их характеристическому излучению (рентгеновский микроанализ).
). Поэтому закон Мозли используется для определения порядкового номера элементов, а также для определения состава сложных веществ по их характеристическому излучению (рентгеновский микроанализ).
При возбуждении атома – удалении электрона с одной из внутренних оболочек – возникает та или иная серия: при выбивании электронов из 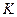 -оболочек атомов анода возникает
-оболочек атомов анода возникает 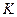 -серия, причем, сразу вся. Кроме того,
-серия, причем, сразу вся. Кроме того, 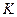 -серия обязательно сопровождается остальными сериями. Это связано с тем, что различные переходы осуществляются с различной вероятностью, определяемой правилом отбора
-серия обязательно сопровождается остальными сериями. Это связано с тем, что различные переходы осуществляются с различной вероятностью, определяемой правилом отбора 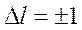 ,
, 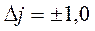 .
.
Из экспериментальных исследований спектров поглощения рентгеновских лучей в различных веществах установлено:
1)  при увеличении энергии кванта рентгеновских лучей коэффициент поглощения монотонно уменьшается, но при определенной энергии кванта, соответствующей характеристической линии поглощения, резко возрастает, а затем вновь плавно убывает;
при увеличении энергии кванта рентгеновских лучей коэффициент поглощения монотонно уменьшается, но при определенной энергии кванта, соответствующей характеристической линии поглощения, резко возрастает, а затем вновь плавно убывает;
2) установлено, что линии поглощения группируются в серии, причем количество линий в каждой серии не зависит от природы элемента, но зависит от типа серии и составляет: для 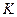 - 1, для
- 1, для 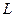 - 3, для
- 3, для  - 5, для
- 5, для 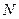 - 7 и т.д. Таким образом спектры поглощения, как и спектры излучения подтверждают квантовую структуру электронных состояний:
- 7 и т.д. Таким образом спектры поглощения, как и спектры излучения подтверждают квантовую структуру электронных состояний: 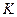 - слой имеет одиночный уровень энергии,
- слой имеет одиночный уровень энергии, 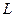 - слой имеет три подуровня
- слой имеет три подуровня  - слой – 5 и т.д.
- слой – 5 и т.д.
Чем же обусловлены указанные числа линий поглощения рентгеновских лучей в каждой серии? Почему эти числа одни и те же у всех элементов?
 -оболочка
-оболочка
 ;
; 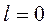 ;
; 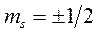 ;
; 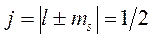 -
- 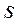 -орбиталь (1 пик поглощения).
-орбиталь (1 пик поглощения).
 -оболочка
-оболочка
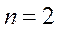 ;
;  ;
; 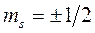 ;
; 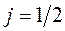 -
-  -орбиталь;
-орбиталь;
 ;
;  ;
; 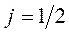 -
- 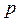 -орбиталь; (3 пика поглощения)
-орбиталь; (3 пика поглощения)
 -
- 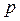 -орбиталь.
-орбиталь.
 -оболочка
-оболочка
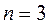 ;
; 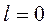 ;
;  ;
;  -
-  -орбиталь;
-орбиталь;
 ;
;  ;
; 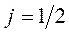 -
- 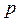 -орбиталь;
-орбиталь;
 -
- 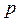 -орбиталь; (5 пиков поглощения)
-орбиталь; (5 пиков поглощения)
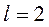 ;
;  ;
; 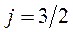 -
-  -орбиталь;
-орбиталь;
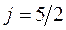 -
-  -орбиталь.
-орбиталь.
Таким образом, спектры поглощения рентгеновских лучей замечательно подтверждают, что у всех атомов (кроме H) разным орбиталям одного и того же слоя соответствует разная энергия: каждой орбитали соответствует один пик поглощения, каждому слою – одна серия; количеству разных типов орбиталей – количество пиков в серии.
Механизм возникновения характеристического излучения связан не с внешними, а с внутренними электронами атома. Поэтому независимо от соединения, в который входит данный атом, его характеристический спектр будет неизменным, и по нему можно идентифицировать элемент.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1791; Нарушение авторских прав?; Мы поможем в написании вашей работы!