
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет процессов идеального газа
|
|
|
|
Все многообразие процессов можно разделить на следующие группы: изохорные, изобарные, изотермические, адиабатные, политропные.
 |
Цель расчета процесса – определение параметров в начальном и конечном состояниях, а также теплоты и работы процесса. Расчет процессов, как правило, сопровождается графическим представлением их в p - v- и T - s- диаграммах (рис. 4.1, рис. 4.2).
Изобары в T - s- диаграмме располагаются эквидистантно между собой
и с увеличением давления смещаются влево; построены на основании уравнения (4.18).
Изохоры в T - s- диаграмме располагаются также эквидистантно между собой и с увеличением объема смещаются вправо; для построения изохор использовалась формула (4.17).
Изотермы в p - v- диаграмме представляют собой симметричные гиперболы, отражающие связь между p и v в изотермическом процессе,
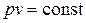 . .
| (4.28) |
Адиабаты (изоэнтропы) в p-v -диаграмме – несимметричные гиперболы, отражающие связь между давлением и объемом в адиабатном обратимом процессе,
 , ,
| (4.29) |
располагаются круче изотерм, т. к. показатель адиабаты k >1.
4.2.1. Изобарный процесс
Дано: параметры начального состояния p 1, v 1, удельный объем конечного состояния v 2.
Определить: недостающие термические параметры T 1 и T 2, работу и теплоту процесса (w, l, q).
Изобарный процесс, построенный на основании исходных данных
(p 1, v 1, v 2), в p - v- и T - s- диаграммах представлен на рис. 4.3 и 4.4.
 |
Из уравнения состояния для точки 1 определяется температура T 1:
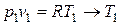 .
.
Сравнение уравнений состояния для точек 1 и 2 при условии
p 1= p 2 = p = const,
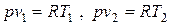
дает связь между v и T в изобарном процессе:
 , ,
| (4.30) |
из которой можно определить искомую температуру T 2.
Формулы для расчета работы и теплоты изобарного процесса легко получить на основании уравнений
|
|
|
 . .
|
Отсюда при p = const имеем
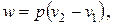
| (4.31) |
 , ,
| (4.32) |
 . .
| (4.33) |
Работа и теплота изобарного процесса в диаграммах представлены заштрихованными площадями. Работа положительна (w > 0), т. к. v 2 > v 1, теплота подводится (q > 0), поскольку s 2 > s 1.
Из T - s- диаграммы следует: изменение энтальпии (Dh) любого процесса, осуществляемого в интервале температур T 1 – T 2, характеризуется площадью под изобарой в этом интервале температур.
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 660; Нарушение авторских прав?; Мы поможем в написании вашей работы!