
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Физические свойства свободного кремния
|
|
|
|
Физические свойства свободного кремния
Аллотропные модификации кремния:
1) Кристаллический кремний – вещество серебристо-серого цвета с металлическим блеском, кристаллическая решетка типа алмаза; является полупроводником.
2) Аморфный кремний – порошок бурого цвета.
Свободный кремний можно получить прокаливанием с магнием мелкого белого песка, который представляет собой диоксид кремния:
SiO2 + 2 Mg ═ 2 MgO + Si
При этом образуется бурый порошок аморфного кремния.
Кремний растворим в расплавленных металлах. При медленном охлаждении раствора кремния в цинке или в алюминии кремний выделяется в виде хорошо образованных кристаллов октаэдрической формы. Кристаллический кремний обладает стальным блеском.
В большинстве реакций кремний выступает в роли восстановителя:
Si0 - 4ē → Si+4
В реакциях с металлами кремний – окислитель:
Si0 + 4ē → Si-4
1) В химическом отношении кремний, особенно, кристаллический, малоактивен; при комнатной температуре он непосредственно соединяется только с фтором. При нагревании аморфный кремний легко соединяется с кислородом, галогенами и серой.
Si + O2 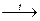 SiO2
SiO2
Si + 2F2 = SiF4
Si + 2HaI2 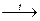 SiHaI4
SiHaI4
Si + 2S 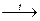 SiS2
SiS2
3Si + 2N2 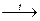 Si3N4
Si3N4
Si + C 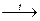 SiC
SiC
2) С водородом кремний непосредственно не реагирует.
3) Кислоты, кроме, смеси фтористоводородной и азотной (плавиковой), не действуют на кремний:
3 Si + 4 HNO3 + 18 HF ═ 3 H2SiF6 + 4 NO + 8 H2O
4) Реагирует с растворами щелочей с образованием силикатов и выделением водорода:
Si + 2 КОН + Н2O = К2SiO3 + 2 H2 ↑
5) При высокой температуре кремний вступает в соединение со многими металлами, образуя силициды. Например, при нагревании диоксида кремния с избытком металлического магния восстанавливающийся кремний соединяется с магнием, образуя силицид магния Mg2Si:
4 Mg + SiO2 = Mg2Si + 2 MgO
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 1050; Нарушение авторских прав?; Мы поможем в написании вашей работы!