
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
S: Сумма коэффициентов в уравнении реакции 3 страница
+: межмолекулярное окисление-восстановление;
-: внутримолекулярное окисление-восстановление;
-: диспропорционирование;
-: особый случай.
I: {{201}}
S: Тип окислительно-восстановительной реакции
2CrCl3 + 3H2O2 + 10NaOH ® 2Na2CrO4 + 6NaCl + 8H2O
+: межмолекулярное окисление-восстановление;
-: внутримолекулярное окисление-восстановление;
-: диспропорционирование;
-: особый случай.
I: {{202}}
S: Общая сумма коэффициентов в молекулярном уравнении реакции
CrCℓ3 + H2O2 + NaOH ® Na2CrO4 + NaCℓ + H2O равна
-: 40;
+: 31;
-: 35;
-: 24.
I: {{203}}
S: Общая сумма коэффициентов в молекулярном уравнении реакции
PbO2 + H2O2 + CH3COOH ® Pb(CH3COO)2 + O2 + H2O равна
-: 10;
+: 8;
-: 12;
-: 14.
I: {{204}}
S: Общая сумма коэффициентов в молекулярном уравнении реакции
FeSO4 + HJO3 + H2SO4 = Fe2(SO4)3 + J2 + H2O равна
-: 30;
+: 29;
-: 18;
-: 32.
I: {{205}}
S: Вещество, при взаимодействии с которым аммиак является восстановителем
+: оксид меди(II);
-: вода;
-: азотная кислота;
-: хлороводород.
I: {{206}}
S: Общая сумма коэффициентов в молекулярном уравнении реакции
NH3 + Br2 → N2 + NH4Br равна
-: 10;
-: 22;
+: 18;
-: 12.
I: {{207}}
S: Окислитель в уравнении окислительно-восстановительной реакции NH3 + Br2 → N2 + NH4Br
-: NH3;
+: Br2;
-: N2;
-: NH4Br.
I: {{208}}
S: Восстановитель в уравнении окислительно-восстановительной реакции
NH3 + Br2 → N2 + NH4Br
+: NH3;
-: Br2;
-: N2;
-: NH4Br.
I: {{209}}
S: Восстановителем и окислителем в реакции 3KNO3 + 8Aℓ + 5KOH + 2H2O = 8KAℓO2 + 3NH3 являются
+: KNO3;
-: KOH;
-: H2O;
+: Aℓ.
I: {{210}}
S: Восстановителем и окислителем в реакции 3KNO3 + 8Aℓ + 5KOH + 2H2O = 8KAℓO2 + 3NH3 являются
+: KNO3, Aℓ;
-: KOH, Aℓ;
-: H2O, Aℓ;
-: KOH, H2O.
I: {{211}}
S:Наименее окисленное состояние азот имеет в соединении
-: NO;
-: N2;
+: NH3;
-: N2O5.
I: {{212}}
S: Наименее окисленное состояние сера имеет в соединении
-: S;
-: SO2;
-: SO3;
+: H2S.
I: {{213}}
S: Окислителем в реакции 2CrCℓ3 + 16KOH + 3Br2 = 2K2CrO4 + 6KBr + 6KCℓ + 8H2O является
-: CrCℓ3;
-: KOH;
+: Br2;
-: K2CrO4.
I: {{214}}
S: Установите соответствие между типом реакции и её выражением
L1: нейтрализации
L2: окислительно-восстановительная
L3:
L4:
R1: NaOH + HCℓ = NaCℓ + H2O
R2: 3K2MnO4 + 2H2SO4 = 2KMnO4 + MnO2 + 2K2SO4 + 2H2O
R3: AgNO3 + HCℓ = ↓AgCℓ + HNO3
R4: CaCO3 = CaO + CO2↑
I: {{215}}
S: Установите соответствие между типом реакции и её выражением
L1: разложения
L2: окислительно-восстановительная
L3:
L4:
R1: CaCO3 = CaO + CO2↑
R2: 3K2MnO4 + 2H2SO4 = 2KMnO4 + MnO2 + 2K2SO4 + 2H2O
R3: AgNO3 + HCℓ = ↓AgCℓ + HNO3
R4: NaOH + HCℓ = NaCℓ + H2O
I: {{216}}
S: Коэффициент, стоящий перед окислителем в уравнении реакции
FeSO4 + HNO3 = Fe(NO3)3 + H2SO4 + NO2 + H2O равен
-: 5;
-: 7;
-: 10;
+: 1.
I: {{217}}
S: Диспропорционирование – это реакции, в которых
+: происходит изменение степеней окисления одного и того же элемента в одной и той же молекуле;
-: окислитель и восстановитель находятся в разных молекулах;
-: окислитель и восстановитель разные элементы, находящиеся в одной и той же молекуле;
-: окислитель и среда, либо восстановитель и среда одно вещество.
I: {{218}}
S: Эквивалентная масса восстановителя в реакции 2Na + Cℓ2 = 2NaCℓ равна
-: 35,5 г/моль;
+: 23,0 г/моль;
-: 11,5 г/моль;
-: 71,0 г/моль.
I: {{219}}
S: Межмолекулярное окисление-восстановление – это реакции, в которых
-: происходит изменение степеней окисления одного и того же элемента в одной и той же молекуле;
+: окислитель и восстановитель находятся в разных молекулах;
-: окислитель и восстановитель разные элементы, находящиеся в одной и той же молекуле;
-: окислитель и среда, либо восстановитель и среда одно вещество.
I: {{220}}
S: Внутримолекулярное окисление-восстановление – это реакции, в которых
-: происходит изменение степеней окисления одного и того же элемента в одной и той же молекуле;
-: окислитель и восстановитель находятся в разных молекулах;
+: окислитель и восстановитель разные элементы, находящиеся в одной и той же молекуле;
-: окислитель и среда, либо восстановитель и среда одно вещество.
I: {{221}}
S: Окислитель и восстановитель в реакции Au + HNO3 + 3HCℓ = AuCℓ3 + NO + 2H2O
+: HNO3, Au;
-: HCℓ, Au;
-: NO, Au;
-: HCℓ, NO.
I: {{222}
S: Окислитель и восстановитель в реакции H2S + 4Cℓ2 + 4H2O = 8HCℓ + H2SO4
-: H2S, H2O;
+: Cℓ2, H2S;
-: H2O, Cℓ2;
-: NO, H2O.
I: {{223}}
S: Коэффициент перед восстановителем в уравнении реакции
H2SO4 + KNO2 + KMnO4 = KNO3 + MnSO4 + K2 SO4 + H2O равен
-: 1;
+: 5;
-: 10;
-: 2.
I: {{224}}
S: Коэффициент перед окислителем в уравнении реакции
H2SO4 + KNO2 + KMnO4 = KNO3 + MnSO4 + K2 SO4 + H2O равен
-: 1;
-: 5;
-: 10;
+: 2.
I: {{225}}
S: Установите соответствие между типом реакции и её определением
L1: диспропорционирования
L2: межмолекулярное окисление-восстановление
L3:
L4:
R1: реакции, в ходе которых происходит изменение степеней окисления одного и того же элемента в одной и той же молекуле
R2: реакции, в ходе которых окислитель и восстановитель находятся в разных молекулах
R3: реакции, в ходе которых окислитель и восстановитель (атомы разных элементов) находятся в составе одной и той же молекулы
R4: реакции, в которых окислитель и среда, либо восстановитель и среда одно вещество
I: {{226}}
S: Вещество, придающее раствору оранжевый цвет
-: Сr2(SO4)3;
+: K2Cr2O7;
-: K2CrO4;
-: CrCℓ3.
I: {{227}}
S: Установите соответствие между исходными веществами и продуктами окислительно-восстановительной реакции
L1: Fe + HCℓ
L2: Fe + H2SO4(разб.)
L3: Fe + H2SO4(конц.)
L4:
L5:
L6:
R1: FeCℓ2 + H2
R2: FeSO4 + H2
R3: Fe2(SO4)3 + SO2 + H2O
R4: FeHCℓ
R5: FeSO3 + H2O
R6: FeCℓ3
I: {{228}}
S: Установите соответствие между исходными веществами и продуктами окислительно-восстановительной реакции
L1: Fe + HCℓ
L2: Fe + Cℓ2
L3: Fe + H2SO4(конц.)
L4:
L5:
L6:
R1: FeCℓ2 + H2
R2: FeCℓ3
R3: Fe2(SO4)3 + SO2 + H2O
R4: FeHCℓ
R5: FeSO3 + H2O
R6: FeSO4 + H2
I: {{229}}
S: Коэффициент, стоящий перед окислителем в уравнении реакции
PbO2 + HNO3 + Mn(NO3)2 = Pb(NO3)2 + HMnO4 +H2O равен
+: 5;
-: 7;
-: 2;
-: 6.
I: {{230}}
S: Сумма коэффициентов в уравнении реакции PbS + HNO3 = S + Pb(NO3)2 + NO + H2O равна
-: 21;
+: 23;
-: 25;
-: 20.
I: {{231}}
S: В реакции K2Cr2O7 +3KNO2 +H2SO4 =Cr2(SO4)3 +3KNO3 +K2SO4 +4H2O окисляется ион
+: NO2-;
-: Cr2O72-;
-: SO42-;
-: NO3-.
I: {{232}}
S: Коэффициент перед окислителем в уравнении реакции 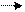 H2S + HNO3(разб) S+NO+H2O равен
H2S + HNO3(разб) S+NO+H2O равен
+: 2;
-: 1;
-: 3;
-: 4.
I: {{233}}
S: Общая сумма коэффициентов в уравнении реакции KClO3 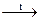 КCl + O2 равна
КCl + O2 равна
+: 7;
-: 8;
-: 6;
-: 9.
I: {{234}}
S: Схема процесса, в котором происходит окисление азота
+: NH4+→ N2;
-: NО3-→ NО2-;
-: N2 → NН3;
-: N2 → NН4+;
I: {{234}}
S: Эквивалент перманганата калия, если ион MnO4 - восстанавливается до Mn2+ , равен ___ моль
+: 1/5;
-: 1;
-: ½;
-: 1/3.
|
|
Дата добавления: 2014-10-31; Просмотров: 1973; Нарушение авторских прав?; Мы поможем в написании вашей работы!