
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
S: Установите соответствие между воздействующим фактором и смещением равновесия
|
|
|
|
S: Установите соответствие между воздействующим фактором и смещением равновесия
L1: повышение давления
S: Установите соответствие между воздействующим фактором и смещением равновесия
L2: повышение температуры
L3:
L4:
R1: в сторону меньшего объёма системы
R2: в сторону эндотермического процесса
R3: в сторону экзотермического процесса
R4: в сторону конечных продуктов реакции
I: {{126}}
L1: повышение давления
L2: повышение концентрации исходных веществ
L3:
L4:
R1: в сторону меньшего объёма системы
R2: в сторону конечных продуктов реакции
R3: в сторону эндотермического процесса
R4: не сместится
I: {{127}}
L1: понижение температуры
L2: повышение концентрации конечных продуктов
L3:
L4:
R1: в сторону экзотермического процесса
R2: в сторону исходных веществ
R3: в сторону меньшего объёма системы
R4: не сместится
I: {{128}}
S: Реакции, для которых изменение объёма системы не вызовет смещения равновесия
-: 2СO(г) + O2(г) ↔ 2СO2(г);
-: N2O4(г) ↔ 2NO2(г);
+: H2(г) + J2(г) ↔ 2HJ(г);
+: С(графит) + О2(г) ↔ СО2(г).
I: {{129}}
S: Энтальпия образования жидкого сероуглерода равна, если при взаимодействии 1 моль углерода и 2 моль серы поглотилось 88,7 кДж тепла
-: –88,7 кДж/моль;
-: +177,4 кДж/моль;
-: –177,4 кДж/моль;
+: +88,7 кДж/моль.
I: {{130}}
S: Стандартная энтропия в ряду соединений NO → NO2 → N2O4
-: не изменяется;
-: убывает;
-: изменяется периодически;
+: возрастает.
I: {{131}}
S: Термическая устойчивость в ряду соединений LiCℓ → NaCℓ → KCℓ
(ΔHо(LiCℓ) = –408,3 кДж/моль; ΔHо(NaCℓ) = -411,1 кДж/моль;
ΔHо(KCℓ) = -436,7 кДж/моль)
-: не изменяется;
-: убывает;
-: изменяется периодически;
+: возрастает.
I: {{132}}
S: Изменение энергии Гиббса (ΔGо) реакции H2(г) + Cℓ2 (г) = 2HCℓ(г); ΔHо= –184,62 кДж
|
|
|
(Sо(HCℓ(г)) = 186,79 Дж/моль×K; Sо(H2) = 130,52 Дж/моль×K; Sо(Cℓ2) = 222,98 Дж/моль×K) равно
-: +190,6 кДж;
+: –190,6 кДж;
-: +95,3 кДж;
-: –95,3 кДж.
I: {{133}}
S: Скорость прямой реакции CO(г) + Сℓ2(г) ↔ CОCℓ2(г) при повышении концентрации оксида углерода(II) в 2 раза увеличится
+: в 2 раза;
-: в 4 раза;
-: в 6 раз;
-: в 8 раз.
I: {{134}}
S: Температурный коэффициент скорости реакции равен ###, если при увеличении температуры на 40° скорость реакции возросла в 81 раз (запишите число с точностью до целых)
+: 3
I: {{135}}
S: Выражение константы равновесия реакции CO2(г) + 4H2(г) ↔ CН4(г) + 2Н2O(г)
-: Кр = [CO2]/[Н2O];
+: Кр = [CН4][H2O]2/[CO2][H2 ]4;
-: Кр = 1/[CO2];
-: Кр = [H2O]2/[CO2][H2 ]4.
I: {{136}}
S: Равновесие реакции 2NО(г) + О2(г) ↔ 2NО2(г) при повышении давления сместится
+: в сторону конечных продуктов;
-: в сторону исходных веществ;
-: не сместится;
-: пройдет через максимум.
I: {{137}}
S: Система, которая лишена возможности обмена веществом или энергией с внешней средой и имеет постоянный объём, называется
+: изолированной;
-: закрытой;
-: открытой;
-: полиморфной.
I: {{138}}
S: Повышение температуры реакционной смеси на 10о приводит к увеличению скорости химической реакции чаще всего в 2 – 4 раза и реже в 5 – 7 раз – это формулировка
+: правила Вант-Гоффа;
-: принципа Ле-Шателье;
-: закона Гесса;
-: постулата Бора.
I: {{139}}
S: Установите соответствие между функцией состояния и её характеристикой
L1: внутренняя энергия
L2: энтальпия
L3:
L4:
R1: общий запас энергии в системе
R2: теплосодержание системы
R3: мера упорядоченности системы или мера беспорядка
R4: смещение равновесия
I: {{140}}
S: Установите соответствие между функцией состояния и её характеристикой
L1: энтальпия
L2: энтропия
L3:
L4:
R1: теплосодержание системы
R2: мера упорядоченности системы или мера беспорядка
R3: общий запас энергии в системе
R4: смещение равновесия
|
|
|
I: {{141}}
S: Установите соответствие между функцией состояния и её характеристикой
L1: внутренняя энергия
L2: энтропия
L3:
L4:
R1: общий запас энергии в системе
R2: мера упорядоченности системы или мера беспорядка
R3: теплосодержание системы
R4: смещение равновесия
I: {{142}}
S: Энтальпия образования газообразного сероводорода равна, если при взаимодействии 1 моль водорода и 1 моль серы выделилось 20,6 кДж тепла
-: –10,3 кДж/моль;
-: +10,3 кДж/моль;
+: –20,6 кДж/моль;
-: +20,6 кДж/моль.
I: {{143}}
S: Изменение энергии Гиббса (ΔGо) реакции
Fe2O3(кр) + 3H2(г) = 2Fe(кр) + 3H2O (г); ΔHо= +96,61 кДж
(Sо(Fe2O3(кр)) = 87,45 Дж/моль×K; Sо(H2(г)) = 130,52 Дж/моль×K;
Sо(H2O (г)) = 188,72 Дж/моль×K; Sо(Fe(кр)) = 27,15 Дж/моль×K) равно
+: +54,46 кДж;
-: –87,45 кДж;
-: +27,15 кДж;
-: +188,72 кДж.
I: {{144}}
S: Скорость прямой реакции 2Н2(г) + O2(г) ↔ 2H2O(г) при повышении давления в 3 раза возрастет
-: в 3 раза;
-: в 9 раз;
+: в 27 раз;
-: в 12 раз.
I: {{145}}
S: Скорость реакции возрастет, если температуру повысить на 20о (γ = 2)
-: в 2 раза;
+: в 4 раза;
-: в 6 раз;
-: в 8 раз.
I: {{146}}
S: Выражение константы равновесия реакции CuO(тв) + H2(г) ↔ Cu(тв) + Н2O(г)
-: Кр = [Cu]/[Н2O];
+: Кр = [H2O]/[H2];
-: Кр = 1/[Cu];
-: Кр = [H2O]/[CuO][H2].
I: {{147}}
S: Равновесие реакции N2(г) + О2(г) ↔ 2NO(г) при повышении давления сместится
-: вправо;
-: влево;
+: не сместится;
-: имеет минимум.
I: {{148}}
S: Происходящее изменение в системе СО(г) + Н2(г) ↔ СН3OН(г), ΔHо < 0 при уменьшении давления
+: уменьшится выход продуктов;
-: увеличится выход продуктов;
-: равновесие останется неизменным;
-: равновесие сместится неоднозначно.
I: {{149}}
S: Совокупность всех гомогенных частей системы, одинаковых по составу и по всем физическим и химическим свойствам, не зависящим от количества вещества и отделенных друг от других частей системы некоторой поверхностью раздела, называется
+: фазой;
-: компонентом;
-: системой;
-: веществом.
I: {{150}}
S: Совокупность промежуточных состояний, через которые проходит система, называют
+: путем процесса;
-: параметром состояния;
-: кинетическим порядком реакции;
-: формальным порядком реакции.
I: {{151}}
S: Химическая реакция, протекающая в сторону образования продуктов реакции, называется ###
+: прям#$#.
I: {{152}}
S: Энтальпия образования газообразного оксида серы(IV) равна, если при взаимодействии 1 моль кислорода и 1 моль серы выделилось 296,9 кДж тепла
|
|
|
-: +105,3 кДж/моль;
-: +148,5 кДж/моль;
-: –210,6 кДж/моль;
+: –296,9 кДж/моль.
I: {{153}}
S: Изменение энергии Гиббса (ΔGо) реакции H2(г) + ½О2(г) = H2О(г); ΔHо = –241,8 кДж
(Sо(H2(г)) = 130,5 Дж/моль×K; Sо(О2(г)) = 205,0 Дж/моль×K; Sо(H2О(г)) = 188,7 Дж/моль×K) равно
-: -257,2 кДж;
-: –87,9 кДж;
-: +87,9 кДж;
+: –91,45 кДж.
I: {{154}}
S: Скорость прямой реакции 2H2(г) + O2(г) ↔ 2H2O(г) изменится, если уменьшить давление системы в 3 раза
-: увеличится в 8 раз;
-: увеличится в 6 раз;
+: уменьшится в 27 раз;
-: уменьшится в 9 раз.
I: {{155}}
S: Температуру (град) газообразной смеси следует повысить для увеличения скорости реакции в 32 раза (γ = 2) на
-: 20;
-: 30;
-: 40;
+: 50.
I: {{156}}
S: Выражение константы равновесия реакции N2(г) + 3H2(г) ↔ 2NН3(г)
-: Кр = [H2]3/[NH3]2;
-: Кр = [N2][H2]3/[NH3]2;
+: Кр = [NH3]2/ [N2][H2]3;
-: Кр = [NH3]2/ [N2].
I: {{157}}
S: Направление смещения равновесие реакции: 2SО2(г) + О2(г) ↔ 2SО3(г) при повышении давления
-: не сместится;
+: в сторону конечных продуктов;
-: в сторону исходных веществ;
-: имеет максимум.
I: {{158}}
S: Фаза, состоящая из одного химически индивидуального вещества, называется
+: простой;
-: грязной;
-: сложной;
-: смешанной.
I: {{159}}
S: Химическая реакция, протекающая в сторону исходных продуктов реакции, называется
+: обратной;
-: прямой;
-: гомогенной;
-: гетерогенной.
I: {{160}}
S: Энтальпия образования газообразного этилена равна, если при взаимодействии 2 моль водорода и 2 моль углерода поглотилось 52,3 кДж тепла
-: –26,15 кДж/моль;
+: +52,3 кДж/моль;
-: –52,3 кДж/моль;
-: +26,15 кДж/моль.
I: {{161}}
S: Изменение энергия Гиббса (ΔGо) реакции O2(г) + 2CO(г) = 2CO2(г); DH°= –566 кДж
(Sо(CO2(г)) = 213,66 Дж/моль×K; Sо(O2(г)) = 205,04 Дж/моль×K;
Sо(CO(г)) = 197,55 Дж/моль×K) равно
-: +197,55 кДж;
+: –514,5 кДж;
-: –205,04 кДж;
-: +213,66 кДж.
I: {{162}}
S: Скорость реакции увеличится в ### раз, если начальная концентрация исходных веществ в системе CO + Cℓ2 «COCℓ2 была равна (моль/дм3): [CO] = 0,3; [Cℓ2] = 0,2, а через некоторое время концентрации [CO] повысили до 0,6, а [Cℓ2] – до 1,2
-: 6;
|
|
|
-: 8;
+: 12;
-: 10.
I: {{163}}
S: Температуру газообразной смеси следует повысить для увеличения скорости реакции в 16 раз (γ = 2) на
-: 20°;
-: 30°;
+: 40°;
-: 50°.
I: {{164}}
S: Выражение константы равновесия реакции C(графит) + Н2O(г) ↔ CO(г) + H2(г)
+: Кр = [CO][H2 ]/[Н2O];
-: Кр = [H2O]/[CO][H2];
-: Кр = 1/[CO2];
-: Кр = [H2O]/[C][H2].
I: {{165}}
S: Направление смещения равновесие реакции: СО2(г) + C(графит) ↔ 2СО(г) при повышении давления
-: не сместится;
-: в сторону конечных продуктов;
+: в сторону исходных веществ;
-: имеет линейный характер.
I: {{166}}
S: Фаза, содержащая два или больше индивидуальных веществ, называется
-: простой;
-: чистой;
-: сложной;
+: смешанной.
I: {{167}}
S: Всякое изменение состояния системы, связанное с изменением хотя бы одного параметра, называется
+: термодинамическим процессом;
-: скоростью реакции;
-: механизмом реакции;
-: путем процесса.
I: {{168}}
S: Состояние, наступающее при равенстве скоростей прямой и обратной реакции, называется ###
+: равновесн#$#
I: {{169}}
S: Энтальпия образования жидкой воды равна, если при взаимодействии 2 моль водорода и 1 моль кислорода выделилось 571,66 кДж тепла
+: –285,83 кДж/моль;
-: +285,83 кДж/моль;
-: –571,66 кДж/моль;
-: +571,66 кДж/моль.
I: {{170}}
S: Изменение энергия Гиббса (ΔGо) реакции
O2(г) + 4HCℓ(г) «2H2O(г) + 2Cℓ2(г); DHо = –114,5 кДж
(Sо(H2O(г)) = 188,72 Дж/моль×K; Sо(Cℓ2(г)) = 222,98 Дж/моль×K;
Sо(HCℓ(г)) = 186,79 Дж/моль×K; Sо(O2(г)) = 205,04 Дж/моль×K) равно
-: +91,67 кДж;
+: –76,12 кДж;
-: +76,12 кДж;
-: –91,45 кДж.
I: {{171}}
S: Скорость прямой реакции Н2(г) + Сℓ2(г) ↔ 2HСℓ(г) при повышении давления в 6 раз возрастет
-: в 6 раз;
+: в 36 раз;
-: в 28 раз;
-: в 12 раз.
I: {{172}}
S: Реакция протекает при любой температуре, если
+: ΔН < 0 и ΔS > 0;
-: ΔН > 0 и ΔS > 0;
-: ΔН < 0 и ΔS < 0;
-: ΔН > 0 и ΔS < 0.
I: {{173}}
S: Реакция невозможна при
-: ΔН < 0 и ΔS > 0;
-: ΔН > 0 и ΔS > 0;
-: ΔН < 0 и ΔS < 0;
+: ΔН > 0 и ΔS < 0.
I: {{174}}
S: Реакция может протекать только при низкой температуре, если
-: ΔН < 0 и ΔS > 0;
-: ΔН > 0 и ΔS > 0;
+: ΔН < 0 и ΔS < 0;
-: ΔН > 0 и ΔS < 0.
I: {{175}}
S: Реакция может протекать только при высокой температуре, если
-: ΔН < 0 и ΔS > 0;
+: ΔН > 0 и ΔS > 0;
-: ΔН < 0 и ΔS < 0;
-: ΔН > 0 и ΔS < 0.
I: {{176}}
S: Абсолютная энтропия в ряду однотипных соединений по мере усложнения атомов, входящих в состав молекул, ###
+: растет.
I: {{177}}
S: Энтропия твёрдого вещества ###, чем энтропия вещества в аморфном и стеклообразном состоянии
+: меньш#$#.
I: {{178}}
S: Энтропия вещества в аморфном и стеклообразном состоянии ###, чем энтропия твёрдого вещества
+: больш#$#.
I: {{179}}
S: Изменение энтропии в ходе реакции образования соединения из простых веществ называется
+: энтропией образования вещества;
-: энтропией разложения вещества;
-: энтропией гидролиза вещества;
-: энтропией возгонки вещества.
I: {{180}}
S: Процессы, для которых ΔS > 0
+: расширения газов;
+: испарение жидкости;
-: сжатие газов;
-: конденсация веществ.
I: {{181}}
S: Процессы, для которых ΔS > 0
+: растворение кристаллических веществ;
+: испарение жидкости;
-: сжатие газов;
-: кристаллизация веществ.
I: {{182}}
S: Процессы, для которых ΔS > 0
+: расширения газов;
+: растворение кристаллических веществ;
-: сжатие газов;
-: конденсация веществ.
I: {{183}}
S: Процессы, для которых ΔS < 0
-: расширения газов;
-: испарение жидкости;
+: сжатие газов;
+: конденсация веществ.
I: {{184}}
S: Процессы, для которых ΔS < 0
-: растворение кристаллических веществ;
-: испарение жидкости;
+: сжатие газов;
+: кристаллизация веществ.
I: {{185}}
S: Процессы, для которых ΔS < 0
-: расширения газов;
-: растворение кристаллических веществ;
+: сжатие газов;
+: конденсация веществ.
I: {{186}}
S: Выражение константы равновесия реакции CH4(г) + 2H2O(г) ↔ CO2(г) + 4H2(г)
+: Кр = [CO2][H2]4/[CH4][H2O]2;
-: Кр = [CH4]/[CO2][H2O]2;
-: Кр = [CH4][H2O]2/[CO2][H2]4;
-: Кр = [H2O]2/[H2]4.
I: {{187}}
S: Температуру (град) газообразной смеси следует повысить для увеличения скорости реакции в 16 раз (γ = 4) на
+: 20;
-: 30;
-: 40;
-: 50.
I: {{188}}
S: Реакция, в которой увеличение объёма системы вызовет смещения равновесия в сторону, исходных веществ
+: 2SO2(г) + O2(г) ↔ 2SO3(г);
-: N2O4(г) ↔ 2NO2(г);
-: H2(г) + Сℓ2(г) ↔ 2HCℓ(г);
-: H2(г) + J2(г) ↔ 2HJ(г).
I: {{189}}
S: Реакции, в которых увеличение объёма системы не вызовет смещения равновесия
-: 2SO2(г) + O2(г) ↔ 2SO3(г);
-: N2O4(г) ↔ 2NO2(г);
+: H2(г) + Сℓ2(г) ↔ 2HCℓ(г);
+: H2(г) + J2(г) ↔ 2HJ(г).
I: {{190}}
S: Равновесие реакции СО(г) + 3H2(г) ↔ СH4(г) + H2O(г) при увеличении давления сместится
+: в сторону конечных продуктов;
-: в сторону исходных веществ;
-: не сместится;
-: проходит через максимум концентраций.
I: {{191}}
S: Вещества, входящие в состав фаз, называются
+: компонентами;
-: смесями;
-: соединениями;
-: солями.
I: {{192}}
S: Состояние системы с неравномерно изменяющимися во времени термодинамическими параметрами называется
+: неравновесным;
-: равновесным;
-: подвижным;
-: гибким.
I: {{193}}
S: Отношение произведений равновесных молярных концентраций продуктов реакции к исходным веществам в степени их стехиометрических коэффициентов называется
+: константой равновесия;
-: константой скорости реакции;
-: скоростью химической реакции;
-: термодинамическим процессом.
I: {{194}}
S: Тепловой эффект химической реакции при р=const равен разности между суммой энтальпий образования продуктов реакции и суммой энтальпий образования исходных веществ с учетом стехиометрических коэффициентов – это формулировка
+: следствия из закона Гесса;
-: следствия из закона Рауля;
-: принципа Ле-Шателье;
-: правила Вант-Гоффа.
I: {{195}}
S: Энтальпия образования газообразного оксида азота(I) равна, если при взаимодействии 1 моль азота и 0,5 моль кислорода поглотилось 82 кДж тепла
-: –164 кДж/моль;
-: +164 кДж/моль;
-: –82 кДж/моль;
+: +82 кДж/моль.
I: {{196}}
S: Изменение энергия Гиббса (ΔGо) реакции N2(г) + 3H2(г) = 2NH3(г); ΔHо= –92,4 кДж
(Sо(N2(г)) = 200,00 Дж/моль×K; Sо(NH3(г)) = 192,66 Дж/моль×K; Sо(H2(г)) = 130,52 Дж/моль×K) равно
-: +30,90 кДж;
+: –30,90 кДж;
-: +10,45 кДж;
-: –10,45 кДж.
I: {{197}}
S: Скорость прямой реакции 4NH3(г) +5O2(г) ↔ 4NO(г) + 6H2O(г) изменится, если увеличить давление системы в 2 раза
-: в 2 раза;
-: в 16 раз;
+: в 512 раз;
-: в 216 раз.
I: {{198}}
S: Температуру (град) газообразной смеси следует повысить на ###, чтобы скорость реакции увеличилась в 8 раз (γ = 2)
-: 20;
+: 30;
-: 40;
-: 50.
I: {{199}}
S: Выражение константы равновесия реакции 2NO(г) + O2(г) ↔ 2NO2(г)
-: Кр = [NO]/[NO2];
-: Кр = [O2]/[NO]2;
+: Кр = [NO2]2/[O2][NO]2;
-: Кр = [O2][NO]2/ [NO2].
I: {{200}}
S: Реакция, в которой увеличение объёма системы не вызовет смещения равновесия
-: 2SO2(г) + O2(г) ↔ 2SO3(г);
-: N2O4(г) ↔ 2NO2(г);
+: H2(г) + Сℓ2(г) ↔ 2HCℓ(г) ;
-: N2(г) + 3H2(г) ↔ 2NH3(г).
I: {{201}}
S: Реакции, в которых увеличение объёма системы не вызовет смещения равновесия
-: 2СO(г) + O2(г) ↔ 2СO2(г);
+: С(графит) + O2(г) ↔ СO2(г);
+: H2(г) + F2(г) ↔ 2HF(г) ;
-: 2NO(г) + O2(г) ↔ 2NO2(г).
I: {{202}}
S: Состояние системы, если термодинамические параметры со временем самопроизвольно не изменяются и сохраняют одинаковое значение в пределах каждой фазы, а энергия минимальна, называется ###
+: равновесн#$#.
I: {{203}}
S: Если на систему, находящуюся в состоянии химического равновесия, оказать какое-либо воздействие, то равновесие сместиться в таком направлении, что оказанное воздействие будет ослаблено – это формулировка
-: правила Вант-Гоффа;
+: принципа Ле-Шателье;
-: закона действия масс;
-: закона Гульдберга и Вааге.
I: {{204}}
S: Установите соответствие между путем процесса и параметром, который постоянен
L1: изобарный
L2: изохорный
L3:
L4:
R1: давление
R2: объём
R3: температура
R4: концентраци
I: {{205}}
S: Установите соответствие между путем процесса и параметром, который постоянен
L1: изобарный
L2: изотермический
L3:
L4:
R1: давление
R2: температура
R3: объём
R4: концентрация
I: {{206}}
S: Установите соответствие между путем процесса и параметром, который постоянен
L1: изохорный
L2: изотермический
L3:
L4:
R1: объём
R2: температура
R3: давление
R4: концентрации
I: {{207}}
S: Следствие из закона, которому соответствует математическое выражение
DНо = å∆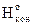 – åD
– åD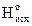
+: Гесса;
-: Рауля;
-: Авогадро;
-: Менделеева.
I: {{208}}
S: Правило, которому соответствует математическое выражение υt2 = υt1γt2 – t1/10
+: Вант-Гоффа;
-: Клечковского;
-: Паули;
-: Рауля.
I: {{209}}
S: Закон, которому соответствует математическое выражение υ = k [A]a[B]b
+: действия масс;
+: Гульдберга и Вааге;
-: Гесса;
-: Планка.
I: {{210}}
S: Энтальпия образования газообразного аммиака равна, если при взаимодействии 3 моль водорода и 1 моль азота выделилось 91,88 кДж тепла
-: –91,88 кДж/моль;
-: +45,94 кДж/моль;
+: –45,94 кДж/моль;
-: +91,88 кДж/моль.
I: {{211}}
S: Изменение энтропии (ΔSо) реакции N2(г) + 3H2(г) = 2NH3(г)
(Sо(N2(г)) = 200,00 Дж/моль×K; Sо(NH3(г)) = 192,66 Дж/моль×K; Sо(H2(г)) = 130,52 Дж/моль×K) равно
-: +192,66 Дж/K;
+: –206,20 Дж/K;
-: +287,9 Дж/K;
-: –345,2 Дж/K.
I: {{212}}
S: Скорость прямой реакции Н2(г) + Cℓ2(г) ↔ 2HCℓ(г) при повышении давления в 4 раза возрастет
-: в 4 раза;
-: в 8 раз;
+: в 16 раз;
-: в 12 раз.
I: {{213}}
S: Температурный коэффициент скорости реакции равен ###, если при увеличении температуры на 20о скорость реакции возросла в 16 раза
-: 2;
-: 3;
+: 4;
-: 5.
I: {{214}}
S: Константа равновесия реакции C(графит) + 2N2O (г) ↔ 2N2(г) + СO2(г) равна, если равновесные концентрации (моль/дм3): [N2] = 0,4; [N2O] = 0,2; [CO2] = 0,06
-: 0,16;
-: 0,40;
+: 0,24;
-: 0,32.
I: {{215}}
S: Реакция, химическое равновесие которой сместится в сторону образования исходных веществ, как при понижении температуры, так и повышении давления
-: N2(г) + O2(г) ↔ 2NO(г); ΔHo < 0;
+: 2SО3(г) ↔ 2SO2(г) + O2(г) ; ΔHo > 0;
-: 4HCℓ(г) + O2(г) ↔ 2Cℓ2(г) + 2H2O(ж); ΔHo < 0;
-: Н2(г) + Cℓ2(г) ↔ 2HCℓ(г); ΔHo < 0.
I: {{216}}
S: Реакция, химическое равновесие которой сместится в сторону образования исходных веществ, как при повышении температуры, так и понижении давления
-: N2(г) + O2(г) ↔ 2NO(г); ΔHo < 0;
-: 2SО3(г) ↔ 2SO2(г) + O2(г) ; ΔHo > 0;
+: 4HCℓ(г) + O2(г) ↔ 2Cℓ2(г) + 2H2O(ж); ΔHo < 0;
-: Н2(г) + Cℓ2(г) ↔ 2HCℓ(г); ΔHo < 0.
I: {{217}}
S: Реакция, химическое равновесие которой сместится в сторону образования конечных продуктов при понижении температуры и давления
-: 2Н2(г) + O2(г) ↔ 2Н2O(г); ΔHо < 0;
+: 2SО3(г) ↔ 2SO2(г) + O2(г) ; ΔHо > 0;
-: 4HCℓ(г) + O2(г) ↔ 2Cℓ2(г) + 2H2O(ж); ΔHо < 0;
-: Н2(г) + Cℓ2(г) ↔ 2HCℓ(г); ΔHо < 0.
I: {{218}}
S: Реакции, химическое равновесие которых сместится в сторону образования конечных продуктов при повышении температуры
-: N2(г) + O2(г) ↔ 2NO(г); ΔHo < 0;
+: 2SО3(г) ↔ 2SO2(г) + O2(г) ; ΔHo > 0;
-: 4HCℓ(г) + O2(г) ↔ 2Cℓ2(г) + 2H2O(ж); ΔHo < 0;
-: Н2(г) + Cℓ2(г) ↔ 2HCℓ(г); ΔHo < 0.
I: {{219}}
S: Термическая устойчивость в ряду соединений H2Те → H2Se → H2S
-: не изменяется;
-: убывает;
-: изменяется периодически;
+: возрастает.
I: {{220}}
S: Термическая устойчивость в ряду соединений HgO → CdO → ZnO
(ΔHо(ZnO) = –350,6 кДж/моль; ΔHо(CdO) = -260,0 кДж/моль;
ΔHо(HgO) = +90,9 кДж/моль)
-: не изменяется;
-: убывает;
-: изменяется периодически;
+: возрастает.
I: {{221}}
S: Стандартная энтропия в ряду соединений СO2 → CO → Cu2O → CuO
-: не изменяется;
+: убывает;
-: изменяется периодически;
-: возрастает.
I: {{222}}
S: Термическая устойчивость в ряду соединений КCℓ → NaCℓ → LiCℓ
(ΔHо(LiCℓ) = –408,3 кДж/моль; ΔHо(NaCℓ) = -411,1 кДж/моль;
ΔHо(KCℓ) = -436,7 кДж/моль)
-: не изменяется;
+: убывает;
-: изменяется периодически;
-: возрастает.
I: {{223}}
S: Скорость прямой реакции CO(г) + Сℓ2(г) ↔ CОCℓ2(г) при повышении концентрации хлора в 2 раза увеличится
+: в 2 раза;
-: в 4 раза;
-: в 6 раз;
-: в 8 раз.
I: {{224}}
S: Скорость прямой реакции 2H2(г) + O2(г) ↔ 2H2O(г) изменится, если увеличить давление системы в 3 раза
-: увеличится в 8 раз;
-: уменьшится в 6 раз;
+: увеличится в 27 раз;
-: уменьшится в 9 раз.
I: {{225}}
S: Температуру газообразной смеси следует понизить для уменьшения скорости реакции в 32 раза (γ = 2) на ____ градусов
-: 20;
-: 30;
-: 40;
+: 50.
I: {{226}}
S: Веществом, энтальпия образования которого считается 0 кДж/моль, является
+: О2(г);
-: SO2(г);
-: HCl (г);
-: лед.
I: {{227}}
S: Веществом, энтальпия образования которого считается 0 кДж/моль, является
+: Н2(г);
-: SO2(г);
-: HCl (г);
-: лед.
I: {{228}}
S: Веществом, энтальпия образования которого считается 0 кДж/моль, является
+: Fe(тв);
-: SO2(г);
-: HCl (г);
-: лед.
I: {{229}}
S: В соответствии с термохимическим уравнением
FeO(тв) + H2(г)= Fe(тв) + H2O(г), ΔгНо = 23 кДж для получения 560 г железа необходимо затратить ___ кДж тепла
+: 230;
-: 115;
-: 345;
-: 460.
I: {{230}}
S: Для получения 22,4 дм3 (н.у.) аммиака по реакции N2(r)+3H2(r) =2NH3(r)—93,2 кДж, требуется затратить ___ кДж теплоты
+: 46,6;
-: 23,3;
-: 69,9;
-: 93,2.
I: {{231}}
S: Для системы N2 (r) +3H2 (r) ↔ 2NH3 (r) уравнение константы равновесия имеет вид
+: Kр= [NH3]2/[N2][H2]3;
-: Kр= [N2][H2]3/[NH3]2;
-: Kр= [NH3]2/[H2]3;
-: Kр= [NH3]2/[N2].
I: {{232}}
S: Для смещения равновесия в системе CaCО3(тв) ↔ CaO(тв)+CO2(г), ΔrH0 больше 0
+: увеличить температуру;
-: понизить температуру;
-: увеличить давление;
-: уменьшить давление.
I: {{233}}
S: Для смещения равновесия в системе МgO(г) + СО2(г) = МgСO3(т), ΔНо < 0 в сторону продуктов реакции необходимо
-: увеличить температуру;
+: понизить температуру;
-: увеличить давление;
-: уменьшить давление.
I: {{234}}
S: Для смещения равновесия в системе SO2(г) + Сl2(г) = SO2Cl2(т), ΔНо < 0 в сторону продуктов реакции необходимо
-: увеличить температуру;
+: понизить температуру;
-: увеличить давление;
-: уменьшить давление.
I: {{235}}
S: Для смещения равновесия в системе 2NOCl(r) ↔ 2NO(r)+ 2Cl2(r), ∆rH>0 в сторону исходного вещества необходимо
-: увеличить температуру;
+: понизить температуру;
-: увеличить давление;
-: уменьшить давление.
I: {{236}}
S: Для увеличения выхода аммиака по уравнению реакции
N2(г) + 3Н2(г) = 2NН3(г), ΔгНо < 0 необходимо
-: увеличить температуру;
+: понизить температуру;
-: увеличить давление;
-: уменьшить давление.
I: {{237}}
S: Для увеличения выхода продуктов реакции реакция
2Pb(NO3)2 (тв) = 2PbO(тв) + 4NO2(г) + O2(г), ΔгНо>0 необходимо
+: увеличить температуру;
-: понизить температуру;
-: увеличить давление;
-: уменьшить давление.
I: {{238}}
S: Энтальпия образования оксида кальция равна____кДж/моль, если при окислении 10 граммов кальция выделяется 160 кДж теплоты
+: -640;
-: -320;
-: +640;
-: +320.
I: {{239}}
S: Количество затраченного тепла равно ___ кДж, если при разложении перхлората калия, согласно термохимическому уравнению KClO4(тв) 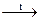 КCl(тв) + 2O2(г), ΔНо = 33 кДж, образовалось 10 моль кислорода
КCl(тв) + 2O2(г), ΔНо = 33 кДж, образовалось 10 моль кислорода
+: 165;
-: 320;
-: 640;
-: 80.
I: {{240}}
S:Температурный коэффициент скорости реакции равен, если при увеличении температуры от 20 оС до 50 оС скорость реакции увеличивается в 8 раз
+: 2;
-: 3;
-: 4;
-: 5.
I: {{241}}
S: Объём кислорода (дм3), который необходимо затратить для получения 1132 кДж тепла по реакции 2NO(г) + O2(г) = 2NO2(г); ΔгНо = – 566 кДж
+: 44,8;
-: 22,4;
-: 11,2;
-: 56,0.
I: {{242}}
S: Количество теплоты (кДж), которую требуется затратить для получения 17 г сероводородв по реакции H2(г) +S(т) = H2S(г) – 21 кДж
+: 11,5;
-: 23,0;
-: 34,5;
-: 5,8.
I: {{243}}
S: Энтальпия образования (кДж/моль) оксида кальция равна, если при окислении 10 граммов кальция выделяется 160 кДж теплоты
+: -640;
-: -320;
-: -480;
-: -760.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1527; Нарушение авторских прав?; Мы поможем в написании вашей работы!