
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Качественной характеристикой в полярографии является
|
|
|
|
Количественной характеристикой в полярографии является
| a)p | Количество электричества |
| b)p | Потенциал пика |
| c)p | Время накопления |
| d)p | Потенциал полуволны |
| e)p | Сила диффузионного тока |
| Вопрос №676 |
Инверсионную вольтамперометрию применяют для определения:
| a)p | больших концентраций ионов |
| b)p | органических соединений |
| c)p | трудновосстанавливающихся ионов |
| d)p | ионов с переменной степенью окисления |
| e)p | малых концентраций обратимо восстанавливающихся ионов |
| Вопрос №677 |
Уравнение полярографической волны:
| a)p | E = E1/2 - RT/nF . ln(Id -I)/I |
| b)p | E = E1/2 + RT/nF . lg(Id -I)/I |
| c)p | E = E1/2 + RT/nF . lnI/(Id -I) |
| d)p | E = E1/2 + RT/nF . ln(Id -I)/I |
| e)p | E = Eo + RT/nF . ln(Id -I)/I |
| Вопрос №678 |
На величину предельного диффузионного тока в полярографии не влияет:
| a)p | природа фонового электролита |
| b)p | площадь электрода |
| c)p | температура |
| d)p | концентрация вещества |
| e)p | потенциал электрода |
| Вопрос №679 |
Вид кривой амперометрического титрования, если в электродную реакцию вступает титрант:
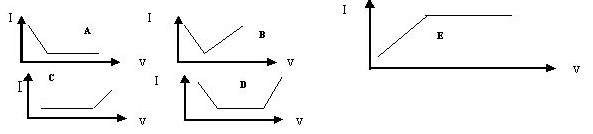
| a)p | B |
| b)p | C |
| c)p | E |
| d)p | A |
| e)p | D |
| Вопрос №680 |
Одновременное определение двух веществ методом классической полярографии возможно при разности Е1/2 этих веществ не менее:
| a)p | 0,04 В |
| b)p | 0,3 В |
| c)p | 0,4 В |
| d)p | 0,2 В |
| e)p | 0,1 В |
| Вопрос №681 |
Потенциал индикаторного электрода при амперометрическом титровании должен быть:
| a)p | меньше Е1/2 |
| b)p | равен Е1/2 |
| c)p | больше Е1/2 |
| d)p | значительно меньше Е1/2 |
| e)p | любым |
| Вопрос №682 |
| a)p | Время накопления |
| b)p | Потенциал полуволны |
| c)p | Потенциал накопления |
| d)p | Количество электричества |
| e)p | Сила диффузионного тока |
| Вопрос №683 |
Вид кривой амперометрического титрования смеси двух веществ:
|
|
|

| a)p | A |
| b)p | Е |
| c)p | C |
| d)p | D |
| e)p | B |
| Вопрос №684 |
Вид кривой амперометрического титрования, если в электродную реакцию вступает определяемое вещество:

| a)p | B |
| b)p | A |
| c)p | E |
| d)p | D |
| e)p | C |
| Вопрос №685 |
Коэффициент диффузии (D) входит в уравнение Ильковича в степени:
| a)p | |
| b)p | 2/3 |
| c)p | 1/2 |
| d)p | 1/6 |
| e)p | 1/3 |
| Вопрос №686 |
Измеряемым параметром в полярографии является:
| a)p | потенциал |
| b)p | электропроводимость |
| c)p | количество электричества |
| d)p | сопротивление раствора |
| e)p | сила тока |
| Вопрос №687 |
В полярографии не используется следующий метод определения концентрации веществ:
| a)p | расчет по уравнению Ильковича |
| b)p | градуировочного графика |
| c)p | отношения площадей пиков |
| d)p | стандартных растворов |
| e)p | добавок |
| Вопрос №688 |
На величину потенциала полуволны не влияет:
| a)p | природа фонового электролита |
| b)p | концентрация комплексообразователя |
| c)p | концентрация вещества |
| d)p | природа вещества |
| e)p | рН раствора |
| Вопрос №689 |
Координаты кривой амперометрического титрования:
| a)p | I = f(V) |
| b)p | E = f(I) |
| c)p | I = f(E) |
| d)p | E = f(V) |
| e)p | I = f(R) |
| Вопрос №690 |
Генераторным электродом в кулонометрическом титровании кислот является:
| a)p | платиновый анод |
| b)p | каломельный электрод |
| c)p | платиновый катод |
| d)p | графитовый анод |
| e)p | графитовый катод |
| Вопрос №691 |
Генераторным электродом в кулонометрическом титровании тиосульфата натрия является:
| a)p | платиновый катод |
| b)p | платиновый анод |
| c)p | каломельный электрод |
| d)p | графитовый катод |
| e)p | графитовый анод |
| Вопрос №692 |
Количество электричества при постоянной силе тока рассчитывают по формуле:
| a)p | Q = 10-It |
| b)p | Q = lgI . t |
| c)p | Q = I . t |
| d)p | Q = I/t |
| e)p | Q = t/I |
| Вопрос №693 |
В основе кулонометрии лежат законы:
|
|
|
| a)p | Ома |
| b)p | Ампера |
| c)p | Кулона |
| d)p | Фарадея |
| e)p | Вольта |
| Вопрос №694 |
Индикатором при кулонометрическом титровании кислот служит:
| a)p | метиловый оранжевый |
| b)p | фенолфталеин |
| c)p | мурексид |
| d)p | крахмал |
| e)p | дифениламин |
| Вопрос №695 |
Измеряемым параметром в кулонометрии является:
| a)p | потенциал |
| b)p | сопротивление раствора |
| c)p | количество электричества |
| d)p | электропроводимость |
| e)p | сила тока |
| Вопрос №696 |
Индикатором при кулонометрическом титровании тиосульфата натрия служит:
| a)p | метиловый оранжевый |
| b)p | дифениламин |
| c)p | фенолфталеин |
| d)p | крахмал |
| e)p | мурексид |
| Вопрос №697 |
Скорость кулонометрического титрования можно изменять изменением:
| a)p | потенциала генераторного электрода |
| b)p | потенциала вспомогательного электрода |
| c)p | времени генерирования титранта |
| d)p | силы генераторного тока |
| e)p | скорости перемешивания раствора |
| Вопрос №698 |
Выражение объединенного закона Фарадея:
| a)p | m=nF/QM |
| b)p | m=QM/nF |
| c)p | m=QF/nM |
| d)p | m=MF/nQ |
| e)p | m=Qn/MF |
| Вопрос №699 |
В кулонометрическом титровании вместо объема титранта используется:
| a)p | скорость перемешивания раствора |
| b)p | потенциал генераторного электрода |
| c)p | время генерирования титранта |
| d)p | потенциал вспомогательного электрода |
| e)p | сила тока |
| Вопрос №700 |
Стеклянный электрод можно применять в потенциометрическом титровании при использовании реакций:
| a)p | комлексообразования |
| b)p | осаждения |
| c)p | кислотно-основных |
| d)p | окислительно-восстановительных |
| Вопрос №701 |
Серебряный электрод – это электрод:
| a)p | первого рода |
| b)p | третьего рода |
| c)p | мембранный |
| d)p | второго рода |
| Вопрос №702 |
Каломельный электрод – это электрод:
| a)p | мембранный |
| b)p | первого рода |
| c)p | третьего рода |
| d)p | второго рода |
| Вопрос №703 |
Вид дифференциальной кривой титрования, соответствующей титрованию смеси хлорида натрия и хлорида калия раствором нитрата серебра:

| a)p | B |
| b)p | C |
| c)p | D |
| d)p | A |
| Вопрос №704 |
К мембранным электродам относится:
| a)p | стеклянный |
| b)p | хлоридсеребряный |
| c)p | платиновый |
| d)p | водородный |
|
|
|
| Вопрос №705 |
Условие подготовки стеклянного электрода к работе:
| a)p | электрод выдерживают в разбавленной (0,1 н.) кислоте |
| b)p | электрод предварительно не подготавливают |
| c)p | электрод выдерживают в концентрированном растворе щелочи |
| d)p | электрод выдерживают в воде |
| Вопрос №706 |
К электродам второго рода относятся:
| a)p | платиновый, серебряный |
| b)p | медный, хингидронный |
| c)p | стеклянный, водородный |
| d)p | каломельный, хлоридсеребряный |
| Вопрос №707 |
Вид дифференциальной кривой титрования лимонной кислоты, имеющей К1 = 7,4.10-4 , К2 = 2,2.10-5 , К3 = 4,0.10-7:

| a)p | C |
| b)p | D |
| c)p | A |
| d)p | B |
| Вопрос №708 |
При потенциометрическом определении веществ точку эквивалентности устанавливают по дифференциальной, а не по интегральной кривой титрования потому, что:
| a)p | дифференциальная кривая позволяет более точно установить точку эквивалентности |
| b)p | преимуществ в установлении точки эквивалентности нет |
| c)p | предпочтение определяется выбором систем электродов |
| d)p | интегральную кривую титрования можно построить только для титрования сильных электролитов |
| Вопрос №709 |
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 838; Нарушение авторских прав?; Мы поможем в написании вашей работы!