
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные химические реакции процесса горения. Теплота сгорания
|
|
|
|
При исследовании процесса горения различных веществ важно знать уравнение химической реакции этого процесса.
При построении уравнения поступают следующим образом: горючее вещество и участвующий в горении воздух помещают в левой части уравнения, в правой – образующиеся продукты горения.
Целый ряд горючих веществ и материалов может быть определён формулой 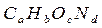 , где индексы a, b, c, d отвечают количеству атомов углерода, водорода, кислорода, азота в молекуле горючего вещества. Известно, что воздух представляет собой смесь газов, основными компонентами которой являются азот (78%), кислород (21%), аргон (0,9%). Процентное содержание газов приведено по объёму. Аргон, как инертный газ, в процессе горения не участвует. Для простоты расчётов принимают, что воздух состоит из 21% кислорода и 79% азота, то есть на один объём кислорода в воздухе приходится 79/21=3,76 объёма азота, или на каждую молекулу кислорода приходится 3,76 молекул азота. Тогда левая часть уравнения (без учёта согласующих коэффициентов) может быть представлена в виде
, где индексы a, b, c, d отвечают количеству атомов углерода, водорода, кислорода, азота в молекуле горючего вещества. Известно, что воздух представляет собой смесь газов, основными компонентами которой являются азот (78%), кислород (21%), аргон (0,9%). Процентное содержание газов приведено по объёму. Аргон, как инертный газ, в процессе горения не участвует. Для простоты расчётов принимают, что воздух состоит из 21% кислорода и 79% азота, то есть на один объём кислорода в воздухе приходится 79/21=3,76 объёма азота, или на каждую молекулу кислорода приходится 3,76 молекул азота. Тогда левая часть уравнения (без учёта согласующих коэффициентов) может быть представлена в виде 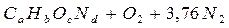 .
.
При определении продуктов сгорания нужно ориентироваться на состав горючего вещества. Углерод горючего при полном сгорании превращается в углекислый газ 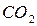 , водород - в воду
, водород - в воду 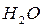 (пары воды). Азот воздуха в процессе горения участия не принимает, он целиком переходит в продукты сгорания. Содержащийся в горючем веществе кислород выделяется в виде соединений с другими элементами горючего, в рассматриваемом случае в виде, например,
(пары воды). Азот воздуха в процессе горения участия не принимает, он целиком переходит в продукты сгорания. Содержащийся в горючем веществе кислород выделяется в виде соединений с другими элементами горючего, в рассматриваемом случае в виде, например, 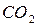 или
или 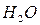 (поэтому при горении веществ, богатых кислородом, как правило, требуется меньше воздуха). Таким образом, правую часть уравнения (без учёта согласующихся коэффициентов) можно представить в виде
(поэтому при горении веществ, богатых кислородом, как правило, требуется меньше воздуха). Таким образом, правую часть уравнения (без учёта согласующихся коэффициентов) можно представить в виде  .
.
|
|
|
В дальнейшем необходимо найти согласующие коэффициенты. Согласно закону сохранения масс, масса веществ, вступивших в реакцию, должна быть равна массе веществ, полученных в результате реакции. Следовательно, число атомов одного и того же элемента в правой и левой частях уравнения должно быть одинаковым, независимо от того, в состав какого вещества этот элемент входит. Сначала уравнивают число атомов углерода, затем водорода, кислорода, азота. Окончательно рассматриваемое уравнение реакции горения будет иметь вид:
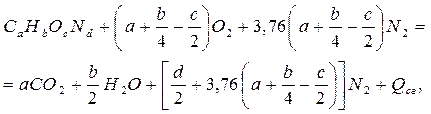 (1.33)
(1.33)
где 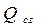 - тепловая энергия, выделяющаяся в процессе рассматриваемой реакции.
- тепловая энергия, выделяющаяся в процессе рассматриваемой реакции.
Следует отметить, что по уравнению (1.33) расчёт ведётся на один моль горючего вещества, поэтому в левой и правой частях уравнения перед 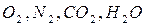 могут появиться дробные коэффициенты.
могут появиться дробные коэффициенты.
Если в состав горючего вещества, кроме углерода и водорода, входят хлор или сера, то при горении они выделяются в виде 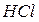 и
и 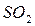 соответственно.
соответственно.
Сгорание веществ может происходить также за счёт кислорода, находящегося в составе других веществ, способных его отдавать. Такими веществами являются азотная кислота 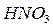 , бертолетова соль
, бертолетова соль 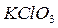 , селитры
, селитры  ,
, 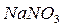 ,
, 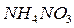 , и др. Смеси этих окислителей с горючим веществом взаимодействуют с большой скоростью, часто со взрывом [6].
, и др. Смеси этих окислителей с горючим веществом взаимодействуют с большой скоростью, часто со взрывом [6].
Количество тепла 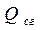 , выделяемое при полном сгорании вещества и отнесённое к единице массы (или одному молю), называется теплотой сгорания. Теплоту сгорания можно вычислить, пользуясь законом Гесса Г.Г., который является частным случаем закона сохранения энергии. Существо закона состоит в следующем: тепловой эффект химического превращения не зависит от пути, по которому протекает реакция, а зависит лишь от начального и конечного состояния системы при условии, что температура и давление (или объём) в начале и конце реакции одинаковы.
, выделяемое при полном сгорании вещества и отнесённое к единице массы (или одному молю), называется теплотой сгорания. Теплоту сгорания можно вычислить, пользуясь законом Гесса Г.Г., который является частным случаем закона сохранения энергии. Существо закона состоит в следующем: тепловой эффект химического превращения не зависит от пути, по которому протекает реакция, а зависит лишь от начального и конечного состояния системы при условии, что температура и давление (или объём) в начале и конце реакции одинаковы.
С целью пояснения рассмотрим пример вычисления теплоты сгорания метана. Реакции получения и сгорания метана можно записать в виде [6]:
|
|
|
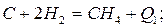 Q1=74,8 кДж
Q1=74,8 кДж

Такие же продукты образуются при сгорании водорода и углерода
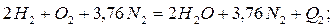 Q2=570,6 кДж
Q2=570,6 кДж
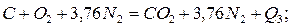 Q3=392,9 кДж
Q3=392,9 кДж
Поскольку начальные и конечные продукты в обоих случаях одинаковы, их общие тепловые эффекты согласно закону, равны, то есть
Q1+Qсг=Q2+Q3
или Qсг=Q2+Q3 -Q1 =570,6+392,9-74,8=888,7 кДж
Согласно закону Гесса Г.Г. теплота сгорания химического вещества (или смеси) равна разности между суммой теплот образования продуктов сгорания и теплотой образования сгоревшего вещества (или веществ, составляющих горючую смесь).
Теплотой образования называется тепловой эффект, получающийся при образовании одного моля вещества из свободных элементов в стандартных условиях. За стандартне условия принимают температуру 25 °С и давление 1 атм. всех веществ, участвующих в реакции. Теплоту образования химических веществ определяют по термохимическим таблицам [7]. Теплота образования продуктов сгорания:
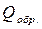 ½
½ 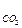 = 94,5 ккал/моль
= 94,5 ккал/моль
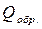 ½
½  =26,4 ккал/моль
=26,4 ккал/моль
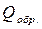 ½
½ 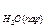 = 57,7 ккал/моль
= 57,7 ккал/моль
Следует отметить, что теплота образования простых веществ (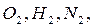 и др.) принимается равной нулю.
и др.) принимается равной нулю.
Пример. Определить теплоту сгорания углерода (С).
Решение. 1. Составляем уравнение реакции горения углерода, принимая в уравнении (1.33) значения величин а=1, b=c=d=0.
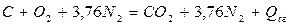
2. Находим теплоту образования углекислого газа 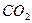 и углерода С. Согласно приведённым выше пояснениям
и углерода С. Согласно приведённым выше пояснениям
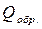 ½
½ 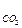 = 94,5 ккал/моль,
= 94,5 ккал/моль, 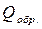 ½
½ 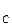 =0
=0
3. Определяем теплоту сгорания углерода

Теплоту сгорания различных веществ определяют также экспериментально в калориметрической бомбе и газовом калориметре.
Различают высшую 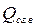 и низшую
и низшую  теплоты сгорания. Принято считать, что высшая теплота сгорания больше низшей на величину испарения влаги, находящейся в продуктах сгорания. Более строгое определение
теплоты сгорания. Принято считать, что высшая теплота сгорания больше низшей на величину испарения влаги, находящейся в продуктах сгорания. Более строгое определение 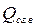 ,
,  приведено, например, в [6].
приведено, например, в [6].
Высшей теплотой сгорания называют количество тепла, выделяемое при полном сгорании единицы массы горючего вещества при условии, что содержащийся в нём водород сгорает с образованием жидкой воды (при конденсации водяного пара). Низшей теплотой сгорания называется количество тепла, выделяемое аналогично при полном сгорании единицы массы горючего вещества при условии сгорания водорода до образования водяного пара и испарении влаги горючего вещества.
|
|
|
При задании элементного состава твёрдого или жидкого горючего вещества в весовых (массовых) процентах для определения 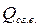 и
и  рекомендуется использовать формулы Д.И. Менделеева [6]:
рекомендуется использовать формулы Д.И. Менделеева [6]:
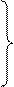
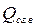 =
= 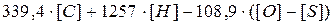
, (1.34)
 =
= 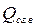
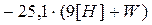
где  и
и  - высшая и низшая теплоты сгорания,
- высшая и низшая теплоты сгорания, 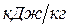 ;
;
[ C ], [ H ], [ O ], [ S ], W – содержание в горючем веществе углерода, водорода, кислорода, серы и влаги, %.
Пример. Определить низшую теплоту сгорания сернистого мазута, в состав которого входят углерод (82,5%), водород (10,65%), сера (3,1%), кислород (0,5%), влага (3%), зола (0,25%).
Решение. Искомую теплоту сгорания вычисляем по второй формуле (1.34)

Существует низший предел теплоты сгорания, ниже которого вещества становятся не способными к горению в атмосфере воздуха. Вещества являются негорючими, если они не относятся к взрывоопасным и если их теплота сгорания не превышает 2,1 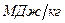 .
.
Следует отметить, что в расчетах выделения тепла в условиях реальных пожаров за величину теплоты сгорания 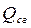 принимается
принимается 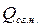 , так как образующийся при сгорании водяной пар уходит в атмосферу, не конденсируясь в воду.
, так как образующийся при сгорании водяной пар уходит в атмосферу, не конденсируясь в воду.
Известно, что при пожарах многие вещества и материалы горят с обра-зованием значительного количества сажи. Сажа (углерод) способна само-стоятельно гореть и выделять тепло. Следовательно, если при горении она образуется, то горючее вещество выделяет тепла меньше, происходит так называемый недожог. Для веществ, богатых углеродом (нефть, мазут, рубероид, бензол и др.) коэффициент недожога  составляет
составляет 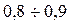 , при горении древесины
, при горении древесины  =0,85 [8].
=0,85 [8].
Размер пожара обычно характеризуется площадью пожара. Количество тепла, выделяемое с единицы площади пожара в единицу времени, называется теплотой пожара qп.
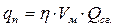 , (1.35)
, (1.35)
где qп – теплота пожара, 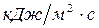 ;
; 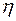 - коэффициент недожога;
- коэффициент недожога;
 – теплота сгорания,
– теплота сгорания, 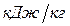 ;
; 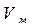 – массовая скорость выгорания,
– массовая скорость выгорания, 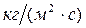 [или
[или 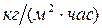 ].
].
Значения qп, 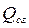 ,
, 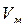 для некоторых веществ приведены в табл.3
для некоторых веществ приведены в табл.3
Таблица 3
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 2678; Нарушение авторских прав?; Мы поможем в написании вашей работы!