
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диаграммы плавкости
|
|
|
|
Диаграмма плавкости веществ с неограниченной растворимостью в жидком и полной нерастворимостью в твердом состоянии.
Этот тип диаграмм характерен для веществ, заметно отличающихся структурой кристаллов.
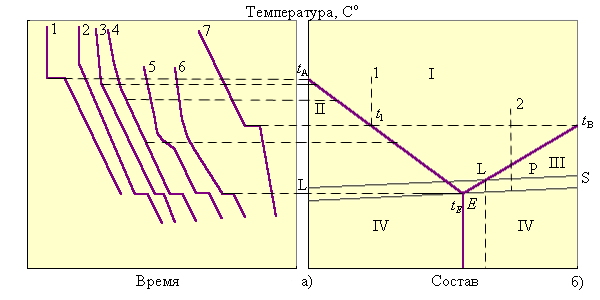
Диаграмма температура–состав строится на основании кривых охлаждения (нагревания). Кривые охлаждения – графическое изображение зависимости температуры от времени для исходных чистых веществ A и B и их смесей различного состава. Вид этих кривых свидетельствует о наличии или отсутствии фазовых превращений при некоторых определенных температурах или в интервале температур (рис. 6.11.).
|
| Рисунок 6.11. Построение диаграммы плавкости для веществ, полностью растворяющихся в жидком и нерастворяющихся в твердом состояниях: а) кривые охлаждения; б) диаграмма плавкости. |
Расплав чистого компонента можно рассматривать как растворитель. Согласно закону Рауля, добавление второго компонента (растворенного вещества) вызывает понижение температуры кристаллизации системы (раствора). При охлаждении расплава, пока в охлаждаемой системе не происходит фазовых превращений, температура расплава падает с определенной скоростью. Появление кристаллов сопровождается выделением теплоты кристаллизации и замедляет или приостанавливает падение температуры, вызывая излом или площадку на кривой охлаждения.
Из анализа кривых охлаждения (рис. 6.11а) следует, что смеси веществ при охлаждении претерпевают по два фазовых превращения, и изломы на их кривых характеризуют начало выделения из расплава кристаллов вещества A (кривая 2) или вещества B (кривая 4), а площадки – выделение эвтектической смеси, насыщенной в отношении обоих компонентов.
|
|
|
Таким образом, кристаллизация жидкой смеси в отличие от кристаллизации чистого вещества (кривые 1,5) сопровождается изменением состава жидкой фазы и лежит в некотором температурном интервале. Смесь эвтектического состава (кривая 3) кристаллизуется подобно чистым компонентам при постоянной температуре, поэтому дает монотонную кривую охлаждения с горизонтальным участком при эвтектической, наименьшей для данной системы температуре.
После окончания кристаллизации идет охлаждение отвердевшей системы до температуры окружающей среды.
Определив с помощью кривых охлаждения температуры кристаллизации для смесей различных составов, строят диаграмму состояния. Способ построения ясен из рисунка 6.11б.
На рис. 6.11б:
· I – гомофазная жидкая область (liquid – жидкий)
· II, III – гетерофазные области (расплав + твердая фаза)
· IV – гетерофазная область (Aтв + Bтв)
· E – эвтектика (состав с наименьшей t пл)
· t АE – линия ликвидуса – геометрическое место точек, отвечающих температурам начала кристаллизации компонента A
· t ВE – линия ликвидуса – геометрическое место точек, отвечающих температурам начала кристаллизации компонента B
· t A t EE t E t B – линия солидуса (solid – твердый), ниже которой существуют только твердые фазы.
Точка на диаграмме состояния, отвечающая составу образца, называется фигуративной.
Рассмотрим ход кристаллизации расплава с позиции правила фаз. Пока фигуративная точка 2 находится в гомогенной области I, никакие фазовые превращения не происходят, в системе имеет место дивариантное равновесие (С = 2 + 1 – 1 = 2), можно менять и температуру, и соотношение компонентов без изменения числа фаз. При температуре t 1 расплав становится насыщенным по компоненту A, который выкристаллизовывается по мере понижения температуры. На кривой охлаждения наблюдается излом. При этом расплав обогащается компонентом B (состав расплава изменяется по линии ликвидуса к точке Е). В системе по линии ликвидуса и в двухфазной области II имеет место моновариантное равновесие, то есть изменение температуры в указанном интервале не приводит к изменению числа фаз (С = 2 + 1 – 2 = 1). Как только мы достигнем температуры t E, расплав окажется насыщенным относительно компонента В, и тогда оба компонента, А и В, выделяются в виде механической мелкодисперсной смеси кристаллов с постоянным составом до полной кристаллизации. Этот расплав называется эвтектическим. Состав расплава не изменяется, температура тоже постоянна, и в равновесии находятся три фазы: одна жидкая и две твердые: LE и Aтв + Bтв. Следовательно, в эвтектической точке имеет место нонвариантное равновесие (С = 2 + 1 – 3 = 0). На кривой охлаждения горизонтальный участок. Нонвариантное равновесие имеет место также при кристаллизации чистого компонента и при кристаллизации химического соединения постоянного состава. Поскольку в данной системе из расплавов можно выделить два вида кристаллов (А и В), то и кривых ликвидуса тоже две. Аналогичным образом будет проходить кристаллизация расплавов по другую сторону от точки эвтектики.
|
|
|
Каждая система имеет строго определенный состав фаз при данной температуре. В двухфазных областях II и III, называемых областями кристаллизации, состав твердой фазы однозначен, а состав жидкой фазы может быть определен пересечением соответствующей изотермы с линией ликвидуса и отнесением на ось состава. Например, для системы Р (рис. 6.9б) состав жидкой фазы отмечен точкой PL и составляет 30% вещества А и 70% вещества В, твердая фаза – 100% В.
Отрезки канноды LS, проведенной через фигуративную точку Р, отображают относительные массовые количества жидкой и твердой фаз:
| LP: PS = m ж: m тв |
по так называемому правилу рычага.
Так, из 100 г смеси для точки Р масса твердой фазы – около 33 г, а в жидкой – около 67 г.
Двухкомпонентная система, состоящая из воды и растворяющейся в ней соли, характеризуется диаграммой состояния эвтектического типа. Выделяющуюся в точке Е эвтектическую водно-солевую смесь называют криогидратом. Затвердевшие криогидраты состоят из мелкодисперсной смеси кристаллов льда и соли.
Криогидратные температуры некоторых солей:
|
|
|
| ||||||||||||||||||||
| Таблица 6.4. |
Такие составы широко используются в практике для получения низкотемпературных смесей.
Диаграмма плавкости веществ с неограниченной растворимостью в жидком и твердом состоянии.
Весьма часто твердая фаза, выделяющаяся при охлаждении расплавов, состоит из кристаллов, образуемых обоими компонентами. Такая однородная система имеет переменный состав и называется твердым раствором. Твердые растворы – системы однофазные, подобно обычным жидким растворам, но в отличие от последних имеют кристаллическую структуру.
Неограниченной взаимной растворимостью в твердом состоянии обладают вещества, имеющие близкие значения атомных или ионных радиусов, энергии химической связи, сходное строение электронных оболочек и одинаковый тип кристаллической решетки (изоморфные вещества). Примерами таких систем могут служить Au–Ag, Cu–Au, Se–Ge, NaCl–NaBr и другие.
|
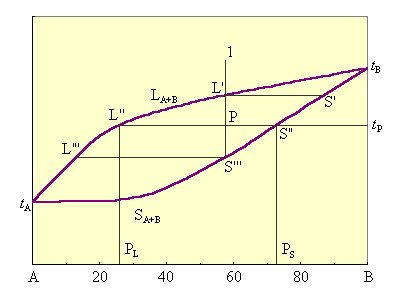
| Рисунок 6.12. Диаграмма плавкости для веществ, неограниченно растворимых в твердом и жидком состояниях. |
Представленная на рис. 6.12. диаграмма состоит из двух непрерывных сопряженных кривых: верхней t AL t B (кривой ликвидуса) и нижней t AS t B (кривой солидуса). Выше линии ликвидуса находится однофазная область – расплав компонентов A и B. В этой области при любых температурах и концентрациях система будет находиться в жидком состоянии (С = 2 + 1 – 1 = 2). Ниже кривой солидуса система существует только в виде одной твердой фазы, представляющей собой непрерывный ряд твердых растворов (С = 2 + 1 – 1 = 2).
Точки t A и t B – температуры плавления компонентов A и B. Между кривыми ликвидуса и солидуса находится двухфазная область, в которой сосуществуют жидкие и твердые растворы (С = 2 + 1 – 2 = 1). Кристаллизация всех промежуточных составов проходит в интервале температур. На кривых охлаждения отмечаются два излома, отвечающих началу и концу кристаллизации.
|
|
|
Рассмотрим особенности кристаллизации систем этого типа (рис. 6.12). Расплав состава, отвечающий фигуративной точке 1, охлаждаем до точки L'. Начинают выпадать кристаллы S'. При охлаждении до точки P выпадают кристаллы S'', состав расплава отвечает точке L''. По мере охлаждения состав кристаллов изменяется по кривой S' – S'' – S''', состав расплава – по кривой L' – L'' – L'''. Если отделить выкристаллизовавшиеся первые порции, обогащенные тугоплавким компонентом B, то неоднократным повторением процесса можно разделить A и B.
Составы жидкой и твердой фаз, сосуществующих при данной температуре, определяют точками пересечения изотермы соответственно с линиями ликвидуса и солидуса и отнесением их на ось составов. Так, для системы P (рис 6.12) при температуре t P состав жидкой фазы PL – 75% A и 25% B, твердой – PS – 28% A и 72% B. Количественные соотношения жидкой и твердой фаз в точке P определяют отношением отрезков PS'': PL'' = m ж: m тв.
Аналогичный вид имеет диаграмма состав–температура для двух жидкостей, неограниченно смешивающихся в жидком и парообразном состоянии.

Тема 6: Химические источники тока.
Цель:
1. Уметь записывать электрохимические уравнения реакций, происходящих на электродах гальванического элемента.
2. Научиться определять потенциал отдельного электрода.
3. Узнать какие типы электродов существуют.
4. Какие электроды сравнения существуют.
5. Понять на чем основан принцип работы концентрационных гальванических элементов.
6. Узнать принцип работы топливных элементов и в чем их преимущество перед другими типами гальванических элементов.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 594; Нарушение авторских прав?; Мы поможем в написании вашей работы!