
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Клітинні і неклітинні форми життя 2 страница
|
|
|
|
Клітинний центр (центросома) — органела, видима під оптичним мікроскопом у клітинах тварин, найпростіших та деяких рослин. Розміщена переважно біля ядра. Складається з 1—2, а іноді більше центріолей, оточених щільним шаром цитоплазми — центросферою. Центріоль має форму циліндра завдовжки 0,2—0,3 мкм і діаметром 0,1— 0,15 мкм. Стінка циліндра складається з 9 пар мікротрубочок, утворених фібрилами.
Центросома визначає орієнтацію веретена поділу клітини між центріолями, які розходяться до полюсів клітини, і бере участь у розходженні хромосом до полюсів. З нею пов'язана здатність деяких клітин до активного руху. Це підтверджується тим, що в основі джгутиків або війок рухливих клітин (найпростіші, сперматозоони) містяться
утвори такої самої структури, як і центросоми. У вищих рослин центросом немає. Веретено поділу формується з речовин ядра і цитоплазми клітини (див. "Мітоз").
Органели руху. Клітини можуть переміщуватися за допомогою спеціальних органел, до яких належать війки і джгутики. Війки клітин завжди численні (у найпростіших кількість їх досягає сотень і тисяч), а довжина становить 10—15 мкм. Джгутиків найчастіше буває 1—8, їх довжина становить 20— 50 мкм. Будова війок і джгутиків клітин як рослинних, так і тваринних організмів подібна. За допомогою електронного мікроскопа виявлено, що уздовж них проходять мікротрубоч-ки, дві з яких розміщені в центрі, а навколо них по периферії лежить ще 9 пар мікротрубочок. Уся ця структура вкрита цитоплазматичною мембраною, що є продовженням клітинної мембрани. Рух джгутиків і війок забезпечує не тільки пересування клітин у просторі, а й переміщення різних речовин по поверхні клітин та надходження харчових грудочок у клітину. Біля основи війок і джгутиків розміщені базальні тільця (гомолог центріолі), які також складаються з мікро – трубочок. Вважають, що базальні тільця є центром формування мікро – трубочок джгутиків І війок. Базальні тільця, в свою чергу, нерідко беруть початок від клітинного центру.
|
|
|
Велика кількість одноклітинних організмів і деякі клітини багатоклітинних не мають спеціалізованих органел руху і переміщуються за допомогою псевдоніжок (псевдоподій). Переміщення за допомогою псевдоніжок дістало назву амебоїдного руху. В його основі лежить рух молекул скоротливих білків.
Включення найчастіше трапляються в рослинних клітинах і від органел відрізняються тим, що вони тимчасові — то з'являються, то зникають у процесі життєдіяльності клітини і зазвичай не оточені мембраною. Кількість їх залежить від інтенсивності обміну речовин і стану організму. Під оптичним мікроскопом вони мають форму зерен або крапель різних величини і форми. За хімічним складом розрізняють: вуглеводні, білкові (зерна) та жирові (краплі) включення. У рослинних клітинах вуглеводи найчастіше відкладаються у вигляді зерен крохмалю, а в тваринних — глікогену. Білкові зерна у великій кількості містяться в цитоплазмі яйцеклітин тварин у вигляді жовтка. Багато їх у насінні рослин. Жирові краплі є в клітинах сполучної тканини тварин і в насінні рослин. У рослинних клітинах трапляються кристалічні включення (солі органічних кислот). За певних Умов усі види включень клітина в процесі життєдіяльності може використати, а потім нагромаджувати їх знову.
У цитоплазмі багатьох рослинних і деяких тваринних клітин є особливі органели — вакуолі. У клітинах безхребетних (кишковопорожнинні, війчасті черви, деякі молюски), в одноклітинних організмах та у фагоцитах вищих тварин утворюються травні вакуолі, що містять травні ферменти. У багатьох одноклітинних організмів є ще й пульсівні вакуолі, які, періодично скорочуючись, виводять із клітин продукти розпаду та регулюють осмотичний тиск (осморегуляція). У рослин вакуолі утворюються в процесі росту клітин, Дрібні й численні вакуолі, поступово збільшуючись, зливаються одна з одною й утворюють одну велику вакуолю, що займає майже всю клітину. Речовини клітинного соку (цукри, крохмаль, кислоти тощо), який заповнює вакуолю, сприяють живленню рослин і створюють пружний стан <тургор) у клітинах і тканинах. Особливо великі вакуолі утворюються в старих клітинах.
|
|
|
Ядро. Будова і функції в період інтерфази. Всі клітини тварин (за невеликим винятком — еритроцити) і рослин мають ядро. В більшості клітин є одне ядро, рідше трапляються дво- і багатоядерні клітини. Багатоядерними є клітини деяких видів найпростіших, а також клітини печінки, мозку і м'язів людини. Вони часто виникають внаслідок злиття кількох клітин в одну. Форма ядра здебільшого залежить від форми та розмірів клітини. Зазвичай у кулястих клітинах ядро має округлу форму, у видовжених м'язових клітинах ядро також видовжене. У деяких клітинах ядра можуть мати неправильну форму, наприклад, у лейкоцитів підковоподібні або лапчасті ядра. Форма ядра може змінюатися з віком клітини й залежить від її функціонального стану. Розміри ядра найчастіше коливаються від 2 до 20 мкм. Для кожного типу клітин існує певне ядерно-плазматичне співвідношення, порушення якого призводить до поділу клітини або її загибелі.
Ядро інтерфазної клітини вкрите двома цитоплазматичними мембранами, які відсутні лише в період мітотичного поділу. Зовнішня мембрана ядра часто переходить у мембрани ендоплазматичної сітки і простір між двома ядерними мембранами сполучається з її каналом.
В ядерних мембранах є пори діаметром 80—100 нм. Крізь них відбувається обмін між ядром і цитоплазмою.
Вміст ядра називають ядерним соком (каріоплазмою). У ньому міститься 1—2 ядерця й особлива речовина — хроматин (гр. спгогла — колір, забарвлення). Ця речовина добре фарбується ядерними барвниками. У прокаріотів хроматин складається лише з молекул ДНК, а в еукаріотів — із ДНК,
|
|
|
основних низькомолекулярних білків (гістонів), невеликої кількості кислих білків та іРНК. В інтерфазному ядрі, тобто в період між поділами клітин, хроматин (інтерфазна хромосома) перебуває у вигляді дрібної дифузної зернистості {еухроматин) або тонких ниток і щільних зерен різного розміру (гетерохроматин). Співвідношення еухроматину та гетеро-хроматину залежить від активності процесів у клітині. Чим інтенсивніше відбуваються різноманітні процеси синтезу в клітині, тим більше в них еухроматину, і навпаки. У процесі мітозу в результаті конденсації і скорочення тонких ниток та злиття окремих грудочок хроматину формуються паличкоподібні хромосоми. В період інтерфази в ядрі клітини відбуваються складні процеси біосинтезу ДНК, яка входить до складу хроматину, а також синтезi iРНК (транскрипція — зчитування інформації про структуру білка; див. "Біосинтез білка").
Ядерця мають розміри 0,5—1,0 мкм, містять велику кількість РНК і білка. Вони є місцем синтезу рибосомальної і транспортної РНК, ядерних білків та рибосом. Під час мітозу ядерця зникають, а потім формуються знову в телофазі. Утворення їх пов'язане з функціонуванням певних ділянок хромосом (ядерцевих організаторів), специфічних для кожного виду.
Ядро — це не просто важлива частина клітини, а центр керування її життєвими процесами — обміном речовин, рухом, розмноженням. В ядрі зосереджена основна маса ДНК, яка є носієм спадкової (генетичної) інформації, тобто ядро виконує функцію зберігання інформації про всі ознаки організму, а під час поділу клітини передає її дочірнім клітинам. Позбавлені ядра клітини (наприклад, еритроцити людини) мають порівняно коротку тривалість життя і не здатні до подальшого поділу і відновлення своєї цілісності в разі пошкодження (мал. 7,).
Мал. 7. Одноклітинна зелена водорість ацетабулярія (ілюстрація ролі ядра в регенерації):
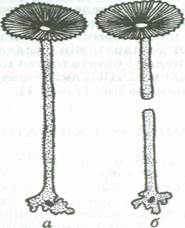
a — цілісний організм; 6 — перерізана особина ацетабуля-ріі; в — нижня частина відновлює "шапку" (верхня частина, яка позбавлена ядра, гине).
|
|
|
Таблиця 1. Характерні ознаки клітин прокаріотів та еукаріотів
| Показник | Прокаріоти | Еукаріоти |
| Зовнішня клітинна | ||
| мембрана | Є | Є |
| Ядро, вкрите | ||
| ядерною мембран - | ||
| ною | Немає | Є |
| Генетичний апарат | Одна нитка ДНК, | Парні хромосоми, |
| зазвичай замкнена в | які складаються з | |
| кільце | комплексу ДНК і | |
| білка | ||
| Ендоплазматична | ||
| сітка | Немає | Є |
| Рибосоми | Є (дрібніші) | Є |
| Клітинний центр | Немає | Є у більшості тва- |
| рин і деяких рослин | ||
| Мітоховдрії | Немає | Є |
| Комплекс Гольджі | Немає | Є |
| Лізосоми | Немає | Є |
| Джгутики | Є у деяких видів | Є у деяких видів, |
| складної будови | ||
| Поділ | Простий, якому пере- | Мітоз (непрямий) |
| дує реплікація ДНК |
Прокаріоти та еукаріоти. Будова органел і інтерфазно-го ядра, що описана вище, характерна для клітин усіх тварин і більшості видів рослин та грибів. Ці організми дістали назву ядерних, або еукаріотів. Інша група організмів, менша за чисельністю і, мабуть, давніша за походженням, дістала назву прокаріотів (доядерних). До них належать бактерії та синьо-зелені водорості (їх відносять до царства Дроб'янки), в яких немає справжнього ядра та багатьох органел цитоплазми. Замість ядра у них є нуклеоїд (утвір, подібний до ядра). Він складається із сукупності нуклеїнових кислот і білків (серед них 90 % ДНК і 10 % припадає на білки і РНК), які лежать у цитоплазмі і не відділені від неї мембраною (табл. 1).
ХІМІЧНА ОРГАНІЗАЦІЯ КЛІТИНИ
Вміст хімічних елементів у клітині. Подібність елементарного хімічного складу клітин усіх організмів свідчить про єдність живої природи. Водночас у живих організмах не виявлено жодного хімічного елемента, який би траплявся в тілах неживої природи. Цим підтверджується спільність живої і неживої природи.
Найбільший вміст у клітині чотирьох елементів: кислоти (65—70 %), вуглецю (15—18 %), водню (8—10 %), азоту
(2--3 %).Це органогенні елементи. Разом їх вміст стануть 95—98 % загальної маси живого організму. Вміст у живому організмі таких елементів, як кальцій, калій, фос-фор, сірка, силіцій, натрій, хлор, магній, залізо, становить десяті частки відсотка. Перелічені хімічні елементи належать до макроелементів. Кобальт, цинк, мідь, манган, хром, бром, бор, йод, літій, радій містяться у дуже малих кількостях (менше 0,01 %). їх називають мікроелементами. Важливість того чи іншого хімічного елемента для живих істот визначається не його кількістю. Багато мікроелементів входить до складу ферментів, гормонів та інших життєво важливих сполук, які впливають на процеси розмноження, кровотворення та ін. Наприклад, цинк входить до складу молекули інсуліну; кобальт — до складу ціанкобаламіну (вітаміну В12) тощо.
Усі живі організми значно відрізняються від навколишньої неорганічної природи за кількісним хімічним складом. Наприклад, вуглецю у рослинах міститься близько 18 %, у грунті — менше 1 %, а силіцію, навпаки, у рослинах — 0,15 %, а у грунті — 33 %. Великий вміст вуглецю в складі живих організмів пов'язаний з наявністю в них вуглецевмісних сполук, які називають органічними.
У деяких живих організмах нагромаджуються певні хімічні елементи. Так, у водоростях нагромаджується йод, у жовтці — літій, у болотній рясці — радій тощо.
Вода та інші неорганічні речовини, їхня роль у життєдіяльності клітини. Із неорганічних сполук у клітині найбільше води. Чим вища інтенсивність обміну речовин у тій чи іншій тканині, тим більше вона містить води. В ембріона людини у віці 1,5 місяця вода становить 97,5 %, у вось-мимісячного — 83, у немовляти — 74, у дорослої людини в середньому 66 %. Вміст води в різних органах і тканинах людського організму також різний. Так, мозок дорослої людини містить 86 %, печінка — 70, кістки — 20 % води. З віком вміст води у тканинах зменшується. Вода виконує в клітинах багато функцій: збереження об'єму, забезпечення пружності клітин, розчинення різних хімічних речовин. Крім того, вода — це середовище, в якому відбуваються всі хімічні процеси. Вона безпосередньо бере участь в усіх хімічних реакціях. Так, розщеплення жирів, вуглеводів та інших органічних сполук відбувається в результаті хімічної взаємодії їх з водою. Завдяки високій теплоємності вода захищає цитоплазму від різких коливань температури, сприяє терморегуляції клітин і організму. Частина молекул води (—15 %) у клітинах перебуває у зв'язаному з білковими молекулами стані. Вони ізолюють білкові молекули одну від одної в колоїдних розчинах.
Багато органічних речовин клітини (ліпіди) мають низьку розчинність у воді. Молекули води слабко притягуються до цих речовин, тому вони, становлячи основу клітинної мембрани, обмежують проникнення води з клітини у внутрішнє середовище і навпаки.
Мінеральні солі у великій кількості містяться у клітинах опорних органів — черепашок, хітинових панцирів, кісток. У цитоплазмі інших клітин багато солей перебуває в дисоційованому стані у вигляді катіонів і аніонів — К+, Nа+, Са2+, СI', НСОз, Н?РО4 та ін.
Вміст у клітині катіонів має велике значення для її функціонування. Від концентрації солей залежить надходження води у клітину, бо клітинна мембрана проникна для молекул води і непроникна для багатьох великих молекул та іонів. Якщо в навколишньому середовищі міститься менше іонів, ніж у цитоплазмі клітини, то відбувається надходження води в клітину до вирівнювання концентрації солей (осмос).
Наявність солей у цитоплазмі визначає її буферні властивості — здатність підтримувати стале значення рН (близьке до нейтральної реакції), хоча в процесі обміну речовин безперервно утворюються кислотні й основні продукти.
Будова і біологічні функції органічних речовин, які входять до складу клітини. Різні клітини можуть дуже різнитися за вмістом органічних речовин. У перерахунку на суху масу в клітинах міститься ліпідів — 5—15 %, білків — близько 10—12, вуглеводів — 0,2—2,0, нуклеїнових кислот — 1—2 % маси клітини. Більшість органічних сполук має довгі молекули (полімери), складені з ланцюгів простіших молекул (однорідних або різнорідних мономерів).
Вуглеводи у великій кількості містяться в рослинних клітинах. У деяких плодах, насінні, бульбах вміст їх іноді досягає 90 %. У тваринних клітинах вуглеводів значно менше — до 5 %. Прості вуглеводи називають моносахаридами, складні — полісахаридами. З моносахаридів у організмах трапляються пентози (цикли з 5 атомів вуглецю) і гексози (цикли з 6 атомів вуглецю). Серед пентоз найважливішими є рибоза (складова частина РНК) і дезоксирибоза (складова частина ДНК). Серед гексоз — глюкоза і фруктоза. Вони містяться в багатьох плодах і в
мелУ і зумовлюють солодкий смак їх. Глюкоза є і в крові людини (близько 0,12 %). Цей вуглевод - основний енергетичний матеріал для всіх клітин.
Полісахариди утворюються в процесі полімеризації двох або кількох моносахаридів. Серед дисахаридів найпоширеніші сахароза (складається з молекул глюкози і фруктози) і лактоза, або молочний цукор (складається з молекул глюкози і галактози). З полімерів у природі найчастіше трапляються крохмаль, целюлоза, або клітковина (у рослин), і глікоген (у тварин). Загальна формула їх — (C6H10O5)n, a мономером цих полісахаридів с глюкоза. Наприклад, кожна молекула клітковини утворена ланцюгом із 150—200 молекул глюкози.
Вуглеводи — своєрідне "паливо" для живої клітини: окиснюючись, вони вивільняють хімічну енергію (1г — 17,6 кДж), яка витрачається клітиною на всі процеси життєдіяльності. У рослин вуглеводи виконують і будівельні функції: з них утворюються оболонки клітин. У тварин і грибів у будові клітин бере участь азотовмісний полісахарид — хітин.
Ліпіди — це низькомолекулярні речовини з гідрофобними властивостями. Разом з білками і вуглеводами це основні компоненти всіх видів клітин. У різних органах і тканинах вміст ліпідів неоднаковий. Особливо багато їх у нервовій тканині, серці, печінці, нирках, крові, насінні і плодах деяких рослин.
За хімічною будовою ліпіди досить різноманітні. До складу їхніх молекул входять вищі жирні кислоти, спирти, альдегіди, азотисті основи, амінокислоти, аміноспирти, вуглеводи, фосфорна кислота та ін. Між цими сполуками можуть утворюватися зв'язки: ефірні, складно ефірні, глікозидні, а мідні, фосфоефірні тощо. Класифікація ліпідів дуже складна у зв'язку зі складністю будови молекул цих речовин та їх різноманітністю. Нині всі ліпіди прийнято поділяти на нейтральні (жири) і фосфоліпіди.
Нейтральні ліпіди — це похідні вищих жирних кислот і трьохатомного спирту гліцерину. Як і вуглеводи, жири використовуються як джерело енергії: під час розщеплення одного грама жиру виділяється 38,9 кДж енергії. Підшкірний жир виконує важливу теплоізоляційну функцію, а також сприяє зменшенню впливу ударів та поштовхів. Для тварин, які впадають у сплячку, жири забезпечують організм необхідною енергією, оскільки поживні речовини ззовні в цей час не надходять. Жири становлять запас поживних речовин І в насінні багатьох рослин.
Фосфоліпіди — найбільша частина ліпідів, які входять до складу клітинних мембран. Якщо в середньому на ліпіди припадає 40 % сухої маси мембран, то 80 % з них — на фосфоліпіди. Отже, основні функції мембран (регулювання проникності різних речовин і клітинного вмісту, функціонування іонних насосів, сприйняття, оброблення і передавання всередину клітини інформації з ЇЇ поверхні, імунна відповідь, синтез білків і багато іншого) здійснюються за участю фосфоліпідів (див. мал. 3).
Ліпіди не розчинні у воді і добре розчинні в органічних розчинниках (бензині, ефірі тощо). Самі ліпіди є розчинниками для деяких вітамінів.
Білки, або протеїни, становлять 50—80 % усіх органічних речовин клітини, вони входять до складу міжклітинної рідини, лімфи» плазми крові. Всі види білків мають високу молекулярну масу, яка в окремих випадках досягає 1,5 млн у. о. (умовних одиниць). Всі білки — полімери, мономерами яких є амінокислоти. До складу білків входить близько 20 різних амінокислот. Загальна форму-
™ р — падикал. який може
ла амінокислот 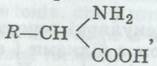 , де R — радикал, який може
, де R — радикал, який може
СООН
бути циклічною або ланцюговою сполукою. Амінна — МН2 (основна) і карбоксильна — СООН (кислотна) групи визначають амфотерність амінокислот, забезпечують буферність їх розчинів і можливість сполучення їх у довгі ланцюги. Зв'язок між аміногрупою однієї молекули кислоти і карбоксильною групою іншої (виникає в разі відщеплення води) називають пептидним (позначено стрілкою):
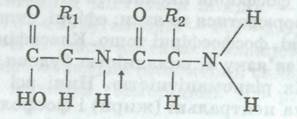 Довгий ланцюг з амінокислотних залишків, сполучених пептидними зв'язками (полі пептид), є первинною струк* турою білка. У цьому ланцюзі різні амінокислоти можуть комбінуватися по-різному. Послідовність розміщення окремих амінокислот (первинна структура білка) визначає специфічність білків. Заміна, відсутність або просто перестановка хоча б одного амінокислотного залишку у поліпептидному ланцюзі спричинює появу нових білків. ХІ°' лі пептидний ланцюг, утворений кількома сотнями амінокислотних залишків, скручується у спіраль, між окремими витками якої утворюються численні, але сланкі водневі зв'язки. Така молекула утворює вторинну структуру білка. Далі ця спіраль може скручуватися ще більше і складатися у клубок, або глобулу (лат. globus — куля). У глобулах залишки амінокислот сполучені слабкими ковалентними зв'язками. Наприклад, зв'язок S—S між радикалами двох молекул цистеїну, які розміщені на великій відстані одна від одної в поліпептидному ланцюзі. На цій стадії білок виконує притаманні йому функції, тобто стає активним.
Довгий ланцюг з амінокислотних залишків, сполучених пептидними зв'язками (полі пептид), є первинною струк* турою білка. У цьому ланцюзі різні амінокислоти можуть комбінуватися по-різному. Послідовність розміщення окремих амінокислот (первинна структура білка) визначає специфічність білків. Заміна, відсутність або просто перестановка хоча б одного амінокислотного залишку у поліпептидному ланцюзі спричинює появу нових білків. ХІ°' лі пептидний ланцюг, утворений кількома сотнями амінокислотних залишків, скручується у спіраль, між окремими витками якої утворюються численні, але сланкі водневі зв'язки. Така молекула утворює вторинну структуру білка. Далі ця спіраль може скручуватися ще більше і складатися у клубок, або глобулу (лат. globus — куля). У глобулах залишки амінокислот сполучені слабкими ковалентними зв'язками. Наприклад, зв'язок S—S між радикалами двох молекул цистеїну, які розміщені на великій відстані одна від одної в поліпептидному ланцюзі. На цій стадії білок виконує притаманні йому функції, тобто стає активним.
Деякі білки утворюють надмолекулярні комплекси, до складу яких входить кілька глобул — це четвертинна структура білка. Наприклад, молекула гемоглобіну складається з чотирьох великих глобул, сполучених між собою також порівняно слабкими зв'язками. Молекули таких білків мають величезну молекулярну масу (кілька мільйонів умовних одиниць).
Під впливом різних фізичних і хімічних факторів можуть відбуватися розкручування білкової молекули і втрата вторинної, третинної та четвертинної структур білка, що призводить до втрати або зміни його властивостей. Порушення специфічної просторової конфігурації білкової молекули має назву денатурації, яка може бути зворотною (у разі збереження первинної структури білка) і незворотною (у разі руйнування первинної структури білка) після припинення дії, яка спричинила зміну його структури.
Значна кількість білків у клітині перебуває у зв'язаному стані з іншими хімічними сполуками. Складові частини таких сполук, як правило, відбиті у їхніх назвах: нуклеопротеїди (нуклеїнова кислота + білок), глюкопротеїд (вуглевод + білок), хромопротеїд (пігмент + білок).
Значення білків дуже велике, бо життя завжди пов'язане з білками. Білки входять до складу всіх органел і мембран клітини, є головним структурним матеріалом.
Дуже важлива рухова функція білків. Комплекси з молекул деяких білків (наприклад, міозину й актину) здатні до скорочення. Завдяки цій властивості білків скорочуються м'язи, рухаються війки і джгутики, переміщуються хромосоми у клітині тощо. Деякі білки виконують в організмі сигнальні функції. З ними пов'язана подразливість клітин і організмів. Ще одна функція білків — захисна, яка забезпечується особливими білками (антитілами), які знешкоджують, нейтралізують побічні (чужорідні) для організму речовини. Нарешті, білки є джерелом енергії. В процесі розщеплення білкової молекули на окремі амінокислоти частина їх може використовуватися для біосинтезу нових молекул білка, а частина розщеплюється повністю, вивільняючи енергію. Внаслідок повного розщеплення 1 г білка вивільняється 17,6 кДж енергії.
Величезне значення мають білки як біокаталізатори, або ферменти.
Ферменти, Молекули простих ферментів складаються лише з амінокислот, а молекули складних можуть функціонувати тільки за наявності в молекулі двох компонентів — білкового (апоферменту) і небілкового (коферменту). Коферментами можуть бути різні органічні речовини, в тому числі і вітаміни, а також метали.
Жодна реакція в клітині не може відбуватися з нормальною швидкістю без участі ферментів як біологічних каталізаторів.
У класифікації ферментів враховують як специфічність їхньої дії на субстрат, так і хімічні реакції, які вони каталізують. Розрізняють ферменти — ліпази (розщеплюють ліпіди), амілази (розщеплюють вуглеводи), пептидази (розщеплюють білки), а також ферменти окисно-відновних реакцій, реакцій гідролізу і синтезу, реакцій перенесення, приєднання або відщеплення певних органічних залишків або груп. Нині складено каталог ферментів, в якому кожному з них присвоєно власний номер і систематичну назву. Наприклад, пепсин за номенклатурою ферментів позначається 3.4.4.1 (пептид пептид о гідролаза), а ліпаза — 3.1.1.3 (гідролаза ефірів гліцерину).
Вибірковість дії ферментів на різні хімічні речовини пов'язана з їхньою будовою. Молекули всіх ферментів мають один або кілька активних центрів, якими вони прикріплюються до тих речовин, на які можуть діяти. Тому дія ферментів завжди специфічна. Наприклад, два травних ферменти — пепсин і трипсин — беруть участь у розщепленні молекул білків до невеликих фрагментів, але кожний з них діє по-різному. Пепсин руйнує зв'язки амінокислоти тирозину, а трипсин — амінокислот аргініну і лізину, причому перший діє на аміногрупи, а другий — на карбоксильні групи амінокислот. Зазвичай ферменти каталізують багато послідовних реакцій, причому речовини, які утворилися за участю першого ферменту, є субстратом для другого тощо. Дія ферментів у клітині завжди узгоджена і відбувається у певній послідовності. Це досягається завдяки тому, що ферменти локалізовані в різних ділянках клітинної мембрани. В органелах клітини ферменти також розміщені послідовно й утворюють упорядковані системи.
Залежно від наявного комплексу ферментів у різних видів організмів і в різних органах обмін речовин відбувається по-різному. Для функціонування кожного ферменту потрібні оптимальні температура і реакція середовища, оскільки одні з них активні в нейтральному середовищі (наприклад, ферменти слини), інші — в кислому (ферменти шлункового соку) або лужному (ферменти підшлункової залози). У разі нагрівання до температури понад 60 °С багато ферментів інактивується (відбувається денатурація білків).
Нуклеїнові кислоти (лат. nucleus — ядро). Ці речовини вперше було виявлено і виділено з ядер клітин. € два види нуклеїнових кислот: дезоксирибонуклеїнова (ДНК) і рибонуклеїнова (РНК). Основна кількість ДНК зосереджена в хромосомах клітини і лише невелика її кількість міститься в мітохондріях і пластидах. РНК міститься в ядерцях, а також у цитоплазмі.
Молекула ДНК — це дуже довгий полінуклеотидний ланцюг, довжина його може досягати десяти міліметрів. Так, вважають, що сумарна довжина молекул ДНК 46 хромосом однієї клітини людини становить 170—180 см. Відповідно дуже велика і молекулярна маса ДНК (сотні мільйонів умовних одиниць).
Кожна молекула ДНК складається з двох сполучених між собою ланцюгів нуклеотидів. До складу кожного нук-леотиду входять азотиста основа, дезоксирибоза і фосфорна кислота. Всього в ДНК є чотири види азотистих основ: аденін (А), гуанін (Г), тимін (Т) і цитозин (Ц) (мал. 8).
Нуклеотиди різняться лише азотистими основами. Назва нуклеотидів також пов'язана з назвою нуклеозидів (сполук азотистих основ з пентозою) цих основ. Наприклад, нуклеотид, який містить аденін, утворюється приєднанням залишку фосфорної кислоти до аденозинового нуклеозиду (аденін + рибоза або дезоксирибоза), називається аденіловим. Відповідно утворюються нуклеотиди гуанозинового, Уридинового, цитидинового і тимідинового нуклеозидів.
Два ланцюги, які складаються з десятків і сотень нуклеотидів, скручуються між собою й утворюють подвійну спіраль. Діаметр цієї спіралі становить 2 * 10-9 м (2 нм), а відстань між сусідніми нуклеотидами — 3,4 • 10-10 м (034 нм; 1 нм = 10-9 м). Розмір витка спіралі (крок спіралі) становить 3,4 • 10-9 м (3,4 нм), у ньому розміщується 10 пар нуклеотидів.
Азотисті основи одного ланцюга сполучені з основами другого ланцюга за допомогою водневих зв'язків у такому порядку: аденін одного ланцюга сполучений з тимі-ном другого ланцюга; гуанін сполучений так само з цитозином
Сполучення інших типів у нормі ніколи не виникають. Це пояснюється тим, що між такими парами нуклеотидів, як аденін" — тимін і гуанін — цитозин, існує особливий тип зв'язку, який дістав назву комплементарного {принцип комплементарності; лат. сотріетепіиш — доповнення).
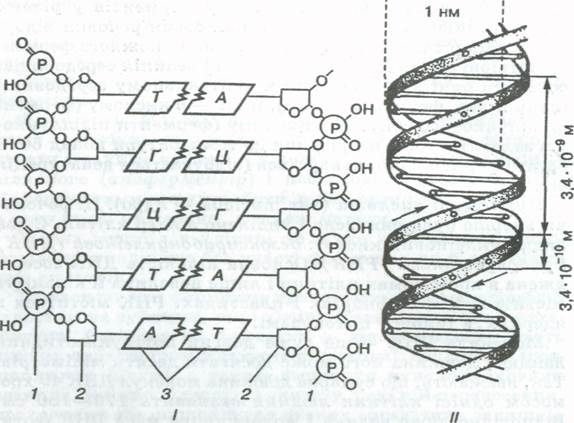
Мал. 8. Схема будови молекули ДНК (/) та її спіральної структури (// ):
1— залишок фосфорної кислоти; 2 — дезоксирибоза, 3 — азотисті
. Сполучення інших типів у нормі ніколи не виникають. Це пояснюється тим, що між такими парами нуклео-тидів, як аденін" — тимін і гуанін — цитозин, існує особливий тип зв'язку, який дістав назву комплементарного {принцип комплементарності; лат. сотріетепіиш — доповнення). При цьому між А і Т утворюється два водневих зв'язки, а між Г і Ц — три. Знаючи послідовність сполучення нуклеотидів одного ланцюга молекули ДНК, можна встановити порядок розміщення нуклеотидів другого. Наприклад, якщо в одному ланцюзі послідовність нуклеотидів буде А—А—А—Ц—Т—Т—Г—Г—Г, то на відповідній ділянці другого ланцюга послідовність обов'язково буде Т—Т—Т^-Г—А—А—Ц—Ц—Ц. Приклад розв'язування задач до цього розділу див. у додатку — задача 2.
Подвійна спіраль молекули ДНК здатна розкручуватися, при цьому водневі зв'язки розриваються й окремі ланцюги ДНК відходять один від одного. Іноді таке роз'єднання ланцюгів відбувається не по всій довжині молекули, а лише на певній ділянці. Ланцюги ДНК можуть знову спаралізуватися, відновлюючи свою попередню структуру.
Редуплікація (лат. duplicatio — подвоєння), реплікація (англ. replica — відбиток) ДНК — процес самовідтворення макромолекул нуклеїнових кислот, який забезпечує точне копіювання генетичної інформації і передавання її з покоління в покоління. Самоподвоєння молекули ДНК відбувається в період інтерфази перед поділом клітин. При цьому молекула ДНК розкручується і з одного кінця спіраль розділяється на окремі ланцюги. Біля кожного з них із вільних нуклеотидів, які є в ядрі клітини, розпочинається синтез другого ланцюга ДНК. Цей синтез відбувається за принципом комплементарності. В результаті замість однієї молекули ДНК утворюються дві молекули такого самого нуклеотидного складу, як і початкова. Один ланцюг у кожній новоутвореній молекулі ДНК походить від початкової молекули (материнський ланцюг), а другий синтезується заново (дочірній). Як процес розділення молекули ДНК на два ланцюги, так і процес синтезу нових ланцюгів здійснюється за рахунок дії низки ферментів (ДНК-полімерази, ДНК-лІгази).
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 865; Нарушение авторских прав?; Мы поможем в написании вашей работы!