
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Обробка результатів
|
|
|
|
Порядок виконання роботи
Теплові ефекти процесів
Лабораторна робота №2
Ознакою перебігу хімічної реакції є утворення або розчинення осаду.
Класи неорганічних сполук
Лабораторна робота №1
Мета роботи – ознайомитися зі способом добування та властивостями поганорозчинних гідроксидів металів.
| Номер завдання | Вихідні речовини | Номер завдання | Вихідні речовини |
| а) сульфат магнію | а) сульфат нікелю | ||
| б) нітрат плюмбуму (ІІ) | б) сульфат цинку | ||
| а) сульфат цинку | а) хлорид феруму (ІІІ) | ||
| б) нітрат кадмію | б) нітрат плюмбуму (ІІ) | ||
| а) сульфат алюмінію | а) сульфат купруму (ІІ) | ||
| б) сульфат магнію | б) сульфат алюмінію | ||
| а) сульфат цинку | а) сульфат цинку | ||
| б) сульфат магнію | б) хлорид феруму (ІІІ) | ||
| а) нітрат кадмію | а) нітрат плюмбуму (ІІ) | ||
| б) сульфат алюмінію | б) сульфат купруму (ІІ) | ||
| а) нітрат плюмбуму (ІІ) | а) сульфат алюмінію | ||
| б) нітрат кадмію | б) сульфат мангану (ІІ) |
Використовуючи набуті знання про властивості сполук, запропонуйте план виконання контрольного завдання.
Дослід 1. Добування та властивості гідроксидів металів:
1. У дві пробірки внесіть 1-2 мл солі “а” та додайте у кожну з них декілька крапель розчину гідроксиду натрію (NaOH) до утворення осаду гідроксиду відповідного металу.
Для визначення хімічного характеру гідроксиду металу до вмісту першої пробірки додайте розчин нітратної кислоти (HNO3), до вмісту другої – надлишок розчину NaOH. В якому випадку осад розчиняється? Зробіть висновок про хімічних характер гідроксиду металу (основний чи амфотерний) та складіть рівняння відповідних реакцій.
2. Повторіть дослід у тому ж порядку з розчином солі “б”.
|
|
|
Дослід 2. Контрольний дослід
Визначте, у якій зі склянок з номерами, що надає викладач, знаходяться розчини солей “а” і “б”, використовуючи тільки розчин лугу.
Мета роботи – визначити масу розчиненої сполуки за кількістю теплоти, що виділяється або поглинається при її розчиненні.
1. Отримайте у викладача завдання: назву (формулу) сполуки, яку слід розчинити у певному об’ємі води V (Н2О), мл.
2. У внутрішню склянку спрощеного калориметра налийте зазначений об’єм води та заміряйте її температуру t 1, °С.
3. Не виймаючи термометра, всипте у воду кристали сполуки. Обережно розмішуючи суміш термометром, досягніть максимального розчинення сполуки та визначте найвищу (або найнижчу) температуру t 2, °С.
1. Обчисліть кількість теплоти q, що виділяється або поглинається при розчиненні виданої кількості сполуки, вважаючи, що густина розчину дорівнює 1 г /мл, об’єм розчину – об’єму води, а теплоємність розчину – теплоємності води с = 4,18 Дж/(г × К):
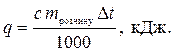
2. Розрахуйте масу розчиненої сполуки m, використовуючи табличне значення стандартної молярної ентальпії розчинення D Н 0розч. і молярну масу сполуки М. Вихідні дані та результати досліду занесіть у таблицю.
| № зав- дання | Формула сполуки | М, г /моль | V (Н2О), мл | D Н 0розч., кДж/моль | t 1, °С | t 2, °С | q, кДж | m, г |
| Н2С2О4 | ||||||||
| K2Cr2O7 | ||||||||
| Na2B4O7×10H2O | ||||||||
| Na3PO4×12H2O | ||||||||
| Na2CO3 | -24 | |||||||
| NaOH | -42 | |||||||
| NH4Cl |
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 352; Нарушение авторских прав?; Мы поможем в написании вашей работы!