
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Объемные доли газовой смеси
|
|
|
|
Задачи
Газовые смеси. Закон Дальтона
Пример 8. Сухие продукты сгорания нефти массой 1 кг имеют следующий состав: mCO2 = 3,20 кг; mCO = 1,01 кг; mO2 = 1,33 кг; mN2 = 17,40 кг. Найти массовые компоненты газов, составляющих эту смесь, молярную массу и удельную газовую постоянную смеси.
Решение. Предварительно найдем массу смеси по уравнению
m = mCO2 +mCO +mO2 +mN2 = 3,20+1,01+1,33+17,40= 22,94 кг.
Вычислим массовые доли компонентов:
wCO2 = mCO2 / m = 3,20/22,94 = 0,394;
wCO = mCO/ m = 1,01/22,94 = 0,44;
wO2 = mO2/ m = 1,33/22,94 = 0,058;
wN2 = mN2/ m = 17,40/22,94 = 0,759.
Проверим произведенные вычисления по контрольному уравнению:
wCO2 +wCO +wO2 +wN2= 0,139+ 0,44+0,058+0,759=1,00.
Сумма массовых долей равна 1, значит, вычисления произведены правильно.
Пользуясь уравнением, определим молярную массу смеси (молярные массы компонентов находим по табл. 1 прил.

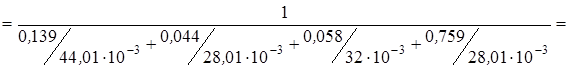
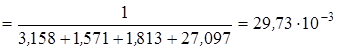 кг/моль.
кг/моль.
Определим удельную газовую постоянную смеси
R0 =R/Mсм = 8,31/(29,73×10-3)= 279,5 Дж/(кг К).
18. Найти относительную молекулярную массу смеси, состоящей из 5 кг CO2 и 3 кг O2 . Ответ: 38,58.
19. Имеется смесь, состоящая из углекислого газа массой 6 кг и азота массой 2 кг. Найти массовые доли компонентов смеси. Ответ: wCO2 = 75%; wN2= 25%.
20. Газовая смесь состоит из углекислого газа, азота и кислорода, массы которых соответственно равны 2 кг, 1 кг и 0,5 кг. Найти плотность и объем смеси при температуре 27°С и давлении 147 кПа. Ответ: r = 2,133 кг/м3; V =1,641 м3.
21. Найти удельную газовую постоянную смеси газов, состоящей из 6,67% водорода и 93,33% угарного газа, а также удельный объем этой смеси при давлении 100 кПа и температуре 0°С. Ответ: 554,1 Дж/(кг К); v= 1,513 м3/кг.
22. До какого давления нужно сжать смесь массой 8 кг, состоящую из 18% углекислого газа, 12% кислорода и 70 % азота, чтобы при температуре 180°С она занимала объем 4 м3? Ответ: 247247 Па
|
|
|
Пример 9. Найти удельную газовую постоянную смеси, состоящей из азота с приведенным объемом 0,4 м3 и кислорода с приведенным объемом 0,2 м3.
Решение. Общий объем смеси
V = VN2 + VO2 = (0,4 +0,2) м3 = 0,6 м3.
Объемные доли компонентов:
хO2 = VO2/ V = 0,2/0,6 =0,333;
хN2 = VN2/ V = 0,4/0,6 =0,667.
Контрольное уравнение:
хO2 +хN2 = 0,333+0,667= 1,000.
Молярная масса смеси:
 0,333×32×10-3+0,667×28×10-3 =
0,333×32×10-3+0,667×28×10-3 =
29,332×10-3 кг/моль.
Удельная газовая постоянная смеси
R0 =R/Mсм = 8,31/29,332×10-3 = 283,3 Дж/(кг К).
Пример 10. Найти для условий предыдущего примера парциальные давления азота и кислорода газовой смеси. Давление смеси равно 0,1 МПа.
Решение. Парциальные давления компонентов:
рO2 = хO2×р = 0,333×0,1×106 =33333 Па;
рN2 = хN2×р = 0,667×0,1×106 =66667 Па.
Контрольное уравнение:
рO2 +рN2 = 33333+66667= 10000 Па = 0,1 МПа.
Пример 11. Продукты сгорания топлива массой 1 кг имеют следующий состав (в моль): nH2O (паров воды) = 60,3; nCO2 = 73,9; nO2 = 123,2; nN2 = 849,5. Найти молярную массу и массу смеси.
Решение. Количество вещества продуктов сгорания
nсм = nH2O +nCO2 +nO2 +nN2 = 60,3+ 73,9+ 123,2+ 849,5 = 1106,9 моль.
Молярные доли компонентов:
хH2O = nH2O/n = 60,3/1106,9=0,0544;
хCO2 = n CO2/ n = 73,9/1106,9 =0,0668;
хO2 = nO2/ n = 123,2/1106,9 =0,1113;
хN2 = nN2/ n = 849,5/1106,9 =0,7675.
Контрольное уравнение:
хH2O +хCO2 +хO2 +хN2 = 0,0544+0,0668+0,1113+0,7675= 1,000.
Молярная масса смеси
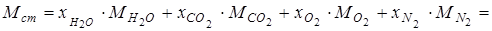
(0,0544×18+ 0,0668×44 +0,1113×32+0,7676×28)×10-3 = 29,332×10-3 кг/моль.
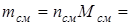 1106,9×29,332×10-3 = 32,47 кг.
1106,9×29,332×10-3 = 32,47 кг.
|
|
|
|
|
Дата добавления: 2015-05-08; Просмотров: 7368; Нарушение авторских прав?; Мы поможем в написании вашей работы!