
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Нарушения ритма 1 страница
|
|
|
|
Изменения ритма, т. е. неодинаковая продолжительность сердечных циклов, значительное учащение или урежение сердечных сокращений, принято называть аритмией независимо от причины (физиологической или патологической), вызвавшей их.
Причинами аритмии могут быть: I) нарушения образования импульсов; 2) нарушения проведения импульсов; 3) комбинированные нарушения образования и проведения импульсов.
Причинами нарушений ритма могут быть органические изменения в миокарде, синусовом узле или в проводящей системе сердца. Они могут быть вызваны многими органическими заболеваниями сердца, такими как кардиосклероз, дистрофия миокарда, поражения сердца при других заболеваниях внутренних органов (тиреотоксикоз, коллагенозы, легочное сердце и др.). Различают тахикардические формы аритмий (при частоте сердечных сокращений 100 и более в 1 мин) и брадикардические (при частоте сокращений менее 60 в 1 мин). Нарушение ритма сердечных сокращений отражается на величине минутного объема сердца, который зависит от ударного (систолического) объема сердца и частоты сокращений.
В норме минутный объем сердца составляет 5—8 л/мин. При умеренно выраженной брадикардии может сохраняться состояние компенсации за счет увеличения ударного (систолического) объема сердца. Однако при частоте сокращений 40 и менее в I мин возникают ишемия мозга, обморок, потеря сознания. При тахикардических формах нарушений ритма длительность диастолы становится короче, в связи с этим уменьшается наполнение кровью желудочков сердца. Это приводит к резкому уменьшению ударного и минутного объема сердца и таким же симптомам, как при брадикардии.
17.10.1. Брадикардия
|
|
|
Наиболее часто брадикардия возникает вследствие атриовентрикулярной блокады проведения импульсов и слабости синусового узла, причиной которых чаще всего являются дегенеративные изменения в специфических мышечных волокнах (проводящих путях), обеспечивающих возбуждение и проведение импульсов. Указанные изменения могут возникать при хронической ишемической болезни сердца, кардиомиопатии, ревматизме, миокардите и других заболеваниях миокарда.
У больных с такой патологией в анамнезе могут быть сведения о применении лекарственных средств, урежающих частоту сердечных сокращений; нарушения кровообращения мозга вследствие заболеваний сосудов. Для обследования применяют неинвазивные инструментальные методы (ЭКГ в покое, при нагрузке и суточная запись ЭКГ по Холтеру с последующей расшифровкой на специальном аппарате, эхокардиография).
Наибольшее значение среди нарушений проводимости имеет атриовентрикулярная блокада и блокада ножек пучка Гиса. Они характеризуются нарушением проведения возбуждения из предсердий в желудочки на разных уровнях. Нарушение проведения импульсов по ветвям пучка Гиса называют дистальной блокадой. Различают три степени этой блокады: [ степень обнаруживается только на ЭКГ, при II степени наблюдается выпадение отдельных желудочковых комплексов, что сопровождается ощущением перебоев ритма сердечных сокращений, выпадением отдельных комплексов ЭКГ. Ат-риовентрикулярная блокада III степени характеризуется полной блокадой проведения импульсов из предсердий в желудочки. Это так называемая полная поперечная блокада. В результате желудочки сокращаются в более медленном ритме (30—40 в 1 мин), чем предсердия, что приводит к уменьшению минутного объема сердца, ишемии мозга. У больных могут возникать обморок, кратковременная потеря сознания, цианоз, судороги. Это может быть связано также с временной асистолией и кратковременным прекращением кровоснабжения мозга (симптомокомплекс Адамса—Стокса— Морганьи).
|
|
|
В связи с нарушением ритма сокращений предсердий в них могут образоваться тромбы, которые служат причиной эмболии периферических артерий.
Лечение. Основным способом лечения брадикардических форм нарушений ритма является лекарственная терапия. При неэффективности лечения антиаритмическими препаратами показано хирургическое лечение — имплантация водителя ритма, т. е. электрокардиостимулятора. Показаниями к имплантации являются слабость синусно-предсердного узла (прекращение функции узла, атриовентрикулярная блокада, патологическая синусовая брадикардия), атриовентрикулярная блокада II—III степени.
Существуют различные системы электрокардиостимуляторов. Первая имплантация постоянного электрокардиостимулятора произведена в 1958 г.
 Рис. 17.7. Трансвенозная установка электрода, дающего импульс имплантированному униполярному электрокардиостимулятору.
Рис. 17.7. Трансвенозная установка электрода, дающего импульс имплантированному униполярному электрокардиостимулятору.
1 — электрод; 2 — синоатриальный узел; 3 — атриовентрикулярный узел; 4 — место нарушения передачи атриовентрикулярного импульса; 5 — правый желудочек.
В настоящее время сотни тысяч пациентов с нарушениями ритма носят имплантируемые стимуляторы.
Наиболее часто имплантируют стимулятор системы "де-манд" (от англ. demand — запрос, требование), который включается и выключаются автоматически ("по запросу") только тогда, когда число сокращений сердца становится ниже заданного (обычно менее 60—72 в 1 мин). Электрокардиостимулятор (рис. 17.7) обычно имплантируют через разрез по линии sulcus deitoideopectoralis в подкожную жировую клетчатку подключичной области. Электроды проводят через подключичную вену в правый желудочек. При установке электродов определяют оптимальное место для стимуляции сокращений сердечной мышцы. Технический прогресс позволил создать программируемые водители ритма. С помощью специального прибора, устанавливаемого снаружи над имплантированным электрокардиостимулятором, можно изменять частоту импульсов, их амплитуду и продолжительность.
Дальнейшим успехом в конструировании электрокардиостимуляторов явилось создание и применение "физиологических последовательных водителей ритма", подающих импульс через предсердие, а при отсутствии ответа — через желудочек. При этом через вену вводят два электрода: в правое предсердие и в правый желудочек.
|
|
|
В качестве источника электроэнергии в стимуляторах используют преимущественно литиевые батареи, длительность работы которых достигает 5—7 лет и более.
17.10.2. Тахикардии
Условно различают желудочковые и наджелудочковые тахикардии.
Желудочковые тахикардии подразделяют на врожденные (15 %) и приобретенные (85 %, встречающиеся у мужчин). Желудочковая тахикардия обычно возникает на фоне коронарной недостаточности или другого тяжелого заболевания сердца (хроническая аневризма, рубцовые изменения после перенесенного инфаркта миокарда, пролапс левого предсердно-желу-дочкового клапана). Причиной желудочковой тахикардии иногда является интоксикация препаратами наперстянки.
Анатомической основой врожденной желудочковой тахикардии служит аномалия структуры миофибрилл сократительного миокарда.
Клиническая картина и диагностика. При частоте сердечных сокращений 140—240 в 1 мин симптоматика обусловлена снижением сердечного выброса. На ЭКГ определяют расширение желудочкового комплекса, предсердно-
желудочковую диссоциацию: предсердия сокращаются реже, чем желудочки.
Желудочковая тахикардия опасна для жизни больного, так как в любой момент может возникнуть фибрилляция желудочков.
Лечение. Борьбу с приступом желудочковой тахикардии начинают с внутривенного введения лидокаина из расчета 1 мг на 1 кг массы тела больного. При неэффективности лидокаина применяют новокаинамид до 100 мг каждые 5 мин, доводя суммарную дозу до 1000 мг. При отсутствии эффекта применяют электрическую дефибрилляцию.
Не поддающуюся перечисленным лечебным мероприятиям желудочковую тахикардию снимают программированной электрокардиостимуляцией. Для этого в правое предсердие вводят специальный четырехполюсный электрод и применяют соответствующую аппаратуру для электростимуляции.
|
|
|
Разработаны специальные имплантируемые системы для программируемой стимуляции и антитахикардической электрической дефибрилляции. Имплантированный дефибриллятор с помощью воспринимающих датчиков "распознает" высокочастотную желудочковую аритмию и через расположенные на поверхности сердца электроды в нужный момент производит дефибрилляцию.
Для радикального лечения желудочковых тахикардии предложен ряд хирургических операций: круговая эндокардиальная вентрикулотомия, эндо-кардиальная резекция проводящих путей миокарда, эндокардиальная крио-деструкция, электродеструкция, лазерная деструкция. Целью этих вмешательств является разрушение "аритмической" ткани миокарда.
Наджелудочковые тахикардии подразделяют на синусно-предсердные, внутрипредсердные, внутриузловые предсердно-желудочковые и эктопические предсердные тахикардии. Наиболее часто возникают узловые, затем синусовые и, наконец, внутрипредсердные тахикардии.
Наджелудочковые тахикардии проявляются на фоне ревмокардита, ИБС, тиреотоксикоза, врожденных пороков сердца, острого перикардита, острого инфаркта миокарда. Часто наджелудочковая тахикардия является симптомом синдрома Вольфа—Паркинсона—Уайта.
Наджелудочковая тахикардия может быть обусловлена наличием дополнительных проводящих путей (пучки Кента в виде мостиков сократительного миокарда, соединяющих миокард предсердия и желудочка).
В основе механизма лежит повторный вход возбуждения — reentry. Импульс приходит к миокарду желудочков по дополнительному пути быстрее, чем по нормальному, и возбуждение миокарда желудочков сердца наступает раньше. Такая патология называется синдромом предвозбуждения желудочков.
Электрокардиографическим выражением предвозбуждения желудочков является синдром Вольфа—Паркинсона—Уайта.
Показаниями к хирургическому устранению дополнительных проводящих путей являются возникновение тахиаритмий, резистентных к лекарственной терапии, и сочетай синдрома Вольфа—Паркинсона—Уайта с мерцательной аритмией, что может стать причиной внезапной смерти.
Для установления точной локализации дополнительных путей проводят картирование аритмогенной ткани через полости сердца. Устраняют дополнительные пути проведения импульсов возбуждения различными методами: пересечением, криодеструкцией или разрушением их электрическим током.
Наджелудочковая тахикардия, обусловленная механизмом reentry (синдром повторного входа возбуждения), может проявляться на фоне ревмокардита, ИБС, тиреотоксикоза и других заболеваний.
Клиническая картина и диагностика. Больных беспокоят приступы сердцебиений с частотой 160—260 в 1 мин от одного раза в год до нескольких раз в день. В зависимости от частоты приступов, состояния миокарда, наличия сопутствующей ИБС жалобы могут быть различными: от головокружения и общей слабости до обморочных состояний.
На ЭКГ комплексы QRS не расширены, зубец Р наслаивается на зубец Т предыдущего сокращения. В переходный период между тахиаритмией и синусовым ритмом может возникнуть асистолия до нескольких секунд с последующим восстановлением синусового ритма.
Лечение. Приступ можно устранить раздражением блуждающего нерва (вагусной пробой — надавливанием на глазные яблоки), введением проти-воаритмических препаратов, электрической дефибрилляцией. Хирургическое лечение заключается в резекции синусно-предсердного узла или создании Полной поперечной блокады с последующей имплантацией электрокардиостимулятора. Новейшим методом является имплантация антитахи-кардического стимулятора.
Глава 18 АОРТА И ПЕРИФЕРИЧЕСКИЕ АРТЕРИИ
Аорта подразделяется на восходящую часть (pars aortae ascendens), дугу (arcus aortae) и нисходящую часть (pars clescendens aortae), состоящую из грудного и брюшного отделов. От дуги аорты отходят артерии, участвующие в кровоснабжении головного мозга и верхних конечностей (плечеголовной ствол, левая общая сонная и левая подключичная артерии). Плечеголов-ной ствол делится на правые общую сонную и подключичную артерии. В каротидном треугольнике общая сонная артерия делится на наружную и внутреннюю. Наружная сонная артерия и ее ветви кровоснабжают большую часть лица и шеи. Внутренняя сонная артерия на шее ветвей не отдает, идет круто вверх, через каротидный канал проникает в полость черепа к основанию мозга. От подключичных отходят позвоночные артерии. Позвоночная артерия попадает в полость черепа через большое затылочное отверстие. На основании мозга внутренние сонные и позвоночные артерии образуют артериальное кольцо (виллизиев круг). Подключичные артерии продолжаются в подмышечные. Подмышечная артерия переходит в плечевую артерию, конечными ветвями которой являются лучевая и локтевая артерии. Они в свою очередь дают начало более мелким ветвям, обеспечивающим кровоснабжение кисти.
Брюшная аорта отдает ветви, кровоснабжающие желудочно-кишечный тракт (чревный ствол, верхняя и нижняя брыжеечная артерии), почки (почечные артерии) и нижние конечности (правая и левая общие подвздошные артерии). Общая подвздошная артерия делится на внутреннюю и наружную подвздошную артерии. Наружная подвздошная артерия продолжается в бедренную артерию, самой крупной ветвью которой является глубокая артерия бедра, отходящая от латеральной поверхности ее ниже паховой связки. В области подколенной ямки бедренная артерия переходит в подколенную артерию, которая делится на переднюю и заднюю большеберцовые артерии. Последняя дает начало малоберцовой артерии. Конечные ветви этих трех артерий голени обеспечивают кровоснабжение стопы.
Стенки артерий состоят из трех оболочек: наружной, или адвентиции (tunica externa), средней (tunica media) и внутренней (tunica intima). Адвентиция образована рыхлой соединительной тканью — продольными пучками коллагеновых волокон, включающих и эластические волокна, которые особенно выражены на границе со средней оболочкой. Средняя оболочка представлена несколькими слоями циркулярно расположенных гладких мышечных волокон, среди которых имеется сеть эластических волокон, образующих с эластическими элементами адвентиции и интимы общий каркас артериальной стенки. Интима артерии образована эндотелием, базальной мембраной и субэндотелиальным слоем, включающим тонкие эластические волокна и звездчатые клетки. За ним располагается сеть толстых эластических волокон, образующих внутреннюю эластическую мембрану. В зависимости от преобладания в стенках сосудов тех или иных морфологических элементов различают артерии эластического, мышечного и смешанного типов.
Кровоснабжение стенок артерий осуществляется за счет собственных артериальных и венозных сосудов (vasa vasonim). Питание артериальной стенки происходит за счет ветвей мелких
периартериальных сосудов. Они проникают через адвентицию и, дойдя до средней оболочки, образуют в ней капиллярную сеть. Интима не имеет кровеносных сосудов.
Иннервацию артерий обеспечивает симпатическая и парасимпатическая нервная система. Важная роль в регуляции сосудистого тонуса принадлежит хемо-, баро- и механорецепторам, находящимся в большом количестве в стенках артерий, в особенности в зоне бифуркации обшей сонной артерии (синокаротидная зона). Лимфоотток от стенок артерий осуществляется по собственным лимфатическим сосудам (vasa lymphatica vasorum).
Непосредственным продолжением артериальной сети является система микроциркуляции, объединяющая сосуды диаметром 2—100 мкм. Каждая морфологическая единица микроцирку-ляторной системы включает 5 элементов: 1) артериолу; 2) предкапиллярную артериолу; 3) капилляр; 4) посткапиллярную венулу и 5) венулу. В микроциркуляторном русле происходит транскапиллярный обмен, обеспечивающий жизненные функции организма. Он осуществляется на основе фильтрации, реабсорбции, диффузии и микровезикулярного транспорта. Фильтрация происходит в артериальном отделе капилляра, где сумма величин гидростатического давления крови и осмотического давления плазмы в среднем на 9 мм рт. ст. превышает значение онкотического давления тканевой жидкости. В венозном отделе капилляра имеются обратные взаимоотношения величин указанных давлений, что способствует реабсорбции ин-терстициальной жидкости с продуктами метаболизма. Исходя из этого, любые патологические процессы, сопровождающиеся повышенной проницаемостью капиллярной стенки для белка, ведут к уменьшению онкотического давления, а следовательно, и к снижению реабсорбции.
18.1. Методы исследования
При большинстве сосудистых заболеваний сопоставление жалоб, анамнеза и данных объективного физикального исследования позволяет установить правильный диагноз. Специальные методы, как правило, лишь детализируют его. Функциональные пробы позволяют определить степень недостаточности кровоснабжения в обследуемой части тела вне зависимости от характера заболевания и причины, вызвавшей нарушение кровоснабжения. Инструментальные исследования уточняют локализацию и характер поражения, степень нарушения кровотока в артериях и компенсаторные возможности кровообращения. Они имеют важное значение при планировании оперативного вмешательства и для последующего наблюдения. Все функциональные методы исследования в основном уточняют степень артериальной недостаточности и ишемии и не дают представления о локализации и характере заболевания магистральных артерий.
Жалобы и анамнез имеют важное значение для диагностики сосудистых поражений. Они изменяются в зависимости от органа, в котором произошло нарушение кровоснабжение, и выполняемых им функций. При нарушении кровоснабжения ЦНС будет преобладать неврологическая симптоматика, при окклюзии внутренней сонной артерии часто развивается гемипарез. Окклюзия верхней брыжеечной артерии может проявляться симптомами angina abdominalis, гангреной кишечника. При стенозе и окклюзии подвздошных и бедренных артерий появляются перемежающаяся хромота, импотенция, боли в ногах в покое, бледность стоп, запустение вен, гангрена пальцев или всей стопы.
Пальпация пульса на артериях — важнейшее клиническое исследование в оценке состояния артериального кровообращения. Определяют наполнение и напряжение пульса на симметричных участках головы и шеи (височная, общая сонная артерии), на верхней конечности (плечевая, лучевая артерии), нижней конечности (бедренная, подколенная, задняя болыиеберцо-вая артерии, артерия тыла стопы). При атеросклеротическом поражении артерия прощупывается вне пульсовой волны в виде плотного, трудносжимае-мого тяжа. При пальпации живота обращают внимание на пульсацию брюшной аорты. Пульс определяют в следующих местах: на височной артерии — кпереди от козелка ушной раковины; на бифуркации общей сонной
артерии — позади угла нижней челюсти, на лучевой артерии — на ладонной поверхности лучевой стороны предплечья на 2—3 см проксимальнее линии лучезапястного сустава; на плечевой артерии — во внутреннем желобке двуглавой мышцы; на артерии тыла стопы — между I и II плюсневыми костями; на задней большеберцовой артерии — между задненижним краем внутренней лодыжки и ахилловым сухожилием; на подколенной артерии — в глубине подколенной ямки при положении больного на животе и при согнутой в коленном суставе под углом 120° голени; на бедренной артерии — ниже паховой связки, на 1,5—2 см кнутри от ее середины; на брюшной аорте — по средней линии живота выше и на уровне пупка.
Аускультация сосудов является обязательным компонентом обследования больных. В норме над магистральными артериями выслушивается тон удара пульсовой волны, при стенозе или аневризматическом расширении артерий возникает систолический шум. Аускультацию проводят над проекцией сонных и подключичных артерий, брахиоцефального ствола, позвоночных артерий, восходящей и брюшной аорты, чревного ствола, почечных, подвздошных и бедренных артерий. При этом шумы с левой подключичной артерии выслушивают сзади грудиноключично-сосцевидной мышцы, у места ее прикрепления к ключице. Справа в этой же точке можно определить шум с брахиоцефального ствола. Шумы с позвоночных артерий проецируются на 2 см проксимальнее середины ключицы, с восходящей аорты — во втором межреберье справа от грудины. По средней линии живота под мечевидным отростком выслушивается шум с чревного ствола при его стенозе. По параректальной линии на середине расстояния между горизонтальными линиями, мысленно проведенными через мечевидный отросток и пупок, выслушивается шум с почечных артерий. По средней линии на уровне пупка и выше локализуются шумы с брюшной аорты. Шум с подвздошных артерий проецируется по линии, соединяющей брюшную аорту с точкой, расположенной на границе внутренней и средней трети паховой связки. Аускультацию бедренной и общей сонной артерий производят в местах, где определяется их пульсация. При выслушивании сосудов шеи следует различать шумы от стеноза артерии и сердечные шумы, интенсивность которых возрастает по мере приближения к сердцу. При аневризмах сосудов и арте-риовенозных свищах максимальная интенсивность шумов отмечается в местах их локализаций.
Определение артериального давления целесообразно производить на четырех конечностях. При измерении артериального давления на ноге на бедро накладывают манжетку от сфигмоманометра и в положении больного на животе выслушивают тоны Короткова над подколенной артерией. Можно определять только систолическое давление, пальпируя первые пульсовые колебания одной из артерий стоп после выпускания воздуха из раздутой манжетки. В норме давление на нижних конечностях равно давлению на верхних или на 20 мм рт. ст. выше. Разница в давлении на симметричных конечностях более 30 мм рт. ст. свидетельствует о нарушении артериальной проходимости. Высокое систолическое давление на верхних конечностях при его резком снижении или отсутствии на нижних конечностях характерно для коарктации аорты.
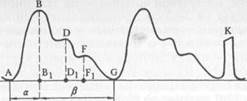
Инструментальная диагностика. Реография — наиболее доступный и простой метод. Она основана на регистрации колебаний электрического сопротивления тканей, меняющегося в зависимости от кровенаполнения конечности! Реографическая кривая в норме (рис. 18.1) характеризуется крутым и быстрым повышением пульсовой волны (АВ), четкой вершиной (В), наличием двух дополнительных зубцов (D, F) в нисходящей части (катакрота). С ее помощью можно определить время распространения пульсовой волны
|
| Рис. 18.1.Рсограмма (норма). Объяснение в тексте. |
(а), скорость максимального кровенаполнения исследуемого сегмента (в) и ряд других показателей, среди которых наиболее информативным является величина реографического индекса — производная от отношения амплитуды основной волны реогра-фической кривой (В—В1) к высоте калибровочного сигнала (К).
Ультразвуковая допплерогра-фия (УЗДГ) несет информацию о
физиологии кровотока. В основу метода был положен известный принцип Допплера, согласно которому ультразвуковой сигнал изменяет свою частоту при отражении от движущихся частиц (элементов крови). Метод основан на регистрации разности частот посылаемого и отраженного ультразвукового сигнала, которая изменяется пропорционально скорости кровотока. УЗДГ позволяет изучать движущиеся структуры (потоки крови): производить графическую регистрацию кровотока, количественную и качественную оценку его параметров, измерять регионарное артериальное давление.
Ультразвуковое сканирование в реальном масштабе времени дает информацию об анатомии сосудов. Для получения изображения используется свойство отражения ультразвуковой волны от сред с различным акустическим сопротивлением. Таким образом удается получить информацию не только о просвете, но и о состоянии стенки сосуда, окружающих тканях и происходящих в них морфологических изменениях, определить причины нарушения кровообращения.
Дальнейшее совершенствование средств ультразвуковой диагностики предопределило появление дуплексного сканирования (ДС) — метода, который сочетает в себе возможности анатомического и функционального исследования сосудов. В приборах ДС используются как свойство отражения ультразвуковой волны, так и свойство изменения ее частоты. С возникновением ДС появилась возможность одновременно и визуализировать изучаемый сосуд, и получать физиологическую информацию о параметрах кровотока.
В последние годы возможности ДС были расширены за счет новых технологий с использованием эффекта Допплера. Это эхо-допплеровская цветная визуализация кровотока или цветовое допплеровское картирование (ЦДК) потока. ЦДК представляет собой обычное двухмерное изображение в серой шкале в реальном времени, на которое накладывается информация о допплеровском сдвиге частот, представленная в цвете. Сигналы, отражающиеся от неподвижных тканей, представляются в серой шкале. Если вернувшийся эхо-сигнал имеет частоту, отличающуюся от посланной датчиком, то наблюдается допплеровское смещение, связанное с движением объекта (эффект Допплера). В любом месте, где был обнаружен допплеровский сдвиг частот, его направление, средняя величина и отклонение представляются в цветовом коде. Разноцветное кодирование потока облегчает поиск сосудов, позволяет быстро дифференцировать артерии и вены, проследить анатомические изменения просвета и стенки сосуда, судить о направлении кровотока, получать изображение мелких, разветвленных сосудов.
Компьютерная томография основана на получении послойных поперечных изображений человеческого тела с помощью вращающейся вокруг него рентгеновской трубки. Она позволяет визуализировать поперечные сечения
 аорты и устьев ее ветвей (подвздошных, брыжеечных, почечных артерий, чревного ствола, брахиоцефальных артерий), судить о состоянии их стенок, взаимоотношениях с окружающими тканевыми структурами. Для исследования сосудов (КТ-ангиографии) используются спиральные или электронно-лучевые компьютерные томографы, которые позволяют получать большое количество срезов за минимальное время. Тем самым появляется возможность изучать быстро протекающие динамические процессы, в том числе движение болюса контрастного вещества в артериях. Для получения изображений артерий внутривенно при помощи автоматического шприца вводят неионный контрастный препарат. Визуализация осуществляется в артериальную фазу введения контраста с учетом времени его циркуляции.
аорты и устьев ее ветвей (подвздошных, брыжеечных, почечных артерий, чревного ствола, брахиоцефальных артерий), судить о состоянии их стенок, взаимоотношениях с окружающими тканевыми структурами. Для исследования сосудов (КТ-ангиографии) используются спиральные или электронно-лучевые компьютерные томографы, которые позволяют получать большое количество срезов за минимальное время. Тем самым появляется возможность изучать быстро протекающие динамические процессы, в том числе движение болюса контрастного вещества в артериях. Для получения изображений артерий внутривенно при помощи автоматического шприца вводят неионный контрастный препарат. Визуализация осуществляется в артериальную фазу введения контраста с учетом времени его циркуляции.
Магнитно-резонансная томография сосудов (МР-ангиография) дает возможность проводить исследования сосудов без введения контрастных веществ в нескольких взаимно перпендикулярных плоскостях. Развитию техники МРА способствовали наблюдения, показывающие, что движущийся поток при некоторых условиях может вызывать изменения МР-сигнала. В результате были разработаны программы, предназначенные для изучения сосудистых структур, нацеленные на усиление сигнала потока крови с одновременным погашением сигнала от неподвижных тканей. Для получения МР-изображения более высокого качества рекомендуется исследование на фоне введения контрастных средств (парамагнетиков). При проведении КТ-или МР-ангиографии существует возможность последующей реконструкции двухмерных изображений в трехмерные. Отдельные срезы изучаются последовательно, с переходом от одного к другому. Информация, полученная по каждому срезу, сохраняется. Затем при помощи компьютеризированной рабочей станции из серии срезов создается трехмерная модель изучаемого сегмента сосудистого русла, на которой отчетливо видна анатомия и топография исследуемых участков. Производя "вращение" объекта, можно исследовать интересующие зоны в различных плоскостях, под разным углом зрения, а также проводить "виртуальную ангиоскопию" — заглянуть внутрь изучаемого сосуда.
Рентгеноконтрастная ангиография — рентгенологическое исследование с контрастными препаратами, вводимыми в просвет сосуда. По способу введения различают: 1) пункционную артериографию, при которой контрастное вещество вводят непосредственно в одну из периферических артерий (бедренную, плечевую), пунктируя их через кожу; 2) аортоартериографию по Сельдингеру, при которой в тот или иной отдел аорты ретроградно через периферическую артерию (бедренную, плечевую) проводят специальный рентгеноконтрастный катетер, устанавливаемый в устье изучаемой артерии, и вводят контрастное вещество, выполняя серию снимков; 3) транслюм-бальную аортографию, при которой аорту пунктируют специальной иглой на уровне XII грудного или I поясничного позвонков. Аортоартериография по Сельдингеру является предпочтительным способом контрастирования.
С помощью ангиографических установок нового поколения можно получать дигитальное (цифровое) субтракционное изображение артерий после введения сравнительно небольших доз контрастного вещества. В основе дигитальной субтракционной ангиографии лежит принцип компьютерного вычитания (субтракции) изображений, записанных в памяти компьютера — снимков до и после ведения в сосуд рентгеноконтрастного вещества. Благодаря этому достигается высокое качество изображений, уменьшается количество вводимого контрастного вещества, появляется возможность внутривенного контрастирования без пункции или катетеризации артерий.
18.2. Общие принципы лечения заболеваний артерий
Существует несколько способов уменьшения или полного устранения симптомов ишемии и предотвращения прогрессирования сосудистой окклюзии:
— нехирургические методы лечения (устранение факторов риска, трени
ровочная ходьба и фармакологическая терапия);
— хирургическое методы лечения (эндартерэктомия, шунтирование, про
тезирование, операции на симпатической нервной системе и др.);
— интервенционные радиологические (рентгеноэндоваскулярные) вме
шательства (баллонная дилатация, установка стента, эндопротезирование).
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 574; Нарушение авторских прав?; Мы поможем в написании вашей работы!