
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энтропия как мера вероятности состояния системы. Зависимость энтропии от различных факторов. Стандартная энтропия
|
|
|
|
Направленность физико-химических процессов
Система самопроизвольно переходит в состояние, которое характеризуется бóльшей вероятностью. Вместо вероятности состояния, для расчёта которой необходимо знать микроскопические характеристики – мгновенные положения в пространстве и скорости движения – для всех молекул системы, удобнее рассматривать некоторое макроскопическое свойство системы – энтропию (S), которая связана с вероятностью состояния системы соотношением:
S = R ln W, (10)
где S – энтропия, отнесённая к одному молю вещества;
R – универсальная газовая постоянная, равная 8,31 Дж/моль·К;
W – вероятность данного состояния, т.е. число способов, которыми можно осуществить данное состояние.
Так как ln W – величина безразмерная, то размерность энтропии совпадает с размерностью R (Дж/моль·К).
Итак, энтропия является мерой вероятности состояния системы. Наиболее вероятным является наиболее хаотическое, наиболее беспорядочное состояние системы. Энтропию называют мерой «беспорядка» системы.
В изолированных системах самопроизвольно протекают процессы, ведущие к увеличению энтропии, т.е. процессы для которых
DS = S2 – S1 > 0. (11)
Значения энтропий, отнесённые к 1 молю вещества и рассчитанные для стандартных условий, обозначают 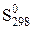 . Для некоторых веществ
. Для некоторых веществ 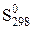 даны в таблице приложения.
даны в таблице приложения.
Энтропия системы зависит:
От объёма системы. Чем больше объём, занимаемый молекулами, тем более вероятно состояние системы и тем больше S.
От давления в системе. Чем больше давление в системе, тем меньше
(при Т = const) объём, занимаемый молекулами в системе, и, следовательно, меньше S.
От температуры. При повышении температуры увеличивается объём системы (при Р = const), возрастает хаотичность, беспорядочность движения молекул, поэтому возрастает вероятность состояния системы, и, следовательно, S. Напротив, при понижении температуры энтропия уменьшается.
|
|
|
От агрегатного состояния вещества. В твёрдом теле (кристалле) возможно только колебательное движение молекул, в жидкости – и колебательное, и вращательное движение, в газе кроме колебательного и вращательного появляется ещё и поступательное движение молекул, вносящее наибольший вклад в энтропию.
Таким образом, всегда при фазовом переходе: тв ® ж ® г
Sтв < Sж << Sг.
От природы вещества. Для веществ, находящихся в одном и том же фазовом состоянии, энтропия увеличивается с усложнением молекулы, так как при этом повышается молекулярная масса вещества и увеличиваются возможности внутримолекулярного колебательного и вращательного движений.
|
|
|
|
|
Дата добавления: 2015-05-10; Просмотров: 2389; Нарушение авторских прав?; Мы поможем в написании вашей работы!