
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Критерії оцінювання
|
|
|
|
Список літератури
1 Гамеева О.С. Физическая и коллоидная химия.- М.: Высшая школа, 1974.
2 Ахметов Б.В., Новиченко Ю.П., Чапурин В.И. Физическая и коллоидная химия. -Л.: Химия, 1986.
3 Ахметов Б.В. Задачи и упражнения по физической и коллоидной химии.- Л.: Химия, 1988.
4 Гамеева О.С. Сборник задач и упражнений по физической и коллоидной химии.-
М.: Высшая школа, 1980.
5 Усков І.О., Єременко Б.В., Пелішенко С.С., Нижник В.В.
Колоїдна хімія з основами фізичної хімії високомолекулярних сполук. – К.: Вища шк., 1995.
6 Краткий справочник физико-химических величин. Под редакцией К.П.Мищенко, А.А.Равделя. Л.Химия,1974.
7 Балезин С.А. Практикум по физической и коллоидной химии – М.: Просвещение,1980.
8 Киреев В.А. Курс физической химии. – М.: Химия, 1975.
9 Практикум по физической химии. Под ред. Н.К.Воробьёва. – Л.: Химия, 1986.
10 Кубасов В.Л., Зарецкий С.А. Основы электрохимии. – М.: Химия, 1985.
Оцінка "5" – не менше 85% правильних відповідей.
Оцінка "4" – не менше 55% правильних відповідей.
Оцінка "3" – не менше 35% правильних відповідей.
При виставленні оцінки враховується дотримання терміну виконання самостійної роботи.
Тема 1 Молекулярно-кинетична теорія агрегатних станів речовини
Мета: - знати загально-наукове та прикладне значення фізичної та колоїдної хімії;
- знати напрямки її подальшого розвитку;
- вміти порівняти властивості газів, рідин та твердих речовин;
- знати особливості реальних газів, їх відмінність від ідеальних;
- вміти визначити властивості реального газу за ізотермами;
- знати рівняння Ван-дер-Ваальса;
- знати способи одержання та умови існування плазми;
- знати приклади використання плазми.
1.1 Вступ. Предмет фізичної хімії. Ломоносов М.В. – засновник фізхімії. Внесок вітчизняних та закордонних вчених у розвиток фізхімії. Досягнення сучасної фізхімії і нові напрямки її подальшого розвитку. Загально-наукове та прикладне значення фізхімії. Використання законів та висновків фізичної та колоїдної хімії.
|
|
|
1.2 Порівняння агрегатних станів речовин з точки зору кинетичної енергії сил взаємодії між ними.
Для кожного питання вибрати правильну відповідь
| № | Питання | № | Відповідь |
| Агрегатні стани однієї речовини відрізняються | хімічним складом | ||
| хімічними властивостями | |||
| фізичними властивостями | |||
| Молекули знаходяться на порявняно великих відстанях одна від одної у | газах | ||
| рідинах | |||
| твердих речовинах | |||
| Мають власний об'єм | гази | ||
| рідини | |||
| тверді речовини | |||
| Сили тяжіння урівноважуються силами відштовхування у | газах | ||
| рідинах | |||
| твердих речовинах | |||
| Мають власну форму | гази | ||
| рідини | |||
| тверді речовини | |||
| В хаотичному поступальному русі знаходяться молекули | газу | ||
| рідини | |||
| твердої речовини |
1.3 Реальні гази. Особливості реальних газів. Ізотерми реальних газів. Критичні параметри речовини. Рівняння Ван-дер-Ваальса.
Навести математичний запис рівняння Ван-дер-Ваальса та пояснити зміст констант.
Відмітити основні особливості реальних газів порівняно з ідеальними газами.
1.3 Реальні гази. Ізотерми реальних газів. Критичні параметри речовини.
Для кожного питання вибрати правильну відповідь з трьох, розташованих у тій же горизонтальній графі
| № | Питання | Відповіді | |||
| Гр.1 | Гр.2 | Гр.3 | |||
 Рисунок 1 – Ізотерма реального газу
Рисунок 1 – Ізотерма реального газу
|  V, м3/кмоль
Рисунок 2 – Ізотерми оксиду карбону (ІV) V, м3/кмоль
Рисунок 2 – Ізотерми оксиду карбону (ІV)
| ||||
| Яка ділянка ізотерми (рис.1) характеризує газуватий стан? | CD | AB | BC | ||
| Яка ділянка ізотерми (рис.1) характеризує рідкий стан? | AB | BC | CD | ||
| Яка ділянка ізотерми (рис.1) характеризує перехідний стан із рідини у газ? | AB | CD | BC | ||
| По ізотермам СО2 (рис.2) визначити критичну температуру вуглекислого газу | 400C | 100C | 31,30C | ||
| Чи можливо за t=800С отримати у рідкому стані СО2 (рис.2) | Можливо, тому, що дана температура вища критичної | Неможливо, тому, що дана температура вища критичної | Можна, якщо збільшити тиск | ||
| Що називається критичною температурою? | Температура, нище якої газ не може бути зконденсований ні при якому тиску | Температура, вище якої газ не може бути зконденсований ні при якому тиску | Температура конденсації газу | ||
| Якими параметрами характеризується критичний стан речовини? | Tкр pкр Vкр | Tкр pкр | pкр Vкр | ||
| Які існують способи зниження температури? | Розширення зтисненого реального газу | Розширення ідеального газу | Зтиснення реального газу | ||
| Що називається ефектом Джоуля – Томсона? | Температурний ефект, який супроводжується зміною об’єму газу | Температурний ефект, який супроводжується зміною об’єму газу при його розширенні без теплообміну з навколишнім середовищем | Тепловий ефект, який відбувається з витратами енергії | ||
1.4 Плазма. Загальна характеристика властивостей, засоби генерування, умови існування плазми.
|
|
|
Плазма в енергетиці майбутнього.
Для кожного питання вибрати правильну відповідь
| № | Питання | № | Відповідь |
| Інтенсивним рухом вільних заряджених часточок обумовлені | звичайна температура | ||
| висока температура | |||
| електрична проводимість | |||
| діелектричні властивості | |||
| Високотемпературна плазма має властивості | ідеального газу | ||
| реального газу | |||
| Плазма – іонізований газ, тому вона | заряджена негативно | ||
| заряджена позитивно | |||
| електронейтральна | |||
| Середні енергії часточок однакові незалежно від їх природи для | газорозрядної плазми | ||
| ізотермічної плазми | |||
| Способи генерування газорозрядної плазми | високочастотний розряд | ||
| електричний розряд | |||
| електричний струм | |||
| Для виробництва енергії можливо використовувати плазму | горячу | ||
| холодну | |||
| Назвати області використання гібридної плазми | зварювання | ||
| металургія | |||
| плазмохімія | |||
| термоядерні реакції |
|
|
|
Тема 2 Хімічна термодинаміка та термохімія
Мета: - вміти пояснити значення термодинаміки для вивчення хімічних процесів;
- знати основні поняття та визначення термодинаміки.
- знати формули розрахунку ентальпії для різних термодинамічних процесів;
- вміти за термохімічними рівняннями визначати тепловий ефект реакції;
- вміти характеризувати оборотні та необоротні процеси;
- вміти характеризувати самочинні оборотні процеси та межу їх протікання;
- знати застосування другого начала термодинаміки до хімічних та фізико - хімічних процесів.
2.1 Предмет термодинаміки, його суть та значення для вивчення хімічних процесів. Загальна характеристика, завдання термодинаміки.
Основні поняття та визначення: стан термодинамічної системи, термодинамічний процес.
Для кожного питання вибрати правильну відповідь
| № | Питання | № | Відповідь |
| Сукупність тіл, умовно відокремлених від навколишнього середовища називається | компонентом | ||
| фазою | |||
| термодинамічною системою | |||
| Система, що не має можливості теплообміну з навколишнім середовищем, називається | ізольованою | ||
| закритою | |||
| адіабатно – ізольованою | |||
| Хімічно індивідуальна складова частина термодинамічної системи називається | фазою | ||
| компонентою | |||
| однорідною | |||
| Частина або сукупність частин термодинамічної системи, що має однакові хімічні і фізичні властивості, називається | фазою | ||
| компонентою | |||
| гомогенною | |||
| Система, що складається з декількох фаз, відокремлених поверхнею розділу, називається | гомогенною | ||
| гетерогенною | |||
| неоднорідною | |||
| Властивості, що використовуються для вираження кількістних характеристик термодинамічної системи, називаються | інтенсивними | ||
| екстенсивними | |||
| параметрами стану |
|
|
|
Назвати розділи термодинаміки:
Визначити завдання термодинаміки:
2.2 Ентальпія системи для кожного термодинамічного процесу
2.2.1 Для кожного питання вибрати правильну відповідь
| № | Питання | № | Відповідь |
| Певному фізичному стану системи відповідає... значення її ентальпії | єдине | ||
| будь – яке | |||
| Ентальпія є величиною | екстенсивною | ||
| інтенсивною | |||
| Зміна ентальпії термодинамічної системи... від шляху процесу | залежить | ||
| не залежить | |||
| Сумарна зміна ентальпії системи в результаті циклічного процесу дорівнює | одиниці | ||
| нулю | |||
| Загальна зміна ентальпії системи в результаті послідовних стадій процесу... сумі змін ентальпій на всіх стадіях | дорівнює | ||
| не дорівнює | |||
| Ентальпія ідеального газу... однозначною функцією температури | являється | ||
| не являється | |||
| Зміна ентальпії у ізохоричному процесі | DH = n C p m DT | ||
| W T = Q T | |||
| DH = const | |||
| Зміна ентальпії у ізобаричному процесі | DH = n C p m DT | ||
| DH = Q p | |||
| DH = DU + P2V2 – P1V1 | |||
| Зміна ентальпії у ізотермічному процесі | DH = 0 | ||
| DH = n C p m DT | |||
| DH = const | |||
| Зміна ентальпії у адіабатичному процесі | DH = DU + P2V2 – P1V1 | ||
| DH = n C p m DT | |||
| DH = Q p |
2.3.2 Вказати номер правильної відповіді для даних задач
| № | Задача | № | Відповідь |
| При утворенні 1моля газуватого НF виділилось 268кДж. Чому дорівнює ентальпія утворення DHHF? | -268 кДж/моль +268 кДж/моль -134 кДж/моль +536 кДж/моль | ||
| При взаємодії 1моль водню і 2моль фтору виділилось 536 кДж. Визначити ентальпію утворення DHHF | -268 кДж/моль +536 кДж/моль -536 кДж/моль +134 кДж/моль | ||
| В суміші, яка складається з 22,4 л фтору і 22,4 л водню, відбулася реакція. Чому дорівнює тепловий ефект даної реакції? | -536 кДж/моль +536 кДж/моль -268 кДж/моль +268 кДж/моль | ||
| В суміші, яка складається з 22,4 л фтору і 22,4 л водню, відбулася реакція. Яка зміна ентальпії в цій реакції? | -134 кДж +53,6 кДж -53,6 кДж -26,8 кДж | ||
| Яка зміна ентальпії при дисоціації 1моль НF на молекули водню та фтору? | +536 кДж/моль -536 кДж/моль +134 кДж/моль +268 кДж/моль |
2.3 Тепловий ефект реакції, термохімічні рівняння.
Вказати одну правильну відповідь з чотирьох, запропонованих в одній горизонтальній графі
| Питання | Відповіді | № відповіді |
| 1 Яка права частина формули для DH =? | = Qv – Dn RT = U1 – U2 = - Qp = Cреаг - Спрод | |
| 2 Яка з хімічних реакцій екзотермічна? | N2 + O2 = 2NO – 180.103Дж 3C + 2Fe2O3 + 464 кДж = 4Fe + 3CO2 CH4 +2O2 = CO2 + 2H2O; DH = -87Дж 2C + 3H2 = C2H6; DH = 83кДж | |
| 3 При якому процесі Q p < Q v | H2 + I2 = 2HI CH4 + 2O2 = CO2 + 2H2O CO2 + C = 2CO CuO + H2 = Cu + H2O | |
| 4 Відмітити правильний запис твердження: теплота утворення NH3 дорівнює 46.103 Дж | N2 + 3H2 = 2NH3 + 46 кДж 1/2 N2 + 3/2 H2 = NH3 - 46 кДж 1/2 N2 + 3/2 H2 = NH3; DH= - 46 кДж 1/2 N2 + 3/2 H2 = NH3; DH= 46 кДж | |
| 5 Враховуючи дані 4Al +3O2 = 2Al2O3 +3346 кДж, вказати яке рівняння для 1моль Al2O3 та зміна ентальпії буде вірне | 2Al + 3/2O2 = Al2O3; DH= - 3346 кДж 2Al + 3/2O2 = Al2O3; DH= - 1674 кДж 2Al + 3/2O2 = Al2O3; DH= 3346 кДж 2Al + 3/2O2 = Al2O3; DH= 1674 кДж |
2.4 Необхідність у другому законі. Оборотні та необоротні процеси. Самочинні та несамочинні процеси. Межа протікання самочинних оборотних процесів. Застосування другого начала термодинаміки до хімічних та фізико - хімічних процесів.
Вказати правильну відповідь з запропонованих в горизонтальній графі
| № | Питання | № | Відповідь |
| Можливість протікання процесів та їх напрямленість визначає... начало термодинаміки | перше | ||
| друге | |||
| Процес, при якому система та навколишнє середовище повертається точно у вихідний стан називається | оборотним | ||
| необоротним | |||
| Якщо в результаті процесу в системі або навколишньому середовищі залишаються зміни, то процес називається | оборотним | ||
| необоротним | |||
| Процес, що відбувається в одному напрямку та не потребує витрат енергії ззовні, називається | оборотним | ||
| необоротним | |||
| самочинними | |||
| До певної межі відбуваються необоротні процеси | самочинні | ||
| несамочинні | |||
| Корисну роботу можна отримати за рахунок термодинамічного процесу | оборотного | ||
| необоротного | |||
| несамочинного | |||
| самочинного | |||
| Теплота термодинамічно необоротного процесу... теплоти термодинамічно оборотного процесу | менше | ||
| більше | |||
| Признаком самочинності протікання процесу є... термодинамічного потенціалу | зменшення | ||
| збільшення | |||
| За умови термодинамічної рівноваги величина термодинамічного потенціалу | максимальна | ||
| мінімальна | |||
| дорівнює нулю | |||
| Максимально можлива немеханічна робота системи при самочинному ізохоричному протіканні хімічного процесу дорівнює | зміні ізохорно – ізотермічного потенціалу | ||
| зміні енергії Гельмгольца | |||
| зміні енергії Гіббса |
Тема 3 Хімічна рівновага
Мета: - знати закон дії мас;
- вміти писати рівняння швидкості прямої та оборотної реакції;
- знати вирази константи рівноваги для гомогенної системи та формули зв'язку між ними;
- вміти пояснити значення спільного використання законів термодинаміки та хімічної кінетики для установлення оптимальних умов проведення хіміко-технологічних процесів.
3.1Оборотність хімічних реакцій. Швидкості прямої та оборотної реакції, закон дії мас. Рівновага в гомогенних системах. Установлення оптимальних умов проведення хіміко-технологічних процесів. Спільне використання законів термодинаміки та хімічної кінетики.
3.1.1 Знайти в гр.А і гр.В правильні відповіді на поставлені питання
Питання:
1. Що називається прямою реакцією?
2. Яка реакція називається оборотною?
3. Вказати визначення (гр.А) та приклади (гр.В) оборотних реакцій
4. Вказати визначення (гр.А) та приклади (гр.В) практично необоротних реакцій
5. Вказати визначення (гр.А) та рівняння (гр.В) момента хімічної рівноваги
6. Що називається «зсувом» хімічної рівноваги (гр.А)?
7. Чому дорівнює швидкість оборотної реакції (гр.А та гр.В)?
8. Вказати визначення (гр.А) та рівняння (гр.В) констант хімічної рівноваги
9. Які рівняння характеризують залежність між КР, КС, КN (гр.В)?
10. В яких хімічних реакціях КР = КС (гр.А та гр.В)?
Відповіді:
| № | Гр.А | № | Гр.В |
| різниці між швидкостями прямої та зворотної реакції | BaCl2 + CuSO4 = BaSO4 + CuCl2 | ||
| відношення констант швидкостей прямої та зворотної реакції | aA + bB <==> cC + dD CCC CDd = ------------ CAa CBb | ||
| реакція між вихідними речовинами | KC (RT)Sn | ||
| стан системи, за якого швидкості прямої та зворотної реакції однакові | KNO3 + NaCl = KCl + NaNO3 | ||
| хімічний процес між продуктами реакції | BaCl2 + K2CrO4 = BaCrO4 + 2KCl | ||
| момент хімічного процесу, коли запас вільної енергії мінімальний, а ентропії – максимальний | aA + bB <==> cC + dD PCC PDd = ------------ PAa PBb | ||
| хімічний процес, в якому продукти реакції можуть знову реагувати, утворюючи вихідні речовини за тих же умов | Na2S + 2HCl = 2NaCl + H2S | ||
| відношення добутку мольних рівноважних концентрацій продуктів реакції до добутку мольних рівноважних концентрацій вихідних речовин за даної температури (з урахуванням коефіцієнтів в рівнянні реакції) | CO(г) + H2O(п) <=> CO2(г) +H2(г) Sn = 0 | ||
| перехід від одного рівноважного стану до іншого, який визваний зміною умов реакції |   V – V = 0
V – V = 0
| ||
| тоді, коли в результаті реакції не відбувається зміни кількості молекул газу | = КN (RT / V) Sn | ||
| реакції, які практично можуть відбуватись тільки в одному напрямі за даних умов |  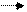 =V – V
=V – V
| ||
| відношення добутку рівноважних парціальних тисків продуктів реакції до добутку рівноважних парціальних тисків вихідних речовин, узятих в ступенях їх стехіометричних коефіцієнтів | Кпр = ----- Кзв |
3.1.2 КОНСТАНТИ ХІМІЧНОЇ РІВНОВАГИ
Для кожної задачі вибрати правильний хід вирішення з трьох, запропонованих в одній горизонтальній графі (номер задачі відповідає номеру графи).
1 В рівноважній системі І2 + Н2 <==> 2НІ СІ2 = а моль/л; СН2 = b моль/л; СНІ = с моль/л.
Визначити КС та вихідні концентрації (С|І2) йоду та водню (С|Н2).
2 В рівноважній системі N2 + 3Н2 <==> 2NН3 СN2 = а моль/л; СН2 = b моль/л;
СNH3 = с моль/л. Визначити КС та вихідні концентрації (С|N2) азоту та водню (С|Н2).
3 Виразити співвідношення між КС та КР для наступних реакцій:
1. 2СО + 2Н2 <==> СН4 + СО2
2. N2 + O2<==>2NO
3. 2CO2 <==> 2CO + O2
4. 3Fe + 4H2O <==> Fe3O4 + 4H2
4 Визначити концентрації речовин в момент рівноваги (С) для системи СО + Н2О <==> СО2 + Н2, якщо за Т = 930,5К КС = 1, а вихідні концентрації відповідно дорівнюють
ССО = а моль/л, СН2О = b моль/л, Т = 930,5К.
| № | Розв’язання | ||
| A | B | C | |
| KC = ab / c2 С|І2 = (c + a) моль/л С|Н2 = (c + b) моль/л | KC = c2 / ab С|І2 = (c / 2 + a) моль/л С|Н2 = (c / 2 + b) моль/л | KC = c2 / ab С|І2 = (c + a) / 2 моль/л С|Н2 = (c + b) / 2 моль/л | |
| KC = c2 / ab3 С|N2 = (1/2 c + a) моль/л С|Н2 = (3/2 c + b) моль/л | Kc = c / ab С|N2 = a моль/л С|Н2 = 3b моль/л | Kc = ab3 / c2 С|N2 = (c + a) моль/л С|Н2 = (c + b) моль/л | |
| 1 KP = KC (RT) -2 2 KP = KC (RT) 3 KP = KC (RT) 4 KP = KC (RT) -2 | 1 KP = KC 2 KP = KC (RT) -1 3 KP = KC (RT) 4 KP = KC (RT) | 1 KP = KC (RT) -2 2 KP = KC 3 KP = KC (RT) 4 KP = KC | |
| 1 С|Н2 = С|CO2 = x 2 CCO = (a – x)моль 3 СН2О = (b – х) моль х2 4 К = --------------- (а – х)(b – х) | 1 С|Н2 = С|CO2 = x 2 CCO = (a + x)моль 3 СН2О = (b + х) моль х2 4 К = ---------------- (а + х)(b + х) | 1 С|Н2 = x; С|CO2 = y 2 CCO = a моль 3 СН2О = b моль х у 4 К = ------- а b |
Примітка:
С| - вихідна концентрація відповідної речовини,
С – рівноважна концентрація відповідної речовини.
Тема 4 Хімічна кінетика
Мета: - знати приклади промислового використання ланцюгових реакцій, вибухових процесів, фото- хімічних реакцій та радіаційно-хімічних реакцій;
- знати особливості цих реакцій;
- вміти пояснити механізм ланцюгових реакцій.
4.1 Ланцюгові реакції та їх особливості. Механізм ланцюгових реакцій.
4.2 Вибухові процеси. Фото- хімічні реакції та радіаційно-хімічні реакції.
4.1.1 Назвати особливості ланцюгових процесів:
4.1.2 Закінчити речення:
Ланцюгові реакції відбуваються завдяки наявності в системі активних частинок – _____________________________________.
4.1.3Дати характеристику Типи ланцюгових реакцій

Реакції з енергетичними ланцюгами: Реакції з матеріальними ланцюгами:
розгалуженими ланцюгами розгалуженими ланцюгами
 |  |
нерозгалуженими ланцюгами нерозгалуженими ланцюгами
 |  |
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 460; Нарушение авторских прав?; Мы поможем в написании вашей работы!