
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергетические уровни молекул. Спектры молекул
Лазеры.
Принцип детального равновесия Коэффициенты Эйнштейна. Формула Планка.
Спонтанное и вынужденное излучение.
Явление комбинационного рассеяния света.
Обменное взаимодействие. Образование ковалентной связи.
Молекулы состоят из одинаковых или различных атомов, соединенных между собой в одно целое химическими связями. Молекулы – носители химических свойств вещества.
Cилы междуатомного взаимодействия в молекулах возникают между внешними, валентными, электронами атомов.
Об этом свидетельствуют следующие факты
- резкое изменение оптического спектра атомов при вступлении их в химическое соединение
- сохранение неизменным рентгеновского характеристического спектра атомов независимо от рода химических соединений, в которые входят эти атомы.
В молекулах отдельная спектральная линия возникает в результате изменения энергии молекулы. Полную энергию W молекулы можно рассматривать как состоящую из нескольких частей:
Wпост— энергии поступательного движения ее центра инерции,
Wэл— энергии движения электронов в атомах молекулы,
Wкол — энергии колебательного движения ядер атомов, входящих в молекулу, около их равновесных положений,
Wвр — энергии вращательного движения молекулы как целого
Wяд – энергии ядер атомов в молекуле:

Энергия Wnост поступательного движения молекулы (~ kT) не квантуется, и ее изменения не могут привести к созданию молекулярного спектра. Вклад движения ядер очень мал. Поэтому, энергия молекулы, определяющая ее оптические свой-, ства, будет состоять из суммы трех слагаемых:
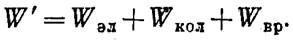
По правилу Бора, частота ν фотона, испускаемого молекулой при изменении ее энергетического состояния, равна
 (14-1)
(14-1)
где ΔWэл, ΔWкол, ΔWвр - изменения соответствующих частей энергии молекулы. Так как каждое из слагаемых (14-1) принимает ряд дискретных квантованных значений, то их изменения также имеют дискретные значения и поэтому спектр молекулы состоит из густо расположенных линий, образующих полосы.
По порядку величин

где m — масса электрона, а величина М имеет порядок массы ядер атомов в молекуле, т. е. m/М ~10-3-10-5, следовательно: Эти слагаемые имеют различную величину:
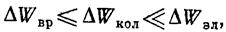
Спектральные линии вращательного спектра возникают при переходах в далекой инфракрасной области спектра (при длинах волн порядка 0,1-1 мм), и соответствуют изменению вращательной энергии молекулы.
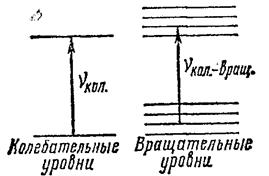
Вращательные уровни энергии можно найти квантованием вращательного движения молекулы, рассматривая её как твёрдое тело с определёнными моментами инерции.

В простейшем случае двухатомной или линейной многоатомной молекулы её энергия вращения
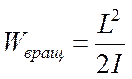 (14-2)
(14-2)
где I — момент инерции молекулы относительно оси, перпендикулярной оси молекулы, а L —момент импульса. Согласно правилам квантования,
 (14-3)
(14-3)
где вращательное квантовое число J = 0, 1, 2,..., и, следовательно, для Wвращ из (14-2) и (14-3) получим:

- вращательная постоянная
Линии колебательного спектра возникают при переходах между колебательными энергетическими уровнями молекулы (длины волн 1-10 мкм).
При изменении колебательных энергетических уровней молекулы одновременно изменяются иее вращательные энергетические состояния. Поэтому переходы между двумя колебательными уровнями сопровождаются изменением вращательных энергетических состояний, т. е. возникает колебательно-вращательныйспектр.
Колебательные уровни энергии (значения Wкол) можно найти квантованием колебательного движения, которое приближённо считают гармоническим. В простейшем случае двухатомной молекулы (одна колебательная степень свободы, соответствующая изменению межъядерного расстояния r) её рассматривают как гармонический осциллятор; его квантование даёт равноотстоящие уровни энергии:
Wкол = h νe (υ +1/2)
где νe — основная частота гармонических колебаний молекулы, υ — колебательное квантовое число, принимающее значения 0, 1, 2,...
Для каждого электронного состояния многоатомной молекулы, состоящей из N атомов (N ≥ 3) и имеющей f колебательных степеней свободы (f = 3 N — 5 и f = 3 N — 6 для линейных и нелинейных молекул соответственно), получается f нормальных колебаний с частотами νi (i = 1, 2, 3,..., f) и сложная система колебательных уровней:

где υ i = 0, 1, 2,... — соответствующие колебательные квантовые числа.
Электронные энергетические уровни возбуждаются в видимой и ультрафиолетовой областях спектра. Каждому электронному уровню соответствует определенное пространственное распределение электронов, принадлежащих атомам - определенная конфигурация электронов.
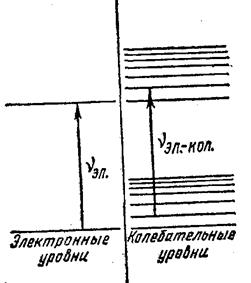
Каждой электронной конфигурации, каждому электронному энергетическому уровню молекулы будут соответствовать различные возможные колебания ядер в молекуле, т. е. целый набор колебательных энергетических уровней. Переходы между такими электронно-колебательными уровнями приводят к возникновению электронно-колебательного спектра молекулы.

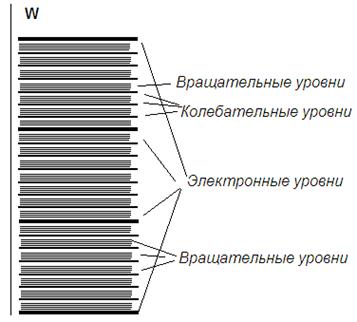
На каждое колебательное энергетическое состояние накладывается, кроме того, система вращательных уровней. Таким образом, каждому электронно-колебательному переходу будет соответствовать определенная полоса, поэтому весь электронно-колебательный спектр в видимой области представляет собой систему из нескольких групп полос – полосатый спектр.
|
|
Дата добавления: 2015-06-04; Просмотров: 2869; Нарушение авторских прав?; Мы поможем в написании вашей работы!