
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Сопоставление определений кислот и оснований
|
|
|
|
В системе из двух способных взаимодействовать с протоном веществ основанием считается то, которое сильнее притягивает протон (обладает большим протонным сродством). В рассмотренных примерах вода имеет большее значение протонного сродства, чем НF, но меньше, чем NН3.
Основание кислота
В этом равновесии участвуют 2 пары кислот и оснований, являющихся сопряженными. Кислоте НF соответствует сопряженное основание F–, а основанию NН3 — сопряженная кислота NН4+.
Кислота I основание II кислота II основание I.
В каждой конкретной реакции роль кислоты или основания может меняться в зависимости от партнера, с которым происходит взаимодействие. Например, вода по отношению к аммиаку является кислотой, а по отношению к фториду водорода — основанием:
| МН 3 Н2О основание |
| + Н2О + HF кислота |
<–> он- + мн4+,
<–> F- + н3о+,
Протолитическая теория Бренстеда—Лоури не может охватить весь спектр кислотно-основных взаимодействий. В 1924 г. Дж. Льюис предложил электронную теорию, которая дала возможность объединить все существующие кислотно-основные теории. По определению Дж. Льюиса, основание — это такая частица, которая способна предоставить пару электронов для образования ковалентной связи, а кислота — это такая частица, которая способна принять пару электронов с образованием ковалентной связи. Таким образом, для оснований общим свойством является наличие пары электронов, а для кислоты — пустой орбитали. В этом случае кислотно-основное взаимодействие идет по механизму образования ковалентной связи:
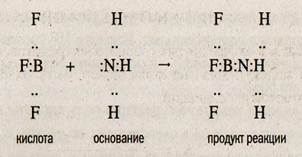
Сопоставление определений кислот и оснований различными теориями представлено в табл. 4.
Таблица 4
| По определению | Кислота | Основание |
| Аррениуса | Содержит Н* | Содержит ОН- |
| Бренстеда-Лоури | Донор Н* | Акцептор Н* |
| Льюиса | Акцептор электронной пары | Донор электронной пары |
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 378; Нарушение авторских прав?; Мы поможем в написании вашей работы!