
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химический потенциал- это энергия Гиббса, приходящаяся на 1 моль вещества в данной системе
|
|
|
|
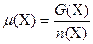 ;
; 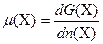
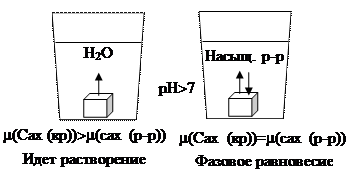
Химический потенциал не дается в справочных таблицах. Он служит для доказательств.
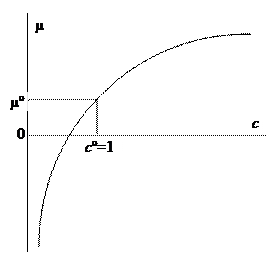
Химический потенциал вещества в растворе зависит от концентрации:
m(Х) = m°(Х) + RT ln c (X)
Это уравнение эвристическое, предложенное логическим путем для идеальных растворов. С ним возникает не мало сложностей. Далее вспомним об этом, когда в теории растворов будет введена активность вместо концентрации. При малых концентрациях m становится отрицательным, при больших – положительным (логарифмический график). Значение m° относится к стандартной концентрации с °= 1 моль/л.
Концентрация под знаком логарифма относительная:
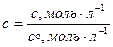 , причем стандартная концентрация принята равной 1 моль/л
, причем стандартная концентрация принята равной 1 моль/л
Применяем химический потенциал к вычислению D rG:
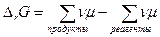
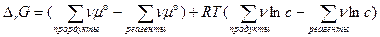
Первое слагаемое обозначаем как DG°, так как оно соответствует концентрациям равным 1, а второе по правилам преобразования логарифмов превращается в логарифм отношения произведений:
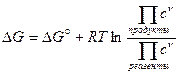 . (1)
. (1)
Полученное уравнение называется уравнением изотермы химической реакции. При концентрациях всех веществ с =1 значение D rG = D rG °. Вспомните, это было: стандартное изменение энергии Гиббса относится к концентрациям, равным 1. Все выражение под логарифмом далее будем коротко обозначать «П с». В учебниках встречается название произведение реакции. Пусть полученное уравнение не потрясает вас своей сложностью. Для конкретных реакций получаются вполне простые и краткие выражения.
 2NO2 N2O4. D rG = D rG ° + RT
2NO2 N2O4. D rG = D rG ° + RT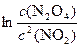
В случае реакций с участием газов, для них вместо концентраций применяются парциальные давления:
O2(г) + Hb(aq) = HbO2(aq)
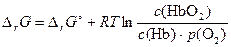
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 492; Нарушение авторских прав?; Мы поможем в написании вашей работы!