
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Бинарные соединения
Соединения с водородом. Гидриды щелочноземельных металлов ЭH2 - белые кристаллические вещества с ионной решеткой, анион Н-. Гидриды Be и Mg - твердые полимерные соединения. Термическая устойчивость гидридов понижается от Ва к Be.
Как технические, так и лабораторные способы получения гидридов Mg, Ca, Sr, Ва сводятся к нагреванию соответствующего металла в атмосфере Н2. BeH2 получают в эфирном растворе по реакции:
BeCl2 + 2LiH ® BeH2 + 2LiCl.
Гидриды ЭН2 - сильные восстановители, разлагаются водой; гидриды элементов Са-Ва легко окисляются кислородом:
ЭН2 + 2Н2О ® Э(ОН)2 + 2Н2,
ЭН2 + O2 ® Э(OH)2
Галогениды. Все галогениды ЭГ2 - бесцветные кристаллические вещества с ионной решеткой. BeF2 существует также в виде стекловидной массы. ЭГ2 термически устойчивы, теплоты образования (абсолютные значения) у них высоки, закономерно повышаются в ряду Be-Ва (исключение - ВаF2) и уменьшаются при переходе от фторидов к иодидам. Температуры плавления изменяются, как правило, аналогично. В воде ЭГ2 хорошо растворяются (кроме фторидов ряда Mg-Ва), из водных растворов выделяются (кроме фторидов) в виде кристаллогидратов, большей частью с 6 или 2 молекулами воды.
Способы получения. СаГ2-ВаГ2 - действие НГ на металл, гидроксид или карбонат соответствующего металла:
Э + 2НГ ® ЭГ2 + H2
Э(OH)2 + 2НГ ® ЭГ2 + H2O (так же получают BeF2 и MgF2)
ЭCOH3 + 2НГ ® ЭГ2 + H2O + CO2 (так же получают и MgF2)
ВеГ2, кроме ВеF2 - нагревание Be с галогенами.
Mg Г2, кроме MgF2 - выделение из его природных соединений.
Химические свойства. Бромиды и иодиды проявляют восстановительные свойства:
ЭI2 + Cl2 ® ЭCl2 + I2
Галогениды Be и Mg сильно гидролизуются. При нагревании образуются оксосоли:
ЭГ2(р)+Н2O «ЭОНГ+НГ
2ЭГ2(р) + Н2О 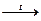 Э2ОГ2 + 2НГ (кроме MgF2),
Э2ОГ2 + 2НГ (кроме MgF2),
2BeCI2×4H2O 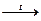 Be2OCI2 + 2HCl + 7H2O.
Be2OCI2 + 2HCl + 7H2O.
Соединения с кислородом. Оксиды ЭО и пероксиды ЭО2 (ВеО2 не получен) - порошкообразные вещества белого цвета. Температуры плавления ЭО очень высоки и понижаются от Mg к Ва. Термическая диссоциация ЭО протекает очень трудно, теплоты образования (абсолютные значения) высокие. Термическая устойчивость ЭО2 повышается от MgO2 к ВаО2. В воде ЭО2 труднорастворимы.
Способы получения. ЭО, кроме ВаО - термическое разложение карбонатов или гидроксидов щелочноземельных металлов:
Э(ОН)2 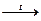 ЭО + Н2О (Э = Ве, Mg),
ЭО + Н2О (Э = Ве, Mg),
ЭСО3 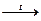 ЭО + СО2 (Э = Ве, Mg, Ca, Sr).
ЭО + СО2 (Э = Ве, Mg, Ca, Sr).
ВаО - по реакции:
2Ba(NO3)2 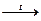 2BaO + 4NO2 + O2.
2BaO + 4NO2 + O2.
ЭО2, кроме ВаО2 - нейтрализация гидроксидов Н2О2:
Э(ОН)2 + Н2О2 «ЭО2 + 2Н2О
ВаО2 - по реакции:
2ВаО + О2  2ВаО2.
2ВаО2.
Химические свойства. Оксиды Mg, Ca, Sr, Ba - основного характера, ВеО проявляет амфотерные свойства. Химическая активность ЭО увеличивается в ряду ВеО - ВаО. Оксиды, кроме ВеО, реагируют с водой; MgO реагирует частично с горячей водой:
ЭО + Н2О ® Э(ОН)2
Оксиды легко реагируют с кислотами (ВеО при нагревании); ВеО реагирует также со щелочами:
ЭО+2НС1 ® ЭС12+Н2О,
ВеО + 2НС1 + 3Н2О 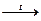 [Be (ОН2)4] С12
[Be (ОН2)4] С12
ВеО + 2КОН + Н2О 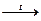 К2 [Be (OH)4]
К2 [Be (OH)4]
ВеО + 2КОН 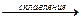 К2ВеО2+Н2О.
К2ВеО2+Н2О.
ВаО при нагревании в присутствии О2 образует ВаО2:
2ВаО + О2  2ВаО2.
2ВаО2.
ЭО2 при растворении в воде подвергаются сильному гидролизу:
ЭО2 + 2Н2О «Э(ОН)2 + Н2О2
Они разлагаются кислотами, даже очень слабыми, например угольной:
ЭО2 + СО2 + Н2О ® ЭСО3 + Н2О2.
Пероксиды благодаря наличию иона [O2]2- проявляют окислительные свойства; при действии сильных окислителей окисляются:
ВаО2 + 2KI + 2Н2О ® I2+ Ва (ОН)2 + 2KOH,
SrO2 + HgCl2 ® O2 + SrCl2 + Hg.
Пероксиды склонны к реакциям диспропорционирования:
2ВаО2 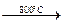 2ВаО + О2
2ВаО + О2
Соединения с другими элементами. Сульфиды ЭS - кристаллические бесцветные вещества с ионной решеткой типа NaCl; термически устойчивы; малорастворимы в воде. Получают ЭS взаимодействием простых веществ или прокаливанием сульфатов с углем:
BaSO4 + 4C 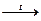 BaS + 4CO.
BaS + 4CO.
В водном растворе сульфиды сильно гидролизованы:
2ЭS + 2Н2О «Э(ОН)2 + Э(НS)2
В ряду BaS - BeS гидролиз усиливается, BeS и MgS гидролизуются полностью.
ЭS являются восстановителями:
BaS + I2 ® S + BaI2
Нитриды Э3N2- термически устойчивые кристаллические вещества. Получают их, как правило, нагреванием металлов в атмосфере N2:
3Э + N2 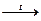 Э3N2
Э3N2
В воде нитриды необратимо гидролизуются:
Э3N2 + 2Н2О ® Э(ОН)2 + 2NH3
Гидроксиды и их производные
Гидроксиды Э(ОН)2 - белые порошкообразные вещества (кристаллическая решетка ионная). Они могут быть получены в безводном состоянии и в виде кристаллогидратов с 1, 2, 3, 8 молекулами воды. Растворимость в воде относительно невелика и увеличивается при переходе от Be(OH)2 к Ва(ОН)2.
При нагревания Э(ОН)2 разлагаются, переходя в оксиды:
Э(ОН)2 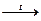 ЭО + H2O
ЭО + H2O
Способы получения. Ве(ОН)2, Mg(OH)2 - обменные реакции между растворимой солью металла и щелочью:
ЭCl2 + 2KOH ® Э(ОН)2 + 2КС1.
В случае Ве(ОН)2 следует избегать избытка щелочи.
Са(ОН)2, Sr(OH)2, Ba(OH)2 - взаимодействие оксидов с водой:
ЭО + H2O ® Э(ОН)2
Химические свойства. Характер диссоциации Э(ОН)2 закономерно изменяется от Ве(ОН)2 (амфотер) до Ва(ОН)2 (сильное основание). Ве(ОН)2, растворяясь в кислотах и щелочах, образует аква- и гидроксокомплексы:
Be (ОН)2 + 2НС1 + 2Н2О ® [Ве (ОН2)4]С12
Be (ОН)2 + 2NaOH ® Na2 [Be (ОН)4]
Mg(OH)2 проявляет только основные свойства, слабый электролит.
При нагревании сульфаты, нитраты, карбонаты разлагаются по схемам:
2ЭSО4 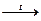 2ЭО + 2SО2 + О2
2ЭО + 2SО2 + О2
2Э(NO3)2 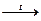 2ЭО + 4NО2 + О2
2ЭО + 4NО2 + О2
ЭCО3 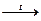 2ЭО + CО2
2ЭО + CО2
Термическая устойчивость нитратов и карбонатов закономерно возрастает от соединений Be к соединениям Ва.
При действии СО2 на осадки карбонатов Са, Sr, Ва образуются растворимые гидрокарбонаты, которые при нагревании опять переходят в карбонаты:
ЭСОз + СО2 + Н2О «Э(НСО3)2
В водном растворе соли Be и Mg, а также соли слабых кислот Са, Sr, Ва гидролизуются; соли Be и Mg гидролизуются особенно легко с образованием основных солей.
|
|
Дата добавления: 2015-07-13; Просмотров: 1063; Нарушение авторских прав?; Мы поможем в написании вашей работы!