
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
I.2.Флавиновые дегидрогеназы
|
|
|
|
Флавиновые ферменты представляют собой сложные белки, простетическими группами которых являются флавинмононуклеотид (ФМН) или флавинадениндинуклеотид (ФАД), которые являются производными рибофлавина – витамина B2. Они содержит общую циклическую (состоящую из 3-х циклов) изоаллоксазиновую группировку, которая способна обратимо восстанавливаться по реакции:




 + 2H+ + 2e
+ 2H+ + 2e
|
|
Биологически активными являются 6,7-диметилпроизводные изоаллоксазина, к которым относится и рибофлавин, кроме того содержащий остаток 5-ти атомного спирта - ребитола

 |
|
ФМН представляет собой рибофлавинз51-фосфат, а ФАД, кроме того, содержит остаток адениловой кислоты (нуклеотида АМФ)
 | |||
 |

|
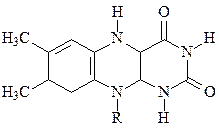
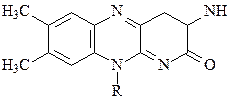
 + SH2 + S
+ SH2 + S
Рибофлавин не синтезируется в организме человека и обязательно должен поступать с пищей.
Коферменты ФМН и ФАД являются простетическими группами и прочно связаны с ферментами. Их называют флавопротеинами.
В ходе реакции дегидрогенизации с участием ФМН и ФАД отщепляемые от субстрата атомы водорода присоединяются к изоаллоксазиновой группировке кофермента (к к атомам азота второго и третьего циклов по схеме:
|
 О
О
C COOH
 |  |
 CH2 + ФАД CH + ФАД-H2
CH2 + ФАД CH + ФАД-H2
 | |||||
 |  | ||||
|
|
|
|
 | |||||||
 | |||||||
 | |||||||
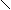 |
|
C COOH
|
|
I.3. Кофермент Q– убихинон.
Этот кофермент обычно входит в состав дегидрогеназ, которые окисляют восстановленные коферменты НАД∙Н и ФМН∙Н2.
Это необходимо для того, чтобы регенерировать их для выполнения ими своих окислительных функций.
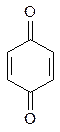
Убихинон содержит в своем составе хиноновый цикл
 |
Система двойных связей и (две С=С в цикле и две С=О в карбонильных группах) называется хиноидной группировкой. Хиноновый цикл способен к реакциям окисления-восстановления, протекающим по схеме:

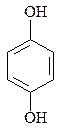
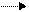
 + 2H+ + 2e
+ 2H+ + 2e
|
|
Убихинон, принимающий участие в клеточном дыхании, имеет следующую формулу:
|
|

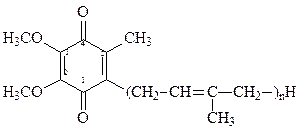
|
Он представляет собой 2,3-диметокси-5-метилхинон, к которому в положении 6 присоединяется фрагмент, содержащий до 10 структурных звеньев изопрена – мономера природного каучука:
 nCH2=C-CH=CH2 [-CH2-C=CH-CH2-]n
nCH2=C-CH=CH2 [-CH2-C=CH-CH2-]n
 | |||
 | |||
|
Присоединяя водород, убихинон превращается в убихинол
Всю систему регенерации дегидрогеназ с участием убихинона, можно представить следующей последовательностью реакций:
 НАД∙Н + Н+ + ФМН ФМН∙Н2 + НАД+
НАД∙Н + Н+ + ФМН ФМН∙Н2 + НАД+
ФМН∙Н2 + Q → ФМН + Q ∙H2
I.4. Группа гемма
Эта группа является окислительно-восстановительным кофактором ферментов дыхательной цепи, фотосинтеза и др.

 Гем представляет собой простетическую группу. Он представляет собой порфириновый цикл, состоящий из 4-х пирольных колец, связанных группами СН, который в свою очередь связан ковалентными связями с белком. Ион Fe3+, входящий в порфириновый цикл, способен восстанавливаться до иона Fe2+ и тем самым осуществлять перенос заряда, который является одним из важнейших процессов в живых клетках Электроны, переходят от одного вещества к другому иногда непосредственно, а иногда по цепи специальных переносчиков заряда. Принцип переноса заряда как раз и заключается в том, что ионы переходных металлов (Fe+2, Cu+2) в составе гема способны существовать в различных степенях окисления и принимать или отдавать электрны.
Гем представляет собой простетическую группу. Он представляет собой порфириновый цикл, состоящий из 4-х пирольных колец, связанных группами СН, который в свою очередь связан ковалентными связями с белком. Ион Fe3+, входящий в порфириновый цикл, способен восстанавливаться до иона Fe2+ и тем самым осуществлять перенос заряда, который является одним из важнейших процессов в живых клетках Электроны, переходят от одного вещества к другому иногда непосредственно, а иногда по цепи специальных переносчиков заряда. Принцип переноса заряда как раз и заключается в том, что ионы переходных металлов (Fe+2, Cu+2) в составе гема способны существовать в различных степенях окисления и принимать или отдавать электрны.
|
|
|
II. Коферменты переноса групп (трансферазы)
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 3612; Нарушение авторских прав?; Мы поможем в написании вашей работы!