
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методы систематического хода анализа катионов. 8 страница
|
|
|
|
Нитритометрическое определение стрептоцида основано на реакции диазотирования:

 NH2 N ≡N+
NH2 N ≡N+

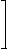 + NaNO2 + НС1 ↔ Сl - + NaC1+ 2Н2О
+ NaNO2 + НС1 ↔ Сl - + NaC1+ 2Н2О
SO2NH2 SO2NH2
Поскольку взаимодействие стрептоцида с NaNО2 проходит в соотношении 1:1, то f (стрептоцида) = 1, f (NaNО2) = 1.
При выполнении реакций диазотирования необходимо соблюдать следующие условия титрования:
1. Титрование обычно выполняют на холоде (так как соли диазония разлагаются при повышенной температуре).
2. Титрование выполняют в присутствии двойного количества хлороводородной кислоты (для предотвращения протекания реакции в другом направлении).
3. Реакция диазотирования протекает медленно, поэтому для ее ускорения используют катализатор KBr.
4. При титровании желательно применять внутренние индикаторы или фиксировать конечную точку титрования потенциомет-рически.
Аналитическая химия - лекция №13
ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ АНАЛИЗА. КЛАССИФИКАЦИЯ МЕТОДОВ. ОПТИЧЕСКИЕ МЕТОДЫ АНАЛИЗА. МОЛЕКУЛЯРНО-АБСОРБЦИОННАЯ СПЕКТРОСКОПИЯ.
Физико-химические или инструментальные методы анализа основаны на измерении с помощью приборов (инструментов) физических параметров анализируемой системы, которые возникают или изменяются в ходе выполнения аналитической реакции.
Бурное развитие физико-химических методов анализа было вызвано тем, что классические методы химического анализа (гравиметрия, титриметрия) уже не могли удовлетворять многочисленные запросы химической, фармацевтической, металлургической, полупроводниковой, атомной и других отраслей промышленности, требовавших повышения чувствительности методов до 10-8 – 10-9 %, их селективности и экспрессности, что позволило бы управлять технологическими процессами по данным химического анализа, а также выполнять их в автоматическом режиме и дистанционно.
|
|
|
Ряд современных физико-химических методов анализа позволяют одновременно в одной и той же пробе выполнять как качественный, так и количественный анализ компонентов. Точность анализа современных физико-химических методов сопоставима с точностью классических методов, а в некоторых, например в кулонометрии, она существенно выше.
К недостаткам некоторых физико-химических методов следует отнести дороговизну используемых приборов, необходимость применения эталонов. Поэтому классические методы анализа по-прежнему не потеряли своего значения и применяются там, где нет ограничений в скорости выполнения анализа и требуется высокая его точность при высоком содержании анализируемого компонента.
КЛАССИФИКАЦИЯ ФИЗИКО - ХИМИЧЕСКИХ
МЕТОДОВ АНАЛИЗА
В основу классификации физико-химических методов анализа положена природа измеряемого физического параметра анализируемой системы, величина которого является функцией количества вещества. В соответствии с этим все физико-химические методы делятся на три большие группы:
- электрохимические;
- оптические и спектральные;
- хроматографические.
Электрохимические методы анализа основаны на измерении электрических параметров: силы тока, напряжения, равновесных электродных потенциалов, электрической проводимости, количе-ства электричества, величины которых пропорциональны содержанию вещества в анализируемом объекте.
Оптические и спектральные методы анализа основаны на измерении параметров, характеризующих эффекты взаимодействия электромагнитного излучения с веществами: интенсивности излучения возбужденных атомов, поглощения монохроматического излучения, показателя преломления света, угла вращения плоскости поляризованного луча света и др.
|
|
|
Все эти параметры являются функцией концентрации вещества в анализируемом объекте.
Хроматографические методы - это методы разделения однородных многокомпонентных смесей на отдельные компоненты сорбционными методами в динамических условиях. В этих условиях компоненты распределяются между двумя несмешивающимися фазами: подвижной и неподвижной. Распределение компонентов основано на различии их коэффициентов распределения между подвижной и неподвижной фазами, что при- водит к различным скоростям переноса этих компонентов из неподвижной в подвижную фазу. После разделения количественное содержание каждого из компонентов может быть определено различными методами анализа: классическими или инструментальными.
МОЛЕКУЛЯРНО-АБСОРБЦИОННЫЙ
СПЕКТРАЛЬНЫЙ АНАЛИЗ
Молекулярно-абсорбционный спектральный анализ включает в себя спектрофотометрический и фотоколориметрический виды анализа.
Спектрофотометрический анализ основан на определении спектра поглощения или измерении светопоглощения при строго определенной длине волны, которая соответствует максимуму кривой поглощения исследуемого вещества.
Фотоколориметрический анализ базируется на сравнении интенсивности окрасок исследуемого окрашенного и стандартного окрашенного растворов определенной концентрации.
Молекулы вещества обладают определенной внутренней энергией Е, составными частями которой являются:
- энергия движения электронов Еэл находящихся в электростати-ческом поле атомных ядер;
- энергия колебания ядер атомов друг относительно друга Екол;
- энергия вращения молекулы Евр
и математически выражается как сумма всех указанных выше энергий:
Е = Еэл + Екол + Евр.
При этом, если молекула вещества поглощает излучение, то ее первоначальная энергия Е0 повышается на величину энергии поглощенного фотона, то есть:
ЕΔ = Е1 – Е0 = hν = hC / λ.
Из приведенного равенства следует, что чем меньше длина волны λ, тем больше частота колебаний и, следовательно, больше Е, то есть энергия, сообщенная молекуле вещества при взаимодействии с электромагнитным излучением. Поэтому характер взаимодействия лучевой энергии с веществом в зависимости от длины волны света λ будет различен.
|
|
|
Совокупность всех частот (длин волн) электромагнитного излучения называют электромагнитным спектром. Интервал длин волн разбивают на области:
ультрафиолетовая (УФ) примерно 10-380 нм, видимая 380-750 нм, инфракрасная (ИК) 750-100000 нм.
Области электромагнитного спектра
γ-излучение рентген вакуум УФ ближн. УФ видимая
______________ │_______│_______________│______│_
λ(нм) …… 10 100 380 750
ближн. ИК далекая ИК радиоволны
λ(нм) 1000 10000 100000 ….
Энергии, которую сообщают молекуле вещества излучения УФ- и видимой части спектра, достаточно, чтобы вызвать изменение электронного состояния молекулы.
Энергия ИК-лучей меньше, поэтому ее оказывается достаточно только для того, чтобы вызвать изменение энергии колебательных и вращательных переходов в молекуле вещества. Таким образом, в различных частях спектра можно получить различную информацию о состоянии, свойствах и строении веществ.
ЗАКОНЫ ПОГЛОЩЕНИЯ ИЗЛУЧЕНИЯ
В основе спектрофотометрических методов анализа лежат два основных закона. Первый из них - закон Бугера – Ламберта, второй закон - закон Бера. Объединенный закон Бугера - Ламберта – Бера имеет следующую формулировку:
Поглощение монохроматического света окрашенным раствором прямо пропорционально концентрации поглощающего свет вещества и толщине слоя раствора, через который он проходит.
Закон Бугера - Ламберта - Бера является основным законом светопоглощения и лежит в основе большинства фотометрических методов анализа. Математически он выражается уравнением:
I =Ι0 · 10-КСl
Или lg I /Ι0 = К · C · l
Величину lg I /Ι0 называют оптuческой плотностью поглощающего вещества и обозначают буквами D или А. Тогда закон можно записать так: D = К · C · l
Отношение интенсивности потока монохроматического излучения, прошедшего через испытуемый объект, к интенсивности первоначального потока излучения называется
nрозрачностью, или nроnусканием, раствора и обозначается буквой Т:
Т = I / Ι0
Это соотношение может быть выражено в процентах. Величина Т, характеризующая пропускание слоя толщиной 1 см, называется коэффициентом nропускания. Оптическая плотность D и пропус-кание Т связаны между собой соотношением
|
|
|
D = -lg Т
или, если Т выражено в процентах,
D = 2 - 1gТ.
D и Т являются основными величинами, характеризующими поглощение раствора данного вещества с определенной его концентрацией при определенной длине волны и толщине поглощающего слоя.
Зависимость D(С) имеет прямолинейный характер, а Т(С) или Т(l) - экспоненциальный. Это строго соблюдается только для монохроматических потоков излучений.
Величина коэффициента погашения К зависит от способа выражения концентрации вещества в растворе и толщины поглощающего слоя. Если концентрация выражена в молях на литр, а толщина слоя - в сантиметрах, то он называется молярным коэффициентом погашения, обозначается символом ε и равен оптической плотности раствора с концентрацией 1 моль/л, помещенного в кювету с толщиной слоя 1 см.
Величина молярного коэффициента светопоглощения зависит:
- от природы растворенного вещества;
- длины волны монохроматического света;
- температуры;
- природы растворителя.
Причины несоблюдения закона Бyгера - Ламберта - Бера.
1. Закон выведен и справедлив только для монохроматического света, поэтому недостаточная монохроматизация может вызвать отклонение закона и тем в большей степени, чем меньше монохроматизация света.
2. В растворах могут протекать различные процессы, которые изменяяют концентрацию поглощающего вещества или его природу: гидролиз, ионизация, гидратация, ассоциация, полимеризация, комплексообразование и др.
3. Светопоглощение растворов существенно зависит от рН раствора. При изменении рН раствора могут изменяться:
- степень ионизации слабого электролита;
- форма существования ионов, что приводит к изменению светопоглощения;
- состав образующихся окрашенных комплексных соединений.
Поэтому закон справедлив для сильно разбавленных растворов, и область его применения ограничена.
ВИЗУАЛЬНАЯ КОЛОРИМЕТРИЯ
Интенсивность окраски растворов можно измерять различными методами. Среди них выделяют субъективные (визуальные) методы колориметрии и объективные, то есть фотоколориметрические.
Визуальными называют такие методы, при которых оценку интенсивности окраски испытуемого раствора делают невооруженным глазом. При объективных методах колориметрического определения для измерения интенсивности окраски испытуемого раствора вместо непосредственного наблюдения пользуются фотоэлементами. Определение в этом случае проводят в специальных приборах - фотоколориметрах, поэтому метод получил название фотоколориметрического.
Цвета видимого излучения:
Интервал длин Основной цвет
волн, нм
340-450 фиолетовый
450-495 синий
495-570 зеленый
570-590 желтый
590-620 оранжевый
620-750 красный
К визуальным методам относятся:
- метод стандартных серий;
- метод колориметрического титрования, или дублирования;
- метод уравнивания.
Метод стандартных серий. При выполнении анализа методом стандартных серий интенсивность окраски анализируемого окра-шенного раствора сравнивают с окрасками серии специально при-готовленных стандартных растворов (при одинаковой толщине слоя).
Метод колориметрического титрования (дублирования) основан на сравнении окраски анализируемого раствора с окраской другого раствора - контрольного. Контрольный раствор содержит все компоненты исследуемого раствора, за исключением определяемого вещества, и все использовавшиеся при подготовке пробы реактивы. К нему добавляют из бюретки стандартный раствор определяемого вещества. Когда этого раствора будет добавлено столько, что интенсивности окраски контрольного и анализируемого растворов уравняются, считают, что в анализируемом растворе содержится столько же определяемого вещества, сколько его было введено в контрольный раствор.
Метод уравнивания отличается от описанных выше визуальных колориметрических методов, в которых подобие окрасок стандартного и испытуемого растворов достигается изменением их концентрации. В методе уравнивания подобие окрасок достигается изменением толщины слоев окрашенных растворов. Для этой цели при определении концентрации веществ используют колориметры сливания и погружения.
Достоинства визуальных методов колориметрического анализа:
- техника определения проста, нет необходимости в сложном дорогостоящем оборудовании;
- глаз наблюдателя может оценивать не только интенсивность, но и оттенки окраски растворов.
Недостатки: - необходимо готовить стандартный раствор или серии стандартных растворов;
- невозможно сравнивать интенсивность окраски раствора в присутствии других окрашенных веществ;
- при длительном сравнивании интенсивности окраски глаз человека утомляется, и ошибка определения увеличивается;
- глаз человека не столь чувствителен к небольшим изменениям оптической плотности, как фотоэлектрические устройства, вследствие этого невозможно обнаружить разницу в концентрации примерно до пяти относительных процентов.
ФОТОЭЛЕКТРОКОЛОРИМЕТРИЧЕСКИЕ МЕТОДЫ
Фотоэлектроколориметрия применяется для измерения поглощения света или пропускания окрашенными растворами. Приборы, используемые для этой цели, называются фотоэлектроколориметрами (ФЭК).
Фотоэлектрические методы измерения интенсивности окраски связаны с использованием фотоэлементов. В отличие от приборов, в которых сравнение окрасок производится визуально, в фотоэлектроколориметрах приемником световой энергии является прибор – фотоэлемент. В этом приборе световая энергия преобразует в электрическую. Фотоэлементы позволяют проводить колориметрические определения не только в видимой, но также в УФ- и ИК-областях спектра. Измерение световых потоков с помощью фотоэлектрических фотометров более точно и не зависит от особенностей глаза наблюдателя. Применение фотоэлементов позволяет автоматизировать определение концентрации веществ в химическом контроле технологических процессов. Вследствие этого фотоэлектрическая колориметрия значительно шире используется в практике заводских лабораторий, чем визуальная.
На рис. 1 показан обычный порядок расположения узлов в приборах для измерения пропускания или поглощения растворов.
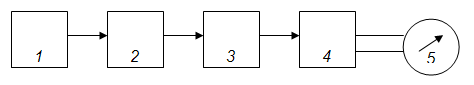
Рис.1 Основные узлы приборов для измерения поглощения излучения: 1 - источник излучения; 2 - монохроматор; 3 - кюветы для растворов; 4 - преобразователь; 5 - индикатор сигнала.
Фотоколориметры в зависимости от числа используемых при измерениях фотоэлементов делятся на две группы: однолучевые (одноплечие) - приборы с одним фотоэлементом и двухлучевые (двуплечие) - с двумя фотоэлементами.
Точность измерений, получаемая на однолучевых ФЭК, невелика. В заводских и научных лабораториях наиболее широкое распространение получил фотоэлектрические установки, снабженные двумя фотоэлементами. В основу конструкции этих приборов положен принцип уравнивания интенсивности двух световых пучков при помощи переменной щелевой диафрагмы, то есть принцип оптической компенсации двух световых потоков путем изменений раскрытия зрачка диафрагмы.
Принципиальная схема прибора представлена на рис. 2. Свет от лампы накаливания 1 с помощью зеркал 2 разделяется на два параллельных пучка. Эти световые пучки проходят через светофильтры 3, кюветы с растворами 4 и попадают на фотоэлементы 6 и 6', которые включены на гальванометр 8 по дифференциaльнoй схеме. Щелевая диафрагма 5 изменяет интенсивность светового потока, падающего на фотоэлемент 6. Фотометрический нейтральный клин 7 служит для ослабления светового потока, падающего на фотоэлемент 6'.
Рис.2. Схема двухлучевого фотоэлектроколориметра
ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ В ФОТОЭЛЕКТРОКОЛОРИМЕТРИИ
Для определения концентрации анализируемых веществ в фотоэлектроколориметрии применяют:
- метод сравнения оптических плотностей стандартного и исследуемого окрашенных растворов;
- метод определения по среднему значению молярного коэффициента светопоглощения;
- метод градуировочного графика;
- метод добавок.
Метод сравнения оптических плотностей стандартного и исследуемого окрашенных растворов. Для определения готовят эталонный раствор определяемогo вещества известной концен-трации, которая приближается к концентрацииисследуемого рас-твора. Определяют оптическую плотность этого раствора при
определенной длине волны Dэт. Затем определяют оптическую плотность исследуемого раствора Dх при той же длине волны и при той же толщине слоя. Сравнивая значения оптических плотностей исследуемого и эталонного растворов, находят неизвестную концентрацию определяемого вещества.
Метод сравнения применим при однократных анализах и требует обязательного соблюдения основного закона светопоглощения.
Метод градуировочноro графика. Для определения концентрации вещества этим методом готовят серию из 5-8 стан-дартных растворов различной концентрации. При выборе интервала концентраций стандартных растворов руководствуются следующими положениями:
Ø он должен охватывать область возможных измерений концентрации исследуемого раствора;
Ø оптическая плотность исследуемого раствора должна соответствовать примерно середине градуировочной кривой;
Ø желательно, чтобы в этом интервале концентраций соблюдался основной закон светопоглощения, то есть график зависимости был прямолинейным;
Ø величина оптической плотности должна находиться в пределах 0, 14… 1,3.
Измеряют оптическую плотность стандартных растворов и строят график зависимости D(С). Определив Dх исследуемого раствора, по градуировочному графику находят Сх (рис. 3).
Этот метод позволяет определить концентрацию вещества даже в тех случаях, когда основной закон светопоглощения не соблюдается. В таком случае готовят большое количество стандартных растворов, отличающихся по концентрации не более чем на 10 %.

Рис. 3. Зависимость оптической плотности раствора от концентрации (калибровочная кривая)
Метод добавок - это разновидность метода сравнения, осно-ванный на сравнении оптической плотности исследуемого раствора и того же раствора с добавкой известно количества определяемого вещества.
Применяют его для устранения мешающего влияния посто-ронних примесей, определения малых количеств анализируемого вещества в присутствии больших количеств посторонних веществ. Метод требует обязательного соблюдения основного закона свето-поглощения.
СПЕКТРОФОТОМЕТРИЯ
Это метод фотометрического анализа, в котором определение содержания вещества производят по поглощению им монохроматического света в видимой, УФ- и ИК-областях спектра. В спектрофотометрии, в отличие от фотометрии, монохроматизация обеспечивается не светофильтрами, а монохроматорами, позволяющими непрерывно изменять длину волны. В качестве монохроматоров используют призмы или дифракционные решетки, которые обеспечивают значительно более высокую монохроматичность света, чем светофильтры, поэтому точность спектрофотометрических определений выше.
Спектрофотометрические методы, по сравнению с фотоколориметрическими, позволяют решать более широкий круг задач:
Ø проводить количественное определение веществ в широком интервал длин волн (185-1100 нм);
Ø осуществлять количественный анализ многокомпонентных систем (одновременное определение нескольких веществ);
Ø определять состав и константы устойчивости светопоглощающих комплексных соединений;
Ø определять фотометрические характеристики светопоглощающих соединений.
В отличие от фотометров монохроматором в спектрофо-тометрах служит призма или дифракционная решетка, позволяя-ющая непрерывно менять длину волны. Существуют приборы для измерений в видимой, УФ- и ИК-областях спектра. Принципи-альная схема спектрофотометра практически не зависит от спектральной области.
Спектрофотометры, как и фотометры, бывают одно- и двулучевые. В двулучевых приборах световой поток каким-либо способом раздваивают или внутри монохроматора, или по выходе из него: один поток затем проходит через испытуемый раствор, другой - через растворитель.
Однолучевые приборы особенно удобны при выполнении количественных определений, основанных на измерении оптической плотности при одной длине волны. В этом случае простота прибора и легкость эксплуатации представляют существенное преимущество. Большая скорость и удобство измерения при работе с двулучевыми приборами полезны в качественном анализе, когда для получения спектра оптическая плотность должна быть измерена в большом интервале длин волн. Кроме того, двулучевое устройство легко приспособить для автоматической записи непрерывно меняющейся оптической плотности: во всех современных регистрирующих спектрофото-метрах для этой цели используют именно двулучевую систему.
И одно-, и двулучевые приборы пригодны для измерений видимого и УФ-излучений. В основе ИК-спектрофотометров, выпускаемых промышленностью, всегда лежит двулучевая схема, поскольку их обычно используют для развертки и записи большой области спектра.
Количественный анализ однокомпонентных систем проводится теми же методами, что и в фотоэлектроколориметрии:
- методом сравнения оптических плотностей стандартного и исследуемого растворов;
- методом определения по среднему значению молярного коэффициента светопоглощения;
- методом градуировочного графика,
и не имеет никаких отличительных особенностей.
СПЕКТРОФОТОМЕТРИЯ В КАЧЕСТВЕННОМ АНАЛИЗЕ
Качественный анализ в ультрафиолетовой части спектра. Ультрафиолетовые спектры поглощения обычно имеют две-три, иногда пять и более полос поглощения. Для однозначной идентификации исследуемого вещества записывают его спектр поглощения в различных растворителях и сравнивают полученные данные с соответствующими спектрами сходных веществ известного состава. Если спектры поглощения исследуемого вещества в разных paстворителях совпадают со спектром известного вещества, то можно с большой долей вероятности сделать заключение об идентичности химического состава этих соединений. Для идентификации неизвестного вещества по его спектру поглощения необходимо располагать достаточным количеством спектров поглощения органических и неорганических веществ. Существуют атласы, в которых приведены спектры поглощения очень многих, в основном органических веществ. Особенно хорошо изучены ультрафиолетовые спектры аромати-ческих углеводородов.
При идентификации неизвестных соединений следует также обратить внимание на интенсивность поглощения. Очень многие органические соединения обладают полосами поглощения, максимумы которых расположены при одинаковой длине волны λ, но интенсивность их различна. Например, в спектре фенола наблюдается полоса поглощения при λ = 255 нм, для которой молярный коэффициент поглощения при максимуме поглощения εmах = 1450. При той же длине волны ацетон имеет полосу, для которой εmах = 17.
Качественный анализ в видимой части спектра. Идентификацию окрашенного вещества, например красителя, также можно проводить, сравнивая его спектр поглощения в видимой части со спектром сходного красителя. Спектры поглощения большинства красителей описаны в специальных атласах и руководствах. По спектру поглощения красителя можно сделать заключение о чистоте красителя, потому что в спектре примесей имеется ряд полос поглощения, которые отсутствуют в спектре красителя. По спектру поглощения смеси красителей можно также сделать заключение о составе смеси, особенно если в спектрах компонентов смеси имеются полосы поглощения, расположенные в разных областях спектра.
Качественный анализ в инфракрасной области спектра.
Поглощение ИК-излучения связано с увеличением колебательной и вращательной энергий ковалентной связи, если оно приводит к изменению дипольного момента молекулы. Это значит, что почти все молекулы с ковалентными связями в той или иной мере способны к поглощению в ИК-области.
Инфракрасные спектры многоатомных ковалентных соединений обычно очень сложны: они состоят из множества узких полос поглощения и сильно отличаются от обычных УФ- и видимых спектров. Различия вытекают из природы взаимодействия поглощающих молекул и их окружения. Это взаимодействие (в конденсированных фазах) влияет на электронные переходы в хромофоре, поэтому линии поглощения уширяются и стремятся слиться в широкие полосы поглощения. В ИК -спектре, наоборот, частота и коэффициент поглощения, соответствующие отдельной связи, обычно мало меняются с изменением окружения (в том числе с изменением остальных частей молекулы). Линии тоже расширяются, но не настолько, чтобы слиться в полосу.
Обычно по оси ординат при построении ИК-спектров откладывают пропускание в процентах, а не оптическую плотность. При таком способе построения полосы поглощения выглядят как впадины на кривой, а не как максимумы на УФ-спектрах.
Образование инфракрасных спектров связано с энергией колебаний молекул. Колебания могут быть направлены вдоль валентной связи между атомами молекулы, в таком случае они называются валентными. Различают симметричные валентные колебания, в которых атомы колеблются в одинаковых направлениях, и асиммeтpичныe валентные колебания, в которых атомы колеблются в противоположных направлениях. Если колебания атомов происходят с изменением угла между связями, они называются деформационными. Такое разделение весьма условно, потому что при валентных колебаниях происходит в той или иной степени деформация углов и наоборот. Энергия деформационных колебаний обычно меньше, чем энергия валентных колебаний, и полосы поглощения, обусловленные деформационными колебаниями, располагаются в области более длинных волн.
Колебания всех атомов молекулы обусловливают полосы поглощения, индивидуальные для молекул данного вещества. Но среди этих колебаний можно выделить колебания групп атомов, которые слабо связаны с колебаниями атомов остальной части молекулы. Полосы поглощения, обусловленные такими колебаниями, называют характеристическими полосами. Они наблюдаются, как правило, в спектрах всех молекул, в которых имеются данные группы атомов. Примером характеристических полос могут служить полосы 2960 и 2870 см-1. Первая полоса обусловлена асимметричными валентными колебаниями связи С-Н в метильной группе СН3, а вторая - симметричными валентными колебаниями связи С-Н этой же группы. Такие полосы с небольшим отклонением (±10 см-1) наблюдаются в спектрах всех насыщенных углеводородов и вообще в спектре всех молекул, в которых имеются СН3- группы.
Другие функциональные группы могут влиять на положение характеристической полосы, причем разность частот может составлять до ±100 см-1, но такие случаи немногочисленны, и их можно учитывать на основании литературных данных.
Качественный анализ в инфракрасной области спектра проводится двумя способами.
1. Снимают спектр неизвестного вещества в области 5000-500 см-1 (2 - 20 мк) и отыскивают сходный спектр в специальных каталогах или таблицах. (или при помощи компьютерных баз данных)
2. В спектре исследуемого вещества отыскивают характерис-тические полосы, по которым можно судить о составе вещества.
ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА, ИХ КЛАССИФИКАЦИЯ. ПОТЕНЦИОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА. КУЛОНОМЕТРИЯ.
В соответствии с рекомендациями ИЮПАК все электрохимические методы анализа подразделяются на две большие группы:
- методы без протекания электрохимических реакций на электродах электрохимической ячейки (кондуктометрия с использованием токов низких 50-10000 Гц и высоких частот более 1 МГЦ);
- методы с протеканием электрохимических реакций на электродах электрохимической ячейки. К ним относятся потенциометрия, кулонометрия, полярография и другие методы анализа.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1022; Нарушение авторских прав?; Мы поможем в написании вашей работы!