
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основность аминов
|
|
|
|
Основание – электро-донорный реагент, который обладает сродством к протону.
Из этого определения следует, что, взаимодействуя с кислотами, амины образуют соли. Так газообразный метиламин (СH3NH2) при взаимодействии с соляной кислотой (HC l) образует твердую соль – хлоридметил аммония.
Метиламин можно получить в виде основания. (CH3)3N+ образует соль (CH3)3NBr (бромистый триметил аммония). А анилин образует C6H5NH3I.
Алифатические амины в водных растворах являются более сильными основаниями, чем NH3 (аммиак). Причина этого заключается в том, что алкильные группы являются донорами электронов, что приводит к частичной делокализации по отношению к атому углерода.
Во вторичных и третичных аминах в делокализации участвуют 2 и 3 атома углерода, поэтому основность увеличивается к третичным аминам.


 первичный C2H5NH2
первичный C2H5NH2
C2H5
|
вторичный CH3 – CH2 – CH2 – NH
третичный CH3 – CH2 – N – C2H5
|
CH3
Также амины способны к образованию водородных связей.
 H
H

 Н ••• O
Н ••• O
H
 R – N
R – N
 H
H
 H ••• O
H ••• O
H
Комбинация этих двух факторов приводит к тому, что по основности амины распределяются так:
вторичные > первичные > третичные > NH3
Ароматические амины более слабые основания, чем алифатические.
NH2 ••
| и C2H5 N H2
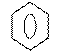
В этом случае неподеленная пара электронов атома азота частично делокализована по ароматическому кольцу. В результате чего происходит сопряжение с электронами бензольного кольца. Поэтому эта пара электронов менее доступна для координации с протоном.
Электро-донордные группы ОН ¯ усиливают основность. А электро-акцепторные группы NO2¯, C l ¯ уменьшают.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 429; Нарушение авторских прав?; Мы поможем в написании вашей работы!