
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение состояния идеального газа. Тема: Молекулярно-кинетическая теорияидеальных газов
|
|
|
|
Лекция №5
Тема: Молекулярно-кинетическая теорияидеальных газов. Основные положения молекулярно-кинетической теории. Уравнение состояния идеального газа. Основное уравнение идеального газа и следствие из него. Кинетическая энергия молекулы. Скорость газовых молекул. Термодинамическая шкала температур (шкала Кельвина).
Молекулярно-кинетической теорией называется учение, объясняющее свойства тел взаимодействием и движением молекул. Основные ее положения таковы: 1. Все тела состоят из мельчайших частиц – атомов и молекул. 2. Между атомами и молекулами существуют силы взаимодействия, которые обнаруживаются на расстояниях, сравнимых с размерами молекул. Взаимодействие существенно зависит от типа молекул и расстояний между ними. 3. Атомы и молекулы находятся в состоянии непрерывного хаотического движения.
Данный раздел физики базируется на теории вероятностей. Теория вероятностей представляет собой раздел математики, в котором изучаются закономерности массовых явлений, носящих случайный характер.
Рассмотрим газообразное состояние вещества, которое характеризуется четырьмя величинами: массой – m, объемом – V, давлением – Р и температурой Т. Все эти величины в газообразном состоянии вещества зависят друг от друга и при изменении одной из них, вообще говоря, меняются все остальные. Простейшими свойствами обладает газ, взаимодействие между молекулами которого пренебрежимо мало. Такой газ называется идеальным. Всякий реальный газ при достаточном разрежении близок по своим свойствам к идеальному. Некоторые газы, такие, как воздух, азот, кислород, даже при обычных условиях, т. е. при комнатной температуре и атмосферном давлении, мало отличаются от идеального газа. Формула, закономерно связывающая характеристики газообразного состояния вещества, называется уравнением состояния идеального газа или уравнением Менделеева – Клапейрона и записывается:
|
|
|
PV = 
где R – универсальная газовая постоянная(R = 8,31  ;
;  – масса моля. Моль – единица измерения количества вещества в системе СИ. Моль – количество вещества, масса которого в граммах равна его относительной молекулярной массе. В моле любого вещества содержится одинаковое число молекул N А = 6,02 1023
– масса моля. Моль – единица измерения количества вещества в системе СИ. Моль – количество вещества, масса которого в граммах равна его относительной молекулярной массе. В моле любого вещества содержится одинаковое число молекул N А = 6,02 1023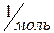 (число Авагадра).
(число Авагадра).
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 242; Нарушение авторских прав?; Мы поможем в написании вашей работы!