
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет изменения энтропии в различных процессах
|
|
|
|
Только с развитием статистической термодинамики удалось выяснить, что стоит за энтропией. В 1896 г. Больцман показал, что смысл энтропии носит статистический (вероятностный) характер.
Энтропия и термодинамическая вероятность системы.
S = k×lnW, (10)
где k – коэффициент пропорциональности, называемый постоянной Больцмана или константой Больцмана
(k =  = 8,314
= 8,314  / 6,02×1023 моль–1»» 1,38×10–23
/ 6,02×1023 моль–1»» 1,38×10–23 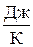 ),
),
W – термодинамическая вероятность данного состояния системы.
Чем больше неупорядоченность системы, тем система более вероятна, и тем ее энтропия больше. Иными словами, можно сказать, что энтропия – это мера хаоса.
Второй закон термодинамики имеет ограниченный (статистический) характер, поскольку он применим к системам, состоящим из большого числа частиц. При этом возможны различные отклонения от второго закона (флуктуации), которые в отдельные моменты времени тем более вероятны, чем меньше частиц содержится в системе (или в отдельном элементе объема системы).
Второй закон термодинамики в виде 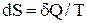 , записанный для равновесных процессов, позволяет вычислить не абсолютное значение энтропии, а только разность энтропий в двух состояниях системы.
, записанный для равновесных процессов, позволяет вычислить не абсолютное значение энтропии, а только разность энтропий в двух состояниях системы.
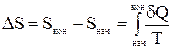 .
.
Расчет изменения энтропии в необратимых процессах.
Запишем равенство и неравенство Клаузиуса для обратимого и необратимого процесса:
 ;
; 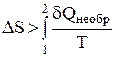 (12)
(12)
Пусть система из состояния 1 в состояние 2 перейдет двумя путями - обратимым и необратимым. Поскольку энтропия есть функция состояния, то ее изменение не зависит от пути перехода системы из одного состояния в другое, т.е. DSнеобр = DSобр =S2 - S1 (13)
Поэтому для нахождения изменения энтропии реального необратимого процесса нужно разбить его на стадии, которые проводятся обратимо, вычислить для них изменения энтропии по соответствующим уравнениям для обратимых процессов, а затем просуммировать изменения энтропии DS для всех стадий.
|
|
|
 |
DS1 = DS2 + DS3 + DS4. (14)
Изменения энтропии в процессе фазового перехода (изотермический процесс).
К изотермическим процессам фазового перехода можно отнести плавление, кипение, и др., здесь Т =const. Данный процесс проведем обратимо и рассчитаем изменение энтропии DS:
 ; где (15)
; где (15)
Q – величина теплового эффекта соответствующего фазового перехода.
Если рассматривать переход при постоянном давлении, то:
Qр = DHф.п.
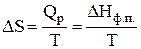 , где (16)
, где (16)
DHф.п – энтальпия фазового перехода.
Обычно DS относят к 1 моль вещества.
Изменение энтропии при нагревании (охлаждении) вещества от Т1 до Т2
при постоянном объеме.
Рассмотрим моль вещества. При постоянном объеме dQ = dQV, но
dQV = dU =СVdT, поэтому
 . (17)
. (17)
Интегрируем:
 ;
;  . (18)
. (18)
Если СV = const, то получаем для 1 моля:
 . (19)
. (19)
Изменение энтропии при нагревании (охлаждении) вещества
от Т1 до Т2 при постоянном давлении.
Аналогично предыдущему получим:
dQ = dQр = dH, dH = СpdT;
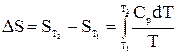 ; (20)
; (20)
Если р = 1 атм и С0p = const:
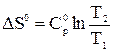 (21)
(21)
Пример 2.1. Определить изменение энтропии при нагреве 1 моль Al от 25 до 6000С, если для него в этом интервале теплоёмкость зависит от температуры следующим образом:

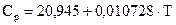 , (Дж/моль К).
, (Дж/моль К).
Решение. Согласно уравнению (2.7) имеем:
 ,
,
 (Дж/моль К).
(Дж/моль К).
Изменение энтропии при изотермическом расширении (сжатии)
идеального газа.
Ранее из объединенного первого и второго закона термодинамики для обратимых процессов было показано, что
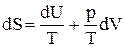 , (22)
, (22)
но dU = СVdT; для 1 моля идеального газа справедливо уравнение Менделеева-Клапейрона pV = RT, следовательно  . Поэтому получим:
. Поэтому получим:
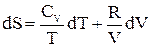 (23)
(23)
При T = const dT = 0, следовательно, 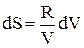 .
.
Проинтегрируем последнее выражение:
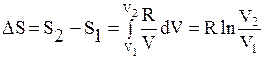 . (24)
. (24)
Так как при постоянной температуре для идеального газа справедлив закон Бойля-Мариотта:
р1V1 = р2V2, то 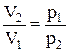 ,
,
|
|
|
следовательно,
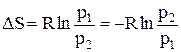 . (25)
. (25)
Изменение энтропии идеального газа при одновременном изменении его температуры и объема или при одновременном изменении его температуры и давления.
Проинтегрировав соотношение  при СV = const, получим:
при СV = const, получим:
 ; (26)
; (26)
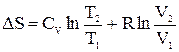 . (27)
. (27)
Из последнего соотношения, с учетом того, что для 1 моля идеального газа выполняется уравнение Майера (Ср – СV = R, следовательно, СV = Ср – R),
проведя соответствующие преобразования и учтя, что  и
и  (объединенный газовый закон), получим:
(объединенный газовый закон), получим:
 . (28)
. (28)
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2563; Нарушение авторских прав?; Мы поможем в написании вашей работы!