
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энтропия
|
|
|
|
Обратимые и необратимые процессы.
Опр.3.4.11. Обратимым термодинамическим процессом называется термодинамический процесс, допускающий возможность возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Необходимым и достаточным условием обратимости термодинамического процесса является его равновесность.
Опр.3.4.12. Необратимым термодинамическим процессом называется термодинамический процесс, не допускающий возможности возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Все реальные процессы протекают с конечной скоростью. Они сопровождаются трением, диффузией и теплообменом при конечной разности между температурами системы и внешней среды. Следовательно, все они неравновесны и необратимы.
Всякий необратимый процесс в одном направлений (прямом) протекает самопроизвольно, а для осуществления его в обратном направлении так, чтобы система вернулась в первоначальное состояние, требуется компенсирующий процесс во внешних телах, в результате которого состояния этих тел.оказываются отличными от первоначальных. Например, процесс выравнивания температур двух соприкасающихся различно нагретых тел идет самопроизвольно, т. е. не связан с необходимостью одновременного существования каких-либо процессов в других (внешних), телах. Однако для осуществления обратного процесса увеличения разности температур тел до первоначальной нужны компенсирующие процессы во внешних телах, обусловливающие, например, работу холодильной машины
Опр.3.4.13. Энтропией называется функция S состояния системы, дифференциал которой в элементарном обратимом процессе равен отношению бесконечно малого количества тепла, сообщенного системе, к абсолютной температуре последней: 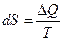 . (3.4.37.)
. (3.4.37.)
|
|
|
Энтропия сложной системы равна сумме энтропии всех ее однородных частей.
Изменение энтропии выражается формулой 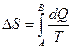 , (3.4.38.)
, (3.4.38.)
где символы А и В показывают пределы интегрирования, соответствующие начальному и конечному состояниям системы.
По знаку изменения энтропии системы в обратимом процессе можно судить о направлении теплообмена. Для всех обычных термодинамических систем внутренняя энергия U неограниченно возрастает при Т , поэтому абсолютная температура в равновесных состояниях может быть только положительной, так что при нагревании системы dS>0, а при охлаждении dS<0.
Опр.3.4.14. Изоэнтропийным процессом называется термодинамический процесс, в котором энтропия системы не изменяется. Например, в обратимом адиабатическом процессе 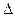 Q = 0 и S = const.
Q = 0 и S = const.
Энтропия тела может быть определена только с точностью до постоянного слагаемого (константы интегрирования).
Формула Больцмана 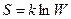 , (3.4.39.)
, (3.4.39.)
где 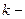 постоянная Больцмана,
постоянная Больцмана, 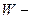 термическая вероятность состояния системы.
термическая вероятность состояния системы.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 436; Нарушение авторских прав?; Мы поможем в написании вашей работы!