
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 10. Теоретическая прочность такого идеального полимера sm, т.е
|
|
|
|
F
F
l 0
А В
lm
Теоретическая прочность такого идеального полимера s m, т.е. удельное напряжение, при котором произойдет разрыв образца, будет равна:
s m = N *Fm 1.
где Fm – сила (энергия связи) взаимодействия двух соседних атомов в цепи, которые находятся на расстоянии длины химической связи lm;
N – число связей между атомами, приходящихся на единицу площади разрыва. Единицей площади разрыва в данном случае является квадратик (смотри пунктирный квадрат) между соседними цепями макромолекул, расположенными на расстоянии l0 друг от друга (т.е. сторона квадрата равна l0);
Если к полимеру не приложена внешняя нагрузка, то теоретическое время ожидания разрыва одной химической связи t в идеальном полимере (т.е. долговечность химической связи) зависит от температуры и описывается уравнением Аррениуса (см. уравнение 2)
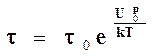 2.
2.
где t0 – период собственных колебаний атомов, 10 –14с; U0р – энергия активации разрыва связи; lm – расстояние между атомами в цепи идеального полимера.
Когда к макромолекулам полимера приложена внешняя растягивающая сила F, то энергия химической связи ослабляется и потенциальный барьер U0 снижается. Он уменьшается на величину той работы (работа = сила * путь, т.е. А= F*lm), которую совершает эта сила на своем пути, равном расстоянию от атома до атома вдоль цепи макромолекул lm. (см. рисунок).
Разрушение полимера облегчается; оно наступает при разрушающем напряжении, меньшем по сравнению с теоретическим sm. Время до наступления разрушения химической связи (время ожидания разрыва), т.е. долговечность связи также уменьшается (см. уравнение 3).
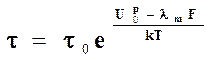 3.
3.
Общее усилие F, которое приходится на площадь квадратика около макромолекулы, находящуюся между атомами соседних цепей, можно выразить как
|
|
|
F=s* l02,
где s -удельная нагрузка на единицу площади, приходящейся на одну молекулярную цепь,
l0 -расстояние между цепями макромолекул.
Если вместо F подставить в уравнение 3 полученное выше выражение, то получим уравнение 7.4.
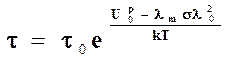 или
или  4.
4.
В уравнении 4 произведение lm* l02 = Vа представляет собой микрообъем (флуктуационный объем), в пределах которого находятся соседние атомы в цепи и атомы соседних цепей. В пределах этого микрообъема происходят колебания атомов под нагрузкой s и разрыв одной самой слабой химической связи между этими атомами.
Уравнение 4 показывает, что приложенная внешняя удельная нагрузка s облегчает разрушение, уменьшает теоретическую прочность полимера и снижает время до наступления разрыва химической связи.
Развивая далее свою теорию Александров А.П. и Журков С.Н. учли следующие факторы:
1. В реальных полимерах по сравнению с идеальной моделью цепи макромолекул свернуты в клубки и не являются строго ориентированными. В момент разрыва не все макромолекулы и их химические связи попадают в поверхность разрыва и поэтому рвутся не все химические связи и рвутся они не одновременно. В момент разрыва в поверхность разрыва попадает только часть химических связей N0. Учитывая это, авторы теории получили уточненное уравнение 5.
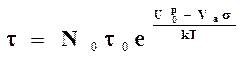 или
или  5
5
2. В реальных полимерах по сравнению с идеальной моделью внешняя нагрузка на связи между атомами в цепи макромолекул распределяется не равномерно. Некоторые связи испытывают перегрузку, поэтому их долговечность (время до разрыва) меньше. Учитывая коэффициент перегрузки таких связей c0 Александров А.П. и Журков С.Н. еще раз уточнили свое прежнее уравнение и получили уравнение для долговечности химической связи реального полимера в виде 6.
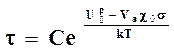 или
или 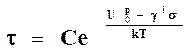 6
6
где c0 – коэффициент перегрузки отдельных связей; С – константа, равная 8 ×10-7 ¸3×10-14
|
|
|
g1 = c0 × Vа - структурный коэффициент
3. В реальных полимерах (в объеме или на поверхности) всегда имеются микродефекты, микротрещины, пустоты, "дырки". В вершинах таких дефектов всегда развиваются перенапряжения
 |
В результате избыточных перенапряжений потенциальный барьер разрыва химической связи U0 еще сильнее снижается и время до ее разрыва уменьшается. Снижение долговечности химической связи с учетом перенапряжений в местах дефектов, пустот, микротрещин авторы теории прочности учли с помощью коэффициента перенапряжений b. Тогда долговечность химической связи в реальном полимере описывается уравнением 7.
 или
или 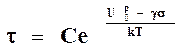 7.
7.
где b - коэффициент перенапряжений в вершинах микротрещин.
Коэффициент g, равный g = b × g1 =c0 × Vа × b получил название структурно-чувствительный коэффициент.
Уравнение 7 стало называться уравнением долговечности реального полимера.
Физический смысл структурно-чувствительного коэффициента g в этом уравнении – это микрообъем, в котором происходит перевод механической энергии в тепловую энергию разрыва химической связи и образуется первичная поверхность разрыва в полимере.
Механизм и причину разрыва непосредственно самой химической связи авторы теории подробно объяснили с позиций термофлуктуационной (или иначе "фононной") теории колебаний атомов.
Согласно термофлуктуационной теории:
1. Когда внешняя нагрузка на полимер мала (s» 0) и температура Т низкая, то атомы совершают около положения равновесия небольшие гармонические колебания. (Гармонические колебания – это колебания, флуктуации, протекающие во времени по синусоидальному закону, в ходе которых амплитуда, частота и фаза колебаний не зависят от времени, т.е. постоянны (const.).
2. Когда повышается внешняя нагрузка s на полимер или растет температура Т, то амплитуда колебаний разных по природе атомов возрастает на разную величину. Колебания атомов становятся неодинаковыми по амплитуде, начинают отличаться по фазе и частоте, т.е. становятся ангармоничными. Это явление получило название ангармонизма. Возможны два вида ангармонизма: силовой (под влиянием s) и температурный (под влиянием Т).
|
|
|
В результате ангармонизма химические связи неравномерно растягиваются и сжимаются в разных локальных участках полимера. Появляются области сильно растянутых связей, которые называются "дилатоны".
На растяжение связей в дилатонах затрачивается энергия, и чтобы скомпенсировать эти затраты в область дилатона подкачивается, подсасывается энергия из соседних участков, микрообъемов полимера.
В итоге в микрообъеме дилатона концентрируется избыток (сгусток, всплеск) энергии, который называется "фонон". За счет энергии фонона химическая связь в дилатоне еще более растягивается и рвется.
Теория фононов называется термофлуктуационной теорией разрушения химической связи в полимерах. Согласно данной теории процесс разрушения полимера идет в две стадии:
1. образование дилатонов за счет ангармонизма колебаний (флуктуаций);
2. разрыв перенапряженной химической связи в дилатоне.
В конечном итоге советский физико-химик Бартенев Г.М. вывел окончательное уравнение долговечности полимера в виде 8, которое сходно с уравнение 7, но в котором значения предэкспоненциального множителя А и структурно-чувствительного коэффициента g учитывают ангармонизм.
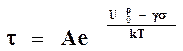 8
8
Из него следует, что с повышением температуры и внешней нагрузки долговечность полимера снижается.
В логарифмической форме уравнение долговечности Бартенева Г.М. имеет вид 9.
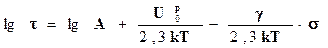 9
9
Графически оно представляет собой серии прямых:
v при стабилизированном значении температуры долговечность падает с повышением нагрузки по уравнению первого порядка (смотри рисунок 49-а);
v при стабилизированном значении внешней нагрузки долговечность также прямолинейно уменьшается при повышении температуры (снижении 1/Т) согласно рисунку 49-б.
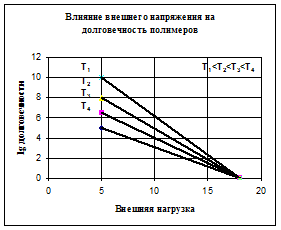
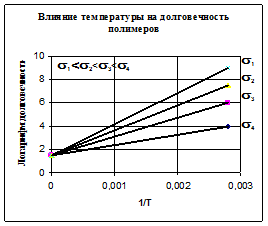
а) б
Рисунок 40 – Влияние внешнего напряжения и температуры на долговечность:
А) при постоянной температуре; б) при постоянной внешней нагрузке
Если уравнение долговечности Бартенева решить относительно значения внешней нагрузки s, то можно рассчитать реальную нагрузку, которую может выдержать полимер, т.е. реальную прочность sр.
|
|
|
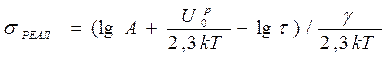 10
10
Эта прочность рассчитывается с учетом всех возможных влияющих факторов (неравноценности нагружения связей, перегрузок и перенапряжений, различий в характере связей, наличия микродефектов, микротрещин, явления ангармонизма).
Поэтому такая реальная прочность на несколько порядков меньше, чем теоретическая прочность s m , найденная авторами теории в самом начале для идеального предельно-ориентированного бездефектного полимера (смотри таблицу 9).
Таблица 9 – Прочность полимеров
| Полимер | Теоретическая прочность, sm, МПа | Реальная прочность, sр, МПа |
| ПЭ | 26 000 – 27 000 | 20 – 40 |
| ПП | 11 000 – 12 500 | 80– 200 |
| ПВХ | 14 000 – 17 000 | 50 – 100 |
Из теории прочности следует, что основная причина разрушения полимеров – это тепловые флуктуации, а внешние нагрузки и дефекты ускоряют и облегчают термофлуктуационный разрыв связей.
Для повышения прочности необходимо:
1. Стремиться повысить степень ориентации цепей (ориентационная вытяжка);
2. Повышать плотность упаковки макромолекул полимера (по возможности медленная кристаллизация или стеклование);
3. Снижать дефектность полимера и уменьшать коэффициент перенапряжений (те же приемы, что в пп. 1-2)
4. Получать трехмерно сшитые полимеры;
5. Создавать структурно- и стереорегулярные полимеры (Ионно-координационная полимеризация, анионная полимеризация);
6. Синтезировать полимеры с прочными химическими связями (например ароматические полиимиды, полифенилены, поликарбонат и др.)
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 602; Нарушение авторских прав?; Мы поможем в написании вашей работы!