
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кулонометрія
Цей метод електрохімічного аналізу, який ґрунтується на вимірюванні кількості електричного струму, витраченого на електрохімічне перетворення аналізованої речовини, ґрунтується на законах електролізу.
Кулонометрію використовують тоді, коли електрогравіметричний метод застосувати не можна:
- коли на електроді виділяється невелика кількість речовини, що зменшує точність аналізу;
- продукт реакції є рідина або газоподібна сполука.
В кулонометричному аналізі використовують 2 електролітичні комірки: у першій знаходиться досліджуваний розчин у другій, яка називається кулонметром, відбувається електрохімічна реакція з виходом за струмом 100%.
 |



 1-комірка з аналізованим розчином;
1-комірка з аналізованим розчином;

 2-потенціостат;
2-потенціостат;

 3-вольтметр;
3-вольтметр;
 4-амперметр;
4-амперметр;

 5-кулонометр.
5-кулонометр.



Рис. 5.2 Схема приладу для проведення кулонометричного аналізу
Оскільки кількість електричного струму, що проходить через досліджуваний розчин і кулонометр, однакова, то відношення:
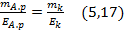
де mа.р.і mк – маса речовини, що виділяється в процесі електролізу аналізованого розчину і того, який знаходиться у кулонометрі, відповідно;
Еа.р і Ек – їх молярні маси еквівалентів.
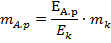
Типи кулонометрів:
I. Гравіметричний кулонометр (мідний або срібний)
Ag+ + е = Ag; Cu2++2e= Ag
Кількість струму, який пройшов через кулонометр, а отже, і через досліджуваний розчин, розраховують за збільшенням маси електрода кулонметра.
II. Титраційний кулонометр. Кількість струму визначають за об’ємом розчину тіосульфату натрію, витраченого на титрування йоду, що утворився в результаті електролізу йодиду калію:
2I- - 2e = I2
I2 + 2S2O32- → 2I- + S4O62-
III. Газовий кулонометр. Фіксують сумарний об’єм водню і кисню, виділених у процесі електролізу води, і розраховують кількість пройденого електричного струму через кулонометр і електролітичну комірку з досліджуваним розчином.
(-) H2O + 2e → H2 ↑ + 2OH-
(+) 2H2O - 4e = O2↑ +4H+
Пряму кулонометрію використовують, як високоточний і високоселективний метод, який дає змогу визначати вміст речовини до 10-5 моль/л.
Цим методом визначають:
- іони металу;
- нітро- і галоген похідні при катодному відновленні;
- Hal – іони;
- іони металів у нижчих ступенях окиснення при анодному окисненні.
Кулонометричне «титрування»
Використовується значно частіше, ніж пряма кулонометрія, оскільки цим методом можна визначити як електроактивні, так і електронеактивні сполуки, здатні кількісно реагувати з титрантом у кислотно основних, окисновідновних реакціях, реакціях осадження.
Титрант не вводять зовні, він утворюється на генераторному електроді внаслідок електрохімічної реакції (електрогенерації титранта) за участю:
а) розчинника в наслідок відновлення води до OH-
2 H2O + 2e = H2+ 2OH - (титрант)
СН3СООН + ОН-→СН3СОО- + Н2О;
б) Матеріал аноду (окиснення срібла до Ag+)
Ag – e → Ag+ (титрант)
Cl-+Ag+→AgCl
в) Допоміжного реагенту (окиснення йодид-іонів до вільного йодиду);
2I- - 2e = I2 (титрант)
AsO33-+I2+H2O= AsO43-+2I-+2H+
Кулонометричне титрування має ряд переваг, порівняно з прямою кулонометрією, оскільки розширює спектр визначення речовин, відсутня необхідності приготування розчинів титр антів, їх стандартизація і зберігання.
За допомогою одного і того ж джерела струму можна готувати різні титранти, зокрема і не стійкі за звичайних умов. У кулонометричному титруванні можна визначати малі кількості речовини (10-4, 10-5 моль/л)
Індикацію кінця титрування проводять за допомогою індикаторів, чи одним із інструментальних методів фотоколориметричним, потенціометричним, амперметричним, при цьому фіксують зміну оптичної густини розчину, величини потенціалу індикаторного електрода, сили струму.
|

|
|


 | |||
 | |||
т.е τ т.е τ
Fe2+ + Ce2+→ Fe3+ + Ce3+ (титрування) [Fe(CN)6]3- + e = [Fe(CN)6]4- (генерація «титранта»)
Ce4+: Ce3+ - e → Ce2+ (генерація «титранта») Zn2+ + 2K++[Fe(CN)6]3-→ K2Zn3[Fe(CN)6]2↓(титрування)
Рис. 5.3. Криві кулонометричного титрування.
Кулонометричне титрування проводять:
- за постійної сили струму (у гальваностатичному режимі)
- за постійної напруги (у потенціостатичному режимі)
В кулонометричному титруванні використовують всі типи реакцій титрометричного аналізу:
- кислотно-основні взаємодії (визначають малі кількості кислот і основ (10-4-10-5 моль/л) з електрогенерованими гідроксид-іонами та протонами;
- осадження (визначають галогенід- та сульфід іони з електрогенеративними йонами Ag+);
- комплексоутворення (зокрема, комплексонометрію) (катіони металів «титрують» розчином електрогенерованого із Hg2- трилоном Б – HgY2- + 2e= HgY2+ Hg);
- окиснення-відновлення (електрогенерованим «титрантом» - бром - «титрують»відновники (І-, AsO33-, гідразин) та фелол, який при цьому хромується).
|
|
Дата добавления: 2014-01-11; Просмотров: 1925; Нарушение авторских прав?; Мы поможем в написании вашей работы!