
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Выход по току. Применение закона Фарадея к расчету скорости обработки металлов
|
|
|
|
Лекция 2. Законы Фарадея и скорость электрохимического процесса
Электрохимические реакции – это гетерогенные химические реакции, протекающие на границе раздела различных фаз, сопровождающиеся переносом зарядов через эту границу.
Все электрохимические реакции при своей записи должны содержать в левой или правой части электроны, потому что происходит их перенос при протекании реакции.
Первое, что необходимо знать - это скорость реакции:
Vm = d∆m/dt, (2.1)
где Vm - количество вещества, перешедшее через границу в единицу времени.
Обозначим через N число ионов, перешедших в раствор, а через Q - полный заряд иона, получающегося в результате реакции
Ме 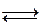 Ме +n+n
Ме +n+n 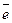 , (2.а)
, (2.а)
где 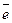 - элементарный заряд, заряд электрона. Тогда
- элементарный заряд, заряд электрона. Тогда
N = Q/ne. (2.2)
Учитывая, что масса иона а равна атомной массе М, деленной на число Авогадро Na, получим:
∆m = aN =MQ/Na n 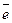 (2.3)
(2.3)
Произведение Na 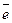 – это произведение двух фундаментальных постоянных (числа Авогадро и заряда электрона). Это произведение носит название константы Фарадея F = 96500 Кл/моль = 26,8 А·час/моль.
– это произведение двух фундаментальных постоянных (числа Авогадро и заряда электрона). Это произведение носит название константы Фарадея F = 96500 Кл/моль = 26,8 А·час/моль.
Тогда:
∆m = 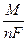 Q =
Q = 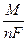 It, (2.4)
It, (2.4)
где I - ток, t - время, Q - количество электричества. Уравнение (2.4) представляет собой т.н. объединенный закон Фарадея.
Масса вещества, перешедшая в раствор (или выделившаяся на катоде) пропорциональна заряду, прошедшему через систему:
∆m = CQ (2.5)
C = 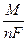 (2.6)
(2.6)
Величина С носит название электрохимического эквивалента (размерность г/Кл; г/А час).
Закон Фарадея является простым следствием атомарной природы вещества. Величие этого закона природы в том, что благодаря ему осуществляется связь между микромиром (заряд иона, единичный заряд) и макромиром (вес осадка на электроде, количество прореагировавшего вещества).
Отношение 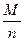 носит название химического эквивалента.
носит название химического эквивалента.
|
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 625; Нарушение авторских прав?; Мы поможем в написании вашей работы!