
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Сера и ее соединения
|
|
|
|
Сера представлена в природе четырьмя изотопами: 32S (95%), 33S, 34S и 36S. Кларк серы составляет 0,03 мол.%. Значительное количество серы находится в виде простого вещества (самородная сера). Однако бóльшая часть серы входит в состав минералов, как сульфидных, так и сульфатных: ZnS - цинковая обманка, сфалерит; PbS - свинцовый блеск, галенит; Cu2S - медный блеск; HgS - киноварь; FeS2 - железный колчедан или пирит; CuFeS2 - халькопирит; Na2SO4×10H2O - глауберова соль или мирабилит; CaSO4×2H2O - гипс.
Элемент сера образует несколько аллотропных модификаций. Наиболее устойчива ромбическая сера (a-сера), представляющая собой желтые хрупкие кристаллы, нерастворимые в воде, но растворимые в некоторых органических растворителях (сероуглерод, толуол). При температуре выше 96 °С устойчива моноклинная сера (b-сера). Обе модификации имеют молекулярное строение и построены из циклических молекул S8 , по-разному упакованных в кристалле, т.е. фактически представляют собой полиморфные модификации.

При нагревании кристаллической серы до 113 °С она плавится, образуя темную подвижную жидкость, которая при дальнейшем нагревании вначале густеет, а затем снова размягчается и при температуре 445 °С закипает. В парах сера, в зависимости от температуры, образует молекулы разного состава:
>1500 °C
S8 ¾® S6 ¾® S4 ¾® S2 ¾® S
При выливании кипящей серы в воду образуется пластическая сера, представляющая собой тягучую массу, напоминающая сырой каучук, образованная полимерными зигзагообразными цепями

Пластическая сера неустойчива и со временем переходит в ромбическую серу.
Чистая сера не ядовита. Прием внутрь небольших ее количеств способствует заживлению ран и нарывов. Серный порошок входит в состав мазей для лечения кожных заболеваний.
|
|
|
Строение атома серы - 1s22s22p63s23p43d0 - обуславливает проявление этим элементом степени окисления - 2 при взаимодействии с элементами меньшей электроотрицательности. Образуя связи с элементами большей электроотрицательности (F, O, N, Cl), сера проявляет высшие валентности и положительные степени окисления (в основном +4 и +6) за счет переноса части валентных электронов на вакантные d-орбитали:
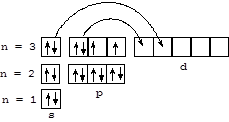
Химические свойства. Сера - активный неметалл, легко взаимодействующий с активными металлами и неметаллами. В парах серы горит водород:
t
H2 + S  H2S
H2S
При нагревании сера окисляет углерод и кремний:
t t
С + 2S = CS2; Si + 2S = SiS2
В качестве окислителя сера выступает также при взаимодействии с металлами. Большинство реакций данного типа требует нагревания, при комнатной температуре с серой реагирует только ртуть.
t
Zn + S = ZnS; Hg + S = HgS
Использование избытка серы приводит к образованию полисульфидов, простейшим представителем которых является дисульфид железа(II), образующий минерал пирит:
Fe + 2S = FeS2
При взаимодействии с галогенами и кислородом сера выступает в качестве восстановителя. Фтор обычно окисляет серу до высшей степени окисления с образованием SF6. Взаимодействие серы с хлором идет ступенчато:
t t
2S + Cl2 = S2Cl2; S2Cl2 + Cl2 = 2SCl2
Горение серы на воздухе и в атмосфере кислорода приводит к образованию оксида серы(IV):
t
S + O2 = SO2
При кипячении с кислотами-окислителями (азотная и концентрированная серная кислота) сера также окисляется:
t
S + 4HNO3(конц) = SO2 + 4NO2 + 2H2O
При нагревании с водными растворами щелочей сера диспропорционирует:
3S + 6KOH = 2K2S + K2SO3 + 3H2O
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 813; Нарушение авторских прав?; Мы поможем в написании вашей работы!