
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. Опыт 1. Получение золя гидроксида железа (III) методом конденсации
Выполнение работы
Опыт 1. Получение золя гидроксида железа (III) методом конденсации
Пробирку заполнить водой (примерно до половины ее объема) и поставить в горячую водяную баню. Через 5–7 минут внести в пробирку 2–3 капли концентрированного раствора FeCl3. Наблюдать образование краснооранжевого золя Fe(OH)3. Раствор сохранить для опыта 3.
Требование к результатам опыта
Указать состав ядра коллоидной частицы полученного золя, состав коллоидной частицы, состав мицеллы.
Опыт 2. Получение золя гидроксида железа (III) методом диспергирования осадка Fe(OH)3
В стакан объемом 50 мл налить 25 мл воды и добавить 10 капель 20 %-го раствора хлорида железа FeCl3. Перемешать содержимое стакана и после этого добавить по каплям раствор гидроксида аммония NH4OH до полного осаждения гидроксида Fe(OH)3.
После того как осадок уплотнится на дне стакана, осторожно слить с него избыток раствора. Осадок промыть 2–3 раза, добавляя к нему небольшие порции воды и сливая эту воду после того, как между ними и осадком четко обозначится граница раздела.
К осадку гидроксида железа (III) прилить 25 мл H2O и 3 капли 20 %-го раствора FeCl3. Смесь хорошо перемешать. Для ускорения процесса пептизации нагреть раствор на водяной бане. Прекратить нагревание, когда раствор приобретет устойчивую краснооранжевую окраску.
Требование к результатам опыта
Составить схему строения мицеллы золя гидроксида железа (III) в растворе хлорида железа FeCl3.
Опыт 3. Коагуляция золя гидроксида железа электролитами
Разлить в три пробирки золь гидроксида железа, полученный в опыте 1. По каплям прибавить в первую пробирку NaCl, во вторую – Na2SO4 , в третью – Na2HPO4. Считать число капель до изменения вида раствора (появления мути и осадка).
Требования к результатам опыта
1. Написать формулу мицеллы золя гидроксида железа.
2. Объяснить влияние заряда коагулирующего иона на время, проходящее до начала коагуляции.
Пример 10.1. Золь иодида серебра получен при добавлении к раствору AgNO3 избытка KI. Определить заряд частиц полученного золя и написать формулу его мицеллы.
Решение. При смешивании растворов AgNO3 и KI протекает реакция
AgNO3 + KI (изб.) = AgI + KNO3.
Ядро коллоидной частицы золя иодида серебра состоит из агрегата молекул (mAgI) и зарядообразующих ионов I‾, которые находятся в растворе в избытке и обеспечивают коллоидным частицам отрицательный заряд. Противоионами являются гидратированные ионы калия. Формула мицеллы иодида серебра имеет вид {[(m AgI)· n I‾·(n-x)К+· y H2O] x − + x К+∙ z H2O}0.
Пример 10.2. Золь кремневой кислоты был получен при взаимодействии растворов K2SiO3 и HCl. Написать формулу мицеллы золя и определить, какой из электролитов был взят в избытке, если противоионы в электрическом поле движутся к катоду.
Решение. Образование золя кремневой кислоты происходит по реакции
K2SiO3 + 2HCl = H2SiO3 + 2KCl.
Чтобы двигаться к катоду (отрицательному электроду) противоионы должны иметь положительный заряд, а коллоидные частицы золя должны быть заряжены отрицательно. На электронейтральном агрегате частиц (mH2SiO3) адсорбируются ионы элемента, входящего в состав ядра. Таковыми являются ионы HSiO3‾, которые образуются в результате гидролиза соли K2SiO3:
K2SiO3 + H2O 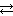 KHSiO3 + KOH или в ионной форме
KHSiO3 + KOH или в ионной форме
SiO32− + H2O 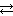 HSiO3‾ + OH‾.
HSiO3‾ + OH‾.
Ионы HSiO3‾, адсорбируясь на поверхности частиц золя кремниевой кислоты, сообщают им отрицательный заряд. Противоионами являются гидратированные ионы водорода H+. Формула мицеллы золя кремневой кислоты
{[(m H2SiO3) · n HSiO3‾·(n-x)H+∙ y H2O] x − + x H+∙ z H2O}.
Так как коллоидные частицы золя кремневой кислоты заряжены отрицательно за счет ионов HSiO3‾, то, следовательно, в избытке был взят K2SiO3.
Пример 10.3. Какого из веществ, K2SO4 или KCl, потребуется меньше, чтобы вызвать коагуляцию коллоидного раствора гидроксида железа (II), полученного по реакции FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl?
Решение. Из формулы коллоидной частицы золя гидроксида железа (II) [(m Fe(OH)2· n Fe2+ 2(n-x)Cl‾∙yH2O]2 x + видно, что частицы золя имеют положительный заряд. Коагуляцию золя вызывает тот из ионов прибавленного электролита, заряд которого противоположен заряду коллоидной частицы. В данной задаче – это ионы SO42− и Cl‾. Коагулирующая способность иона определяется его зарядом – чем больше заряд иона, тем больше его коагулирующая способность. Заряд иона SO42− больше заряда иона Cl‾, поэтому, чтобы вызвать коагуляцию коллоидного раствора гидроксида железа (II), раствора K2SO4 потребуется меньше, чем раствора KCl.
Пример 10.4. Составить схему строения мицеллы золя гидроксида меди (II) в растворе хлорида меди.
Решение. В состав мицеллы гидроксида меди входят: агрегат молекул (mCu(OH)2), адсорбированный слой, состоящий из зарядообразующих ионов меди Cu2+ и гидратированных противоионов хлора, и диффузный слой гидратированных противоионов хлора. Схема строения мицеллы гидроксида меди
{[(m Cu(OH)2·nCu2+ 2(n-x)Cl‾∙ y H2O]2 x + + 2 x Cl‾∙ z H2O}.
|
|
Дата добавления: 2014-10-15; Просмотров: 2697; Нарушение авторских прав?; Мы поможем в написании вашей работы!