
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Температура. Факторы, влияющие на скорость химических реакций
Факторы, влияющие на скорость химических реакций. Реакционный механизм. Переходное состояние промежуточная частица, промежуточное соединение.
Раздел химии, изучающий скорость химических реакций называется химической кинетикой.
Скорость химической реакции – число элементарных актов реакции, происходящих в единицу времени, в единице объема (для гомогенных реакций) или на единице поверхности (для гетерогенных реакций) раздела фаз. Мерой скорости хим. реакции называется количество вещества, вступившего в реакцию или образовавшегося при реакции за единицу времени в единице объема системы (для гомогенных реакций) или на единице поверхности раздела фаз (для гетерогенной реакции).
V, моль·л/с
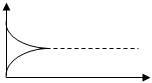 |
Vпрям
Vпрям=Vобратн
Vобратн
T, сек
Факторы влияющие на скорость хим реакции:
Правило Вант-Гоффа: при повышении t на каждые 10 градусов скорость химической реакции возрастает в 2-4 раза.
Vt2=Vt1*γt1-t2/10 где γ – температурный коэффициент реакции.
2.Концентрация реаг.в-тв. (чем больше скорость х.р.,тембольше концентрация).
3.Площадь соприкасновения( только для тв.в-тв)чем больше площадь,тем быстрее идёт р-я.
4.Природы реагир.веществ.
5. Катализаторов – вещество, не расходующееся в результате протекания реакции, но ускоряющее р-ю.Ингибиторов-замедляющих.Промоторы-катализатор катализатора.
Зависимость скорости химической реакции от катализатора – катализатор снижает энергию активации реакции. В присутствии катализатора реакция проходит через другие промежуточные стадии, и эти стадии энергетически более доступны.
Бывают катализаторы как ускоряющие протекание реакции, так и замедляющие ее. В первом случае катализ называется положительным, а во втором - отрицательным.
Реакционный механизм- 
ПЕРЕХОДНОЕ СОСТОЯНИЕ (активированный комплекс), конфигурация системы атомных ядер и электронов, участвующих в элементарном акте химической реакции, в момент преодоления системой энергетического барьера, разделяющего ее начальное и конечное состояния. Теорию переходного состояния применяют для расчета скоростей химических реакций.
Промежуточная частица-
Промежут.соединение-
|
|
Дата добавления: 2015-04-23; Просмотров: 374; Нарушение авторских прав?; Мы поможем в написании вашей работы!