
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теплоємність ідеальних газів.Вивести рівняння майєра
|
|
|
|
Внутрішня енергія термодинамічної системи
Молекулярна фізика дає тлумачення внутрішньої енергії як суми кінетичних енергій всіх молекул та потенціальної енергії їх взаємодії. В подальшому розглядаються тільки такі процеси, в яких не відбувається перетворень молекул, атомів або їх ядер. Енергія, як завжди, визначається з точністю до адитивної константи, тому всі види енергії вказаних джерел вводяться в константу, яка приймається нульовою. Внутрішня енергія ідеальних газів складається тільки з кінетичної енергії руху молекул і дорівнює 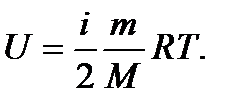
В термодинаміці внутрішню енергію частіше позначають літерою U, тому приймемо його. Кількість теплоти та робота відповідно позначаються літерами Q та A.
Відповідно до визначення теплоємностей і співвідношень для теплоємностей ідеальних газів маємо:
а) для ізохоричного процесу - 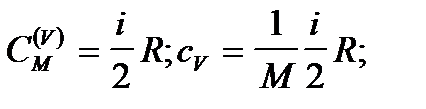
б) для ізотермічного процесу теплоємність не визначена і прямує до нескінченності - 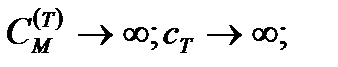
в) для ізобарного процесу - 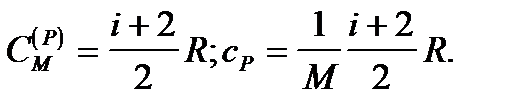
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 856; Нарушение авторских прав?; Мы поможем в написании вашей работы!