
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Закон Авогадро
|
|
|
|
Закон Шарля
V=const – ізохорний процес
Для даної маси ідеального газу при сталому V, зміна температури на 1° С призводить до зміни на 1⁄ 273,16 його початкового об’єму виміряного при 0° С.
Pt = P0 (1 + 1/273, 16 * t)
Якщо 1/273, 16 = β тоді Pt = P0 (1 + β * t)
P=f(t) – ізохора
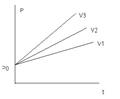
Абсолютна температура Т – це температура, початкове значення якої приймається за 0 К, при якому тиск газу буде також рівний 0.
Для даної маси ідеального газу при сталому об’ємі відношення тисків ідеального газу будуть прямо пропорційні їх абсолютним температурам.
Р1/Р2=Т1/Т2
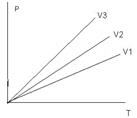
Для даної маси ідеального газу при сталому об’ємі концентрація і густина ідеального газу будуть обернено пропорційні їх абсолютним температурам
С1/С2=Т2/Т1
Одинакові об’єми різних газів при однакових умовах містять однакову кількість молекул.
NA=6.025*1023 молекул / моль
Питомий об’єм ідеального газу Vпит=22.4 / M
Питома густина ρ пит= m/V = M/Vm
Р-ння стану ідеального газу одержане внаслідок обєднання всіх законів.
PV/T=const
P1V1/T1=P2V2/T2
Використовується для приведення газу до н.у.
PV/T=P0V0/T0
Так як ρ=1/V тоді P/Tρ=P0/T0ρ0
Закон Мендєлєєва-Клапейрона
PV=nRT
N=m/M
PV=(m/M)RT
Якщо даний об’єм ідеального газу, то n=P1V1/RT1
Ф.Х.
2. Реальні гази. Рівняння стану реального газу.
Реальний газ – це газоподібний стан речовини, який відповідає наступним ознакам:
1. Між молекулами існують сили міжмолекулярної взаємодії.
2. Молекули мають власний об’єм.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 319; Нарушение авторских прав?; Мы поможем в написании вашей работы!