
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 1.3. Вплив температури на швидкість реакції. Теоретичні уявлення хімічної кінетики. Ланцюгові, фото- та радіаційно-хімічні процеси
|
|
|
|
Тема 1.2. Методи визначення порядку реакції. Кінетика складних реакцій
Запитання і завдання для самоконтролю
1. Для чого використовують метод ізоляції або надлишку реагенту?
2. Чим відрізняються інтегральні та диференціальні методи визначення порядку реакції? Які дані необхідні в першому та другому випадках?
3. До яких методів визначення порядку реакції належить метод підстановки? В чому він полягає?
4. Що являє собою графічний метод визначення порядку реакції?
5. Як визначити порядок реакції за часом напівперетворення?
6. Які диференціальні методи визначення порядку реакції Ви знаєте?
7. У чому суть методу визначення порядку реакції за Вант-Гоффом?
8. Як експериментально визначають константи швидкості реакції?
9. Опишіть методи, за допомогою яких можна визначати дробовий порядок реакції.
10. Як можна встановити порядок реакції за розмірністю її константи швидкості?
11. Які реакції називають паралельними? Наведіть приклади. Як швидкість та константа швидкості паралельного процесу пов’язана із швидкостями окремих реакцій?
12. Які реакції називають послідовними? Покажіть графічно, як залежать від часу концентрації А, В та С в реакції А ® В ® С.
13. Чим обумовлена поява максимуму на кінетичній залежності проміжної речовини в послідовній реакції? Від чого залежить його положення на кінетичній кривій? Відповідь обґрунтуйте.
14. Які реакції називають оборотними? Як за кінетичними даними можна визначити константи швидкості прямої та зворотної реакцій?
15. Які реакції називають спряженими? Поясніть їх механізм та наведіть приклади.
Типові задачі
Визначення константи швидкості та порядку реакції за даним компонентом різними методами.
|
|
|
Література: [ 1, § 201-205; 2, § ІХ.4, ІХ.1-ІХ.4, Х.6; 3, Гл. 13, § 4, Гл. 14, § 1-3; 4, 20.4-20.6].
Запитання і завдання для самоконтролю
1. Сформулюйте правило Вант-Гоффа. Що називають температурним коефіцієнтом швидкості реакції? Як він залежить від температури?
2. Наведіть диференціальне та інтегральне рівняння Арреніуса. Що таке енергія активації? Від чого вона залежиіть?
3. Як енергія активації реакції пов’язана з температурним коефіцієнтом швидкості процесу?
4. Покажіть, як за допомогою рівняння Арреніуса можна визначити енергію активації реакції. Які експериментальні дані необхідні для цього?
5. Який вигляд має графік залежності логарифма константи швидкості реакції від 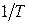 ? Як за цим графіком визначити енергію активації?
? Як за цим графіком визначити енергію активації?
6. Наведіть та поясніть енергетичні діаграми хімічних реакцій.
7. Сформулюйте основні положення теорії активних зіткнень молекул. Що розуміють під стеричним фактором? Як математично описується температурна залежність константи швидкості реакції в цій теорії?
8. Наведіть математичний вираз та графік розподілу молекул за енергіями.
9. Сформулюйте основні положення теорії перехідного стану. Що називають активованим комплексом? Наведіть основне рівняння теорії.
10. Які реакції називають ланцюговими? З яких стадій вони складаються?
11. Які ланцюгові реакції належать до нерозгалужених, а які – до розгалужених? Наведіть приклади.
12. Поясніть, як впливають температура та тиск на швидкість розгалуженої ланцюгової реакції.
13. Які реакції називають фотохімічними? В чому полягають первинний та вторинний фотохімічні процеси? Наведіть приклади фотохімічних реакцій.
14. Сформулюйте закони фотохімії. Що таке квантовий вихід? Яких значень він може набувати і чому?
15. Опишіть кінетику фотохімічних реакцій. В чому її особливість?
16. Які процеси називають радіаційно-хімічними? З яких стадій вони складаються? Чим вони відрізняються від фотохімічних реакцій? Наведіть приклади.
|
|
|
Типові задачі
1. Розрахунки за правилом Вант-Гоффа.
2. Обчислення за рівнянням Арреніуса.
Література: [ 1, § 193, 209-213, 220, 221; 2, § ІХ.6, ХІ.1-ХІ.4, ХІІ.1-ХІІ.5; 3, Гл. 15, § 1-15, Гл. 17, § 1-4; 4, 20.7-20.6, 21.1-21.3, 22, 23].
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 509; Нарушение авторских прав?; Мы поможем в написании вашей работы!