
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вимірювання електродних потенціалів металів
Безпосередньо виміряти потенціал окремого електрода неможливо – його вимірюють відносно величини потенціалу іншого електрода.
Для цього необхідно потенціал будь-якого електродного процесу прийняти за нуль. Як еталон був прийнятий електродний процес  , який відбувається на водневому електроді (рис.33).
, який відбувається на водневому електроді (рис.33).

Рис. 33. Стандартний водневий електрод
Водневий електрод – це платинова платівка, електролітично покрита губчастою платиною і занурена в розчин сульфатної кислоти з концентрацією йонів Гідрогену 1 моль/л, через який пропускається водень під тиском 101325 Па.
Водень добре розчиняється у платині. При цьому молекули водню розпадаються на атоми (платина виступає як каталізатор), які адсорбуються на поверхні платівки. На поверхні стикання платини з розчином кислоти може відбуватись окиснення атомів або відновлення йонів Гідрогену. Платина при цьому відіграє роль губки, просоченої атомарним воднем.
Для визначення потенціалу того чи іншого процесу необхідно скласти гальванічний елемент з досліджуваного і стандартного водневого електрода і виміряти його е.р.с. (рис.34).
Оскільки потенціал стандартного водневого електрода дорівнює нулю, то виміряна е.р.с. і буде потенціалом певного електродного процесу:
 , (6)
, (6)
де 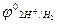 - потенціал стандартного водневого електрода,
- потенціал стандартного водневого електрода,
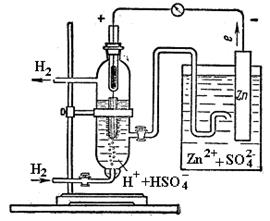
Рис. 34. Прилад для вимірювання електродного потенціалу металу
φХ - потенціал досліджуваного електрода. Розв’язуючи рівняння (6) відносно φХ, одержимо:
якщо  , то
, то  ;
;
якщо 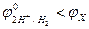 , то
, то 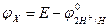 .
.
Якщо як досліджуваний електрод взяти цинк, занурений в розчин його солі з концентрацією йонів 1 моль/л, а як електрод порівняння – стандартний водневий електрод, то схема гальванічного елемента буде мати вид:
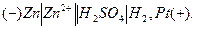
В такому елементі відбувається реакція:
 .
.
Електрони в зовнішньому колі рухаються від цинкового до водневого електрода. Стандартний електродний потенціал цинкового електрода дорівнює – 0,763 В.
Для мідного електрода в сполученні з стандартним водневим електродом за тих самих умов одержимо гальванічний елемент:
 .
.
В цьому випадку відбувається реакція:
 .
.
Електрони в зовнішньому колі рухаються від водневого електрода до мідного. Його стандартний електродний потенціал дорівнює +0,337 В.
Отже, стандартні потенціали електродів, що посилають електрони до водневого електрода, мають знак (-), а ті, що приймають електрони від водневого електрода – знак (+).
|
|
Дата добавления: 2015-05-24; Просмотров: 1503; Нарушение авторских прав?; Мы поможем в написании вашей работы!