
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. Задача 1. Какое количество теплоты выделится при сгорании 1 м3 (н.у.) природного газа, состоящего из пропана C3H8 (50%) и бутана C4H10 (50%)?
Задача 1. Какое количество теплоты выделится при сгорании 1 м3 (н.у.) природного газа, состоящего из пропана C3H8 (50%) и бутана C4H10 (50%)? В обоих случаях продуктами реакции являются CO2(г) и H2O(г). В результате сгорания какого газа выделяется больше теплоты?
Решение. Запишем уравнение реакции горения пропана и расставим стехиометрические коэффициенты:
C3H8 (г)+ 5О2 (г) = 3CO2 (г) + 4H2O(г) (а).
Рассчитаем по соотношению (4) энтальпию реакции 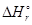 ,т.е. количество теплоты, выделившейся при взаимодействии по уравнению реакции 1 моль C3H8 с 5 моль О2:
,т.е. количество теплоты, выделившейся при взаимодействии по уравнению реакции 1 моль C3H8 с 5 моль О2:
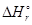 =3
=3 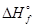 (CO2(г)) + 4
(CO2(г)) + 4 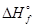 (H2O(г)) -
(H2O(г)) - 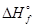 (C3H8(г)) - 5
(C3H8(г)) - 5 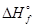 (О2(г)).
(О2(г)).
Данные для DH0f(В) берем из справочной таблицы.
Заметим, что DH0f(О2(Г)) = 0, т.к. это простое вещество в стандартном состоянии и при стандартных условиях.
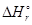 (а) = 3(-393,5) + 4(-241,8) – (-103,9) = - 2043,8 кДж.
(а) = 3(-393,5) + 4(-241,8) – (-103,9) = - 2043,8 кДж.
По условию задачи объем пропана составляет 50% от объема газовой смеси V0(C3H8) = 1×50/100 = 0,5 м3 = 500 л.
Найдем количество вещества вступившего в реакцию пропана:n(C3H8) = VО(C3H8)/22,4 = 500/22,4 = 22,3 моль.
Обратите внимание на то, что объем должна быть выражен в литрах, поскольку единицей измерения молярного объема VОм является л/моль.
Составим пропорцию (5):
по уравнению на 1 моль C3H8 ® выделяется 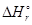 (а) кДж,
(а) кДж,
по условию на 22,3 моль C3H8 ® выделяется 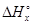 (а) кДж.
(а) кДж.
Вычислив по пропорции 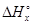 , получаем:
, получаем:
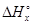 (а) =
(а) = 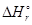 (а) × 22,3/1 = - 2043,8 × 22,3 = -45576,7 кДж.
(а) × 22,3/1 = - 2043,8 × 22,3 = -45576,7 кДж.
Аналогичные расчеты проведем для реакции с бутаном:
C4H10 (Г)+ 6,5О2 (Г) = 4CO2 (Г) + 5H2O(Г) (б).
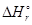 (б) = 4
(б) = 4 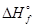 (CO2(Г)) + 5
(CO2(Г)) + 5 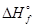 (H2O(Г)) -
(H2O(Г)) - 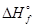 (C4H10(Г)) =
(C4H10(Г)) =
= 4(-393,5) + 5(-241,8) – (-124,7) = -2658,3 кДж.
V0(C4H10) = 1×50/100 = 0,5 м3 = 500 л.
n(C4H10) = VО(C3H8)/ VОм = 500/22,4 = 22.3 моль.
Вычисляем по пропорции (5) количество теплоты,выделяющейся при сгорании 500л бутана:
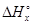 (б)=
(б)= 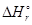 (б)×n(C4H10)/n(C4H10)=-2658,3×22,3/1=59280кДж.
(б)×n(C4H10)/n(C4H10)=-2658,3×22,3/1=59280кДж.
Ответ. Суммарное количество выделившейся теплоты
Q= 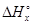 (а)+
(а)+ 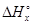 (б) = (-45576,7) + (-59280,1) = -104859.9кДж. При сгорании одинакового количества пропана и бутана, в реакции (б) выделяется больше теплоты,
(б) = (-45576,7) + (-59280,1) = -104859.9кДж. При сгорании одинакового количества пропана и бутана, в реакции (б) выделяется больше теплоты, 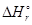 (б) <
(б) < 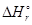 (а), т.е. теплотворная способность бутана как топлива выше.
(а), т.е. теплотворная способность бутана как топлива выше.
Задача 2. Какое количество теплоты выделится (или поглотится) при получении 10 кг гашеной извести по реакции:
CaO(тв) + H2O(ж) = Ca(OH)2 (тв)?
Решение. Рассчитаем по табличным данным энтальпию реакции 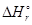 ,т.е. тепловой эффект при взаимодействии 1 моль CaO и 1 моль H2O с образованием 1 моль Ca(OH)2:
,т.е. тепловой эффект при взаимодействии 1 моль CaO и 1 моль H2O с образованием 1 моль Ca(OH)2:
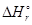 =
= 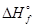 (Ca(OH)2(тв)) -
(Ca(OH)2(тв)) - 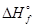 (H2O(ж)) -
(H2O(ж)) - 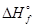 (CaO(тв)) = -986,2 - (-285,8) – (-635,1) = -986,2 + 920,1 = -65,3 кДж.
(CaO(тв)) = -986,2 - (-285,8) – (-635,1) = -986,2 + 920,1 = -65,3 кДж.
Поскольку для данной реакции 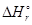 < 0, теплота выделяется.
< 0, теплота выделяется.
Рассчитаем число молей Ca(OH)2, образующихся в процессе:
n(Ca(OH)2) = m(Ca(OH)2)/M(Ca(OH)2)=10000/74 = 135,1 моль.
Обратите внимание, что масса вещества должна быть выражена в граммах, поскольку единицей измерения молярной массы M(B) является г/моль.
Составим пропорцию и решим ее относительно 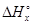 :
:
по уравнению на 1 моль Ca(OH)2 ® выделяется 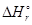 кДж,
кДж,
по условию на 135,1 моль Ca(OH)2 ® выделяется 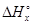 кДж.
кДж.
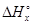 =
= 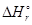 × n(Ca(OH)2)/n(Ca(OH)2) = -65,3×135,1 = -8822 кДж.
× n(Ca(OH)2)/n(Ca(OH)2) = -65,3×135,1 = -8822 кДж.
Ответ. Выделится 8822 кДж теплоты.
Задача 3. При получении железа в доменной печи протекает процесс:
Fe2O3 (Т) + 3CO(Г) = 2Fe(Т) + 3CO2 (Г).
Рассчитайте, какая масса железа образуется и какой объем углекислого газа выделится (при н.у.), если в процессе выделилось 1000 кДж теплоты.
Решение. Из условия следует, что 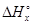 = -1000 кДж, т. к. реакция экзотермическая и теплота выделяется.
= -1000 кДж, т. к. реакция экзотермическая и теплота выделяется.
Рассчитаем по табличным данным энтальпию реакции DH0r:
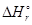 = 3
= 3 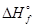 (CO2 (Г)) -
(CO2 (Г)) - 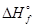 (Fe2O3 (Т)) - 3
(Fe2O3 (Т)) - 3 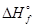 (CO(Г)) =
(CO(Г)) =
= 3(-393,5) – (-821,3) – 3(-110,5) = -27,7 кДж.
Составим пропорцию (5):
по уравнению на 2 моль Fe ® выделяется 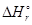 кДж,
кДж,
по условию на n моль Fe ® выделяется 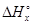 кДж.
кДж.
Вычислив по пропорции n(Fe), получаем:
n(Fe) = DH0x × n(Fe) / 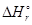 = (-1000 × 2)/(-27,7) = 72,2 моль.
= (-1000 × 2)/(-27,7) = 72,2 моль.
Теперь найдем массу железа по соотношению:
m(Fe) = n(Fe) × M(Fe) = 72,2 × 56 = 4043 г = 4,043 кг.
Аналогично по пропорции (5) вычислим количество CO2:
n(CO2) = DH0x ×n(CO2) / DH0r = (-1000)×3/(-27,7) = 108,3 моль.
Можно составить и другую пропорцию:
по уравнению на n(Fe) =2 моль ® n(CO2) = 3 моль,
по условию на n(Fe) = 72,2моль ® n(CO2) моль.
n(CO2) = 72,2 × 3/2 = 108,3 моль.
Объем газа при н.у. находим умножением количества вещества на молярный объем:
V0(CO2) = n(CO2) × VмО = 108,3 × 22,4 = 2426 л.
Ответ. m(Fe) = 4043 г, V0(CO2) = 2426 л.
Задача 4. При сгорании 100 г C2H5OH(ж) выделилось 2680 кДж теплоты и образовались газообразные CO2 и H2O. Напишите термохимическое уравнение.
Решение. Написать термохимическое уравнение - значит составить уравнение химической реакции и указать соответствующий именно этому уравнению тепловой эффект. Данная задача не предполагает использование справочных данных, можно обойтись и без них.
Запишем уравнение реакции и расставим коэффициенты:
C2H5OH(ж) + 3O2 (г) = 2CO2 (г) + 3H2O(г).
По условию задачи при взаимодействии определенной порции вещества выделилось некоторое количество теплоты, т. е. 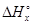 = -2680 кДж.
= -2680 кДж.
Найдем количество вступившего в реакцию вещества:
n(C2H5OH) = m(C2H5OH)/ M(C2H5OH) = 100/46 = 2,17 моль.
Рассчитаем по пропорции (5) энтальпию данной реакции:
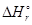 =
= 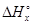 ×n(C2H5OH)/n(C2H5OH)=(-2680)×1/2,17 = 1235 кДж.
×n(C2H5OH)/n(C2H5OH)=(-2680)×1/2,17 = 1235 кДж.
Ответ. Термохимическое уравнение запишется так:
C2H5OH(ж)+3O2(г) = 2CO2(г)+3H2O(г), 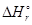 =-1235 кДж.
=-1235 кДж.
III. ЭНТАЛЬПИИ ОБРАЗОВАНИЯ ВЕЩЕСТВ
|
|
Дата добавления: 2015-05-09; Просмотров: 2538; Нарушение авторских прав?; Мы поможем в написании вашей работы!