
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Строение комплексных соединений
|
|
|
|
1. В молекулах любого комплексного соединения один из атомов или ионов занимает пространственно центральное место и называется «центральный ион» или «ион-комплексообразователь».
Чаще всего это d – элементы (Ag+, Hg2+, Cr3+, Mn4+, …).
Реже р – элементы (В3+, Sn4+, As5+, Te6+, J7+, …).
Для s – элементов комплексообразующая способность мало характерна и подобные соединения существуют в основном в растворе.
Из отрицательно заряженных элементов - комплексообразователей следует отметить прежде всего N-3, S-2, J-.
2. Вокруг центрального иона в некоторой близости расположено определённое число ионов с противоположным зарядом или нейтральных молекул. Эти частицы непосредственно присоединяются к центральному иону и называются «лиганды» или «адденды».
Это могут быть:
а) нейтральные молекулы: H2O, NH3, CO, NO;
б) ионы с зарядом -1: OH -, F -, CN -, CNS -, NO2-;
в) ионы с зарядом -2: SO42-, CO32-, S2O32-, C2O42-.
3. Центральный ион и лиганды образуют «внутреннюю координационную сферу» (или «комплексный ион»); ионы, не вошедшие туда, называются «внешняя сфера».
Например: 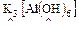
внешняя внутренняя
сфера координационная сфера
4. Ёмкость внутренней сферы ограничена и характеризуется «координационным числом». Координационное число зависит от заряда и радиуса центрального иона, иногда от размера лигандов и может быть различным для некоторых элементов. В зависимости от того, сколько пар электронов может отдать лиганд на связь с центральным атомом и соответственно сколько координационных мест он занимает, лиганды бывают:
а) «монодентатные» - занимают одно координационное место; это или нейтральные молекулы (H2O, NH3, CO, NO);
или ионы с зарядом -1: (OH -, F -, CN -,…).
б) «бидентатные» - занимают два координационных места (SO42-, CO32-,…);
|
|
|
в) «полидентатные» - занимают три и более координационных места (комплексоны ЭДТУ, ЭДТА, …).
Как правило, определённые значения координационных чисел связаны с геометрической конфигурацией комплексного иона:
координационное число = 2 (Ag+, Cu+) – линейное строение;
координационное число = 3 (Mg2+) – плоский треугольник;
координационное число = 4 (Cu2+, В3+, Zn2+) – тетраэдр;
координационное число = 6 (Fe2+, Fe3+, Al3+, Cr3+, Mn4+, Sb5+) – октаэдр.
Реже встречаются комплексы со значениями координационного числа = 8 (Ca2+, Mg2+,…) и координационного числа = 12 (K+, Rb+, …).
Классификация комплексных соединений
1. По природе лигандов и центрального иона:
а) неорганические - 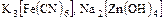 ;
;
б) органические -  ;
;
в) смешанные - 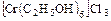 .
.
2. По заряду комплексного иона:
а) катионные - 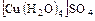 ;
;
б) анионные -  ;
;
в) нейтральные - 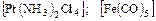 .
.
3. По аналогии с основными классами соединений:
а) комплексные кислоты - 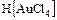 ;
;
б) основания - 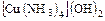 ;
;
в) соли -  .
.
4. По природе лиганда:
а) гидроксокомплексы - 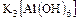 ;
;
б) аквакомплексы - 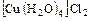 ;
;
в) аммиакаты - 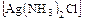 ;
;
г) ацидокомплексы (лигандами являются остатки кислот) - 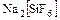 ,
, 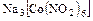 .
.
5. По внутренней структуре комплексных соединений:
а) моноядерные - 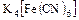 ;
;
б) полиядерные - 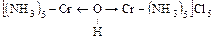
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 529; Нарушение авторских прав?; Мы поможем в написании вашей работы!