
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Мочи по методу Мальфатти
|
|
|
|
Определение титруемой кислотности и аммиака
Реакция рН
Основные симптомы ОПН и ХПН
| Симптомы | Формы почечной недостаточности | |
| острая | хроническая | |
| Изменение диуреза | олигурия, анурия | полиурия |
| Внешний вид мочи | мутная, темно-бурая, или кровянистая | бесцветная, прозрачная |
| Протеинурия | часто высокая | минимальная или умеренная |
| Гемоглобинурия | часто | не характерна |
| Миоглобинурия | часто | не характерна |
| Относительная плотность мочи | снижена | резко снижена |
| Артериальное давление | норма или снижено | повышенное |
| Размеры почек | в пределах нормы | уменьшены |
ЛАБОРАТОРНАЯ РАБОТА
Цель работы: студент должен изучить и знать механизм образования мочи, химический состав мочи здорового человека, патологические компоненты мочи; уметь определить в моче ацетон, кровь, желчные пигменты, уробилин, индикан, глюкозу, белок.
1. Качественное определение реакции с помощью индикатора бромтимолового синего.
Принцип: метод основан на свойствах индикатора имеющего зону перехода окраски в диапазоне рН 6,0 – 7,6.
Подготовка раствора индикатора: 0,1 г тонко растертого бромтимолового синего растворяют в 20 мл теплого этилового спирта. После охлаждения раствор доводят водой до объема 100 мл.
Ход работы. К 2 –3 мл мочи (через 2 –3 часа после мочеиспускания) добавляют 1 –2 капли раствора индикатора. Желтым цветом характеризуется кислая реакция, бурым слабокислая, травянистым нейтральная, буровато – зеленым слабощелочная, синим – щелочная.
2. Определяем с помощью индикаторной бумаги (качественно).
3. Количественное определение титруемой кислотности мочи и аммонийного азота.
Принцип метода. Под титруемой кислотностью мочи понимается общее количество кислот в моче, определяемое титрованием щелочью в присутствии индикатора фенолфталеина.
|
|
|
Кислотность мочи зависит, главным образом, от количества однозамещенных фосфатов (типа NaH2PO4) и различных органических кислот, выводимых с мочой. Она является одним из показателей кислотно-щелочного равновесия организма. Обычно титруемая кислотность мочи определяется наряду с количеством аммиака, находящегося в связи с остатками различных кислот (соли аммония) и, таким образом, характеризующего количество нейтрализованных кислот в моче.
Определение аммиака основано на связывании солей аммония с формалином в виде гексаметилентетраамина, освобождающиеся при этом кислоты титруют щелочью.
Ход работы. Титруемую кислотность и аммиак определяют в одной пробе.
В колбу помещают 10 мл мочи и 10 мл воды, добавляют 2-3 капли фенолфталеина и титруют 0,1Н раствором NaOH до розовой окраски. Отмечают количество ушедшего на титрование раствора щелочи - оно соответствует титруемой кислотности мочи (а). Далее в колбу добавляют 3 мл раствора формалина (окраска исчезает). Титруют снова 0,1Н раствором щелочи до появления стойкого розового окрашивания. Результат второго титрования указывает на количество аммиака (в).
Расчет: Титруемую кислотность мочи обычно пересчитываю на соляную кислоту. Расчет титруемой кислотности проводят по формуле: 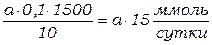 ,
,
где а - количество раствора NaOH, прошедшего на первое титрование, 0,1 - нормальность раствора NaOH, 1500 - суточный диурез, 10 - количество мочи в пробе. В норметитруемая кислотность 27,5 - 63 ммолъ/сутки.
Расчет аммиаказа сутки: 
Суточное выведение аммиака колеблется от 30 до 53 ммолей.
|
|
|
|
|
Дата добавления: 2015-07-02; Просмотров: 807; Нарушение авторских прав?; Мы поможем в написании вашей работы!