
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Оксиды марганца(6,7) их гидроксиды и свойства этих соединений
|
|
|
|
Соединения марганца. Оксиды, гидроксиды.
Марганец образует несколько оксидов. Наиболее устойчивыми являются
+2 +3 +4 + 7
МnО Мn2O3 МnO2 Мn2O7
Оксид марганца (VII) Mn2O7 – маслянистая жидкость черно-зеленого цвета, выше 50°С разлагается с образованием кислорода и низших оксидов, при более высокой температуре взрывается:
2Mn2O7 = 4MnO2 + 3O2.
Проявляет кислотные свойства. Реагирует с водой, образуя марганцовую кислоту:
Mn2O7 + H2O = 2HMnO4.
Оксид марганца можно получить только косвенным путем:
2KMnO4 + H2SO4 = Mn2O7 + K2SO4 + H2O.
Марганцовая кислота – сильная кислота, очень неустойчивая, разлагается уже выше 3°С:
4HMnO4 = 4MnO2 + 2H2O + 3O2.
Манганат калия. Соединения марганца (VI) малоустойчивы, однако наиболее известное соединение — манганат калияK2MnО4 — устойчив в щелочной среде. Он образуется при восстановлении перманганата калия в щелочной среде, например:

Вообще для Mn6+ характерны следующие продукты окислительно-восстановительных реакций:
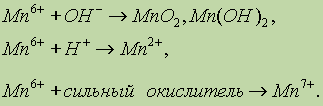
Например: 
Перманганат калия. Высшую степень окисления 7+ марганец имеет в кислотном оксиде Мn2О7 и перманганате калия КмnO4. Последнее вещество — кристаллы фиолетового цвета, хорошо растворимые в воде.
Перманганат калия — сильнейший окислитель. В кислой среде он восстанавливается до ионов Мn2+:
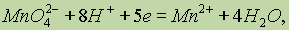
в щелочной среде — до К2МnO4 (см. выше), а в нейтральной среде — до MnO2:
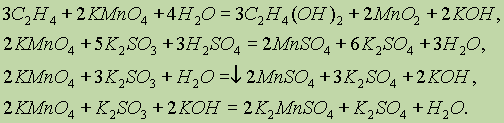
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 2318; Нарушение авторских прав?; Мы поможем в написании вашей работы!