
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Разница между сильными и слабыми электролитами
|
|
|
|
Сильные электролиты – вещества, которые в растворе диссоциируют нацело (например, соли).
К3РО4 = 3К+ + РО43-
Т.е. в растворе молекул К3РО4 нет.
Слабые электролиты – вещества, которые в растворе диссоциируют ступенчато.
Н3РО4 = Н+ + Н2РО4-
Н2РО4- = Н+ + НРО42-
НРО42- = Н+ + РО43-
Равновесия, существующие в растворах слабых электролитов, выражаются константами равновесия, которые называются константами диссоциации.
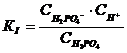
Константы диссоциации имеются в таблицах. Для солей констант диссоциации не существует, так как реакция диссоциации в случае солей необратимая.
Равновесия подчиняются закону Ле-Шателье и зависят:
1) от природы веществ;
2) от концентрации;
3) температуры.
Билет №26
Буферные системы, буферные растворы, буферные смеси, системы, поддерживающие определённуюконцентрацию ионов водорода Н+, то есть определённую кислотность среды. Кислотность буферных растворовпочти не изменяется при их разбавлении или при добавлении к ним некоторых количеств кислот или оснований.

|
Примером буферной системы служит смесь растворов уксусной кислоты CH3COOH и её натриевой солиCH3COONa. Эта соль как сильный электролит диссоциирует практически нацело, т. е. даёт много ионов CH3COO-. При добавлении к буферной системе сильной кислоты, дающей много ионов Н+, эти ионы связываются ионамиCH3COO- и образуют слабую (то есть мало диссоциирующую) уксусную кислоту:
Наоборот, при подщелачивании буферной системы, то есть при добавлении сильного основания (например, NaOH), ионы OH- связываются Н+-ионами, имеющимися в буферной системе благодаря диссоциации уксусной кислоты; при этом образуется очень слабый электролит — вода:

|
По мере расходования Н+-ионов на связывание ионов OH- диссоциируют всё новые и новые молекулы CH3COOH, так что равновесие (1) смещается влево. В результате, как в случае добавления Н+-ионов, так и в случае добавления ОН--ионов, эти ионы связываются и потому кислотность раствора практически не меняется.
|
|
|
Кислотность растворов принято выражать так называемым водородным показателем pH (для нейтральныхрастворов pH=7, для кислых — pH меньше, а для щелочных — больше 7). Приливание к 1 л чистой воды 100 мл 0,01 молярного раствора HCl (0,01 М) изменяет pH от 7 до 3. Приливание того же раствора к 1 л буферной системы CH3COOH + CH3COONa (0,1 М) изменит pH от 4,7 до 4,65, то есть всего на 0,05. В присутствии 100 мл 0,01 Мраствора NaOH в чистой воде pH изменится от 7 до 11, а в указанной буферной системе лишь от 4,7 до 4,8. Кроме рассмотренного, имеются многочисленные другие буферные системы (примеры см. в табл.). Кислотность (и, следовательно, pH) буферной системы зависит от природы компонентов, их концентрации, а для некоторых буферных систем и от температуры. Для каждой буферной системы pH остаётся примерно постоянным лишь до определённого предела, зависящего от концентрации компонентов.
Примеры буферных систем
| Компоненты (концентрации по 0,1 г мол/л) | pH (при 15—250C) |
| Уксусная кислота + ацетат натрия, CH3COOH + CH3COONa | 4,7 |
| Лимоннокислый натрий (двузамещеный), C6H6O7Na2 | 5,0 |
| Борная кислота + бура, Н3ВО3 + Na2B4O7 10H2O | 8,5 |
| Борная кислота + едкий натр, Н3ВО3 + NaOH. | 9,2 |
| Фосфат натрия (двузамещеный)+ + едкий натр, Na2HPO4 + NaOH | 11,5 |
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 870; Нарушение авторских прав?; Мы поможем в написании вашей работы!