
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Сульфохлорирование и сульфоокисление.
При обычной температуре серная кислота на алканы не действует; при нагревании действует как окислитель. Дымящая серная кислота при взаимодействии с алканами дает сульфокислоты:

Однако легче протекает сульфохлорирование

алкансульфолорид
и сульфоокисление

алкансульфокислота
3. Нитрование – реакция замещения атомов водорода на нитрогруппу:

Этот процесс известен как реакция Коновалова, осуществляется при температуре 110 – 140ºС с использованием разбавленной азотной кислоты и характеризуется достаточно высокой региоселективностью. Нитрование алканов – радикальный процесс:


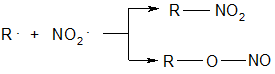 (эфиры азотистой кислоты)
(эфиры азотистой кислоты)
4. Окисление. Алканы являются одними из самых трудно окисляемых органических соединений. Кислород воздуха и обычные окислители (KMnO4, K2CrO4, K2Cr2О7 и др.) окисляют алканы только при высоких температурах с разрывом углеродной цепи и образованием преимущественно кислот. При этом в значительных количествах образуется конечный продукт окисления СО2.
Например, окислением бутана в промышленности получают уксусную кислоту:

В процессе окисления предельных углеводородов в качестве промежуточных веществ образуются органические гидропероксиды. При действии высокой температуры на углеводороды возникают свободные радикалы, которые присоединяют молекулярный кислород. Образующийся при этом перекисный радикал отрывает водород от другой молекулы алкана и дает новый радикал и молекулу гидроперекиси:

Дальнейшая судьба гидроперекисей зависит от их строения.
Третичные гидропероксиды распадаются с образованием спиртов или кетонов по схеме:

Направление распада гидроперекиси вторичных алкилов зависит от условий. При низких температурах они дают преимущественно кетоны и спирты:

При высоких температурах образуются преимущественно альдегиды и спирты:

Гидроперекиси первичных алкилов в этих условиях разлагаются также на спирты и альдегиды:

Последующее окисление спиртов и альдегидов приводит к карбоновым кислотам.
|
|
Дата добавления: 2017-02-01; Просмотров: 81; Нарушение авторских прав?; Мы поможем в написании вашей работы!