
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторно-практическое занятие №5
|
|
|
|
Тема: Алифатические углеводороды (алкины, алкадиены)
Цель занятия: 1. Рассмотреть особенности строения алкинов и алкадиенов
2. Изучить физико-химические свойства алкинов и алкадиенов.
3. Провести реакции, подтверждающие строение и свойства
ненасыщенных углеводородов.
Контрольные вопросы:
1. Алкины. Номенклатура, изомерия.
2. Электронное строение ацетилена: sp- гибридизация, σ- и π- связи.
3. Получение алкинов.
4. Физические свойства алкинов.
5. Химические свойства ацетиленовых углеводородов (реакции присоединения, замещения, полимеризации).
6. Алкадиены; классификация, изомерия, номенклатура. Получение диенов.
7. Особенности химического строения алкадиенов с сопряженными связями.
8. Химические свойства сопряженных диенов. Диеновый синтез.
9. Понятие о синтетических каучуках.
§1. Алкины. Номенклатура, изомерия.
Алкины – это ненасыщенные углеводороды, содержащие в цепи тройную связь. Общая формула алкинов СnH2n-2
По номенклатуре ИЮПАК название алкиновобразуют от названия соответствующего алкана с изменением окончания – ан на –ин.
СН ≡ СН этин, ацетилен СН ≡ С – этинил
СН ≡ С – СН3 пропин, метилацетилен СН ≡ С – СН2 – пропаргил
Изомерия:
1) углеродной цепи

1 – пентин, пропилацетилен
 2 – метил – 1 – бутин, изопропилацетилен
2 – метил – 1 – бутин, изопропилацетилен
2) положение тройной связи


1– бутин 2 – бутин
3) межклассовая (изомерны алкадиенам)
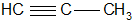

пропин пропадиен
§2. Электронное строение
Атомы углерода тройной связи находятся в sp – гибридизации: две гибридные орбитали лежат в одной плоскости под углом 180º С, две негибридные р – орбитали каждого атома углерода перпендикулярны плоскости гибридных орбиталей и расположены во взаимно перпендикулярных плоскостях.
|
|
|

Длина тройной связи – 0,120нм
Энергия связи – 814 кДж/моль
§3. Получение алкинов
1. Карбидный метод:

2. Ацетилен получают пиролизом этана или этилена:

3. Пиролиз метана:

4. Из дигалогенпроизводных:
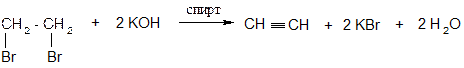


§4. Физические свойства
Ацетилен – газ, без цвета, без запаха, в воде малорастворим в воде, хорошо растворим в ацетоне. Смесь ацетилена с воздухом взрывоопасна
С2 – С4 – газы, без цвета, без запаха
С5 – С16 – жидкости
С17 и выше – кристаллические вещества
Ткип., Тпл.,ρу алкинов выше по сравнению с алканами и алкенами.
§5. Химические свойства ацетиленовых углеводородов
1. Галогенирование.


Раствор брома в воде или в четыреххлористом углероде имеет бурую окраску, продукты присоединения брома бесцветны (качественная реакция на тройную связь).
2. Гидрогалогенирование: присоединение галогенводородов протекает по правилу Марковникова

3. Гидратация (реакция Кучерова):

4. Реакции винилирования

5. Карбонилирование:

6. Кислотные свойства (слабые СН – кислотные свойства):

Взаимодействие ацетиленидов с галогеналкилами (метод получения гомологов ацетилена):

7. Окисление:
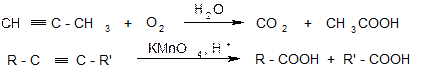
8. Восстановление

9. Полимеризация
а) димеризация

б) тримеризация



§6. Алкадиены; классификация, изомерия, номенклатура. Получение диенов.
Алкадиены – это ненасыщенные углеводороды, содержащие в цепи две двойные связи. Общая формула диенов СnН2n – 2.
По номенклатуре ИЮПАК название алкадиенов образуется от названия соответствующих алканов с изменением окончания – ан на –диен. Цифрами указывают атомы углерода, после которых расположена двойная связь. По взаимному расположению двойных связей диены классифицируют на три типа
• диены с кумулированными связями – двойные связи примыкают к одному атому углерода (1,2 – диены):
|
|
|


• диены с сопряженными связями – двойные связи разделены одной одинарной связью:

• диены с изолированными связями – двойные связи разделены одним и более sp³-гибридными атомами углерода:
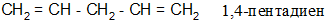

Изомерия:
1) углеродной цепи

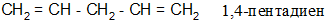
2) положение двойных связей


3) межклассовая (изомерны алкинам)
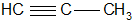

пропин пропадиен
Получение диенов:
1. Из дигалогеналкенов:

2. Термическое превращение этилового спирта (реакция С.В.Лебедева):

3. Дегидратация двухатомных спиртов (метод Реппе):


4. Дегидрирование бутан-бутеновой фракции переработки нефти:

5. Синтез изопрена

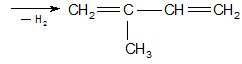
Диеновые углеводороды первых двух типов проявляют своеобразные свойства. Для углеводородов третьего типа характерны обычные реакции алкенов, только в них принимают участие не одна, а обе связи с большей или меньшей селективностью.
§7. Особенности химического строения алкадиенов с сопряженными связями
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 82; Нарушение авторских прав?; Мы поможем в написании вашей работы!