
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Щелочность природных вод
|
|
|
|
Одной из важнейших особенностей большинства природных вод является способность нейтрализовать ионы водорода. Эта способность называется щелочностью воды и определяется экспериментально при титровании пробы воды сильной кислотой, обычно HCl в присутствии фенолфталеина (рН перехода окраски —8,3) и затем метилоранжа (рН перехода окраски —4,5).
Основными компонентами, ответственными за процессы связывания ионов водорода, в большинстве природных вод являются ионы HCO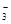 , CO
, CO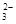 и ОН
и ОН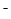 . Другие ионы, источниками которых могут служить органические кислоты, фосфаты, бораты и т. д., вносят лишь незначительный вклад в процессы нейтрализации ионов водорода и начинают играть определенную роль лишь после связывания гидрокарбонат-ионов.
. Другие ионы, источниками которых могут служить органические кислоты, фосфаты, бораты и т. д., вносят лишь незначительный вклад в процессы нейтрализации ионов водорода и начинают играть определенную роль лишь после связывания гидрокарбонат-ионов.
Основные химические реакции, протекающие в водоеме при нейтрализации ионов водорода, можно представить следующими уравнениями:
HCO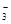 + Н+
+ Н+ 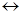 Н2О + СО2
Н2О + СО2
CO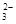 +Н+
+Н+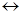 HCO
HCO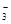
ОН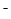 + Н+
+ Н+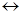 Н2О
Н2О
При экспериментальном определении щелочности на первом этапе (до рН перехода 8,3) связываются все ионы гидроксила, и практически все ионы карбоната переходят в HCO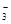 (см. рис. 2.2). Израсходованное при этом количество кислоты соответствует карбонатной щелочности воды. В дальнейшем при титровании пробы (до рН перехода 4,5) связываются практически все гидрокарбонат-ионы (см. рис. 2.2). Поэтому суммарный расход кислоты (израсходованной до рН 4,5) эквивалентен содержанию ионов HCO
(см. рис. 2.2). Израсходованное при этом количество кислоты соответствует карбонатной щелочности воды. В дальнейшем при титровании пробы (до рН перехода 4,5) связываются практически все гидрокарбонат-ионы (см. рис. 2.2). Поэтому суммарный расход кислоты (израсходованной до рН 4,5) эквивалентен содержанию ионов HCO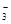 , 2CO
, 2CO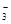 и ОН
и ОН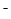 и представляет общую щелочность воды. Таким образом, численное значение щелочности можно определить как сумму концентраций ионов HCO
и представляет общую щелочность воды. Таким образом, численное значение щелочности можно определить как сумму концентраций ионов HCO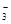 , ОН
, ОН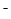 и удвоенной концентрации ионов CO
и удвоенной концентрации ионов CO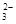 :
:
Щ = [HCO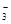 ] + 2[CO
] + 2[CO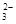 ] + [ОН
] + [ОН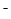 ]
]
где Щ —общая щелочность воды, моль/л.
Если рН водной пробы еще до титрования ниже 4,5, то о такой воде говорят как о воде с нулевой щелочностью.
|
|
|
Необходимо четко представлять себе разницу между основностью и щелочностью раствора. Основность раствора характеризует лишь концентрацию ионов гидроксила в данный момент времени. Щелочность же показывает как бы резервную емкость воды, способность нейтрализовать определенное количество ионов водорода.
Так, например, раствор, содержащий 0,001 моль/л NaOH, будет иметь рН 11 и общую щелочность, равную концентрации ОН-ионов: Щ= 0,001 моль/л. В то же время раствор, содержащий 0,1 моль/л NaHC03, будет иметь более низкое значение рН (рН 8,3), но его щелочность, которая будет определяться в основном концентрацией гидрокарбонат-ионов, будет в 100 раз больше, чем у раствора NaOH с концентрацией 0,001 моль/л.
Величина щелочности природных вод имеет большое значение и с точки зрения фотосинтеза, протекающего в водоемах. В упрощенном виде процесс фотосинтеза может быть представлен следующим образом:
СО2(Р.Р) + Н2О 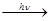 {СН2О} + О2
{СН2О} + О2
HCO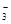 + Н2О
+ Н2О 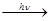 {СН2О} + О2 + ОН
{СН2О} + О2 + ОН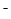
Следовательно, при связывании углерода и синтезе органических соединений в случае отсутствия дополнительного поступления диоксида углерода возрастает рН раствора, а количество синтезируемых органических соединений зависит от содержания СО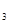 и HCO
и HCO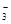 в растворе, или от его щелочности.
в растворе, или от его щелочности.
Иногда в природных водоемах в связи с бурным протеканием процессов фотосинтеза и недостаточной скоростью поступления диоксида углерода рН поднимается до 10 и выше. Такие высокие значения рН, как и закисление, отрицательно сказываются на развитии водных экосистем.
Поскольку, как отмечалось выше, для поверхностных водоемов, находяцщихся в равновесии с карбонатом кальция (кальцитом) и диоксидом углерода, содержащимся в атмосферном воздухе, рН воды должен составлять 7,3-8,4, значение щелочности в этих водоемах будут определяться лишь концентрацией гидрокарбонат-ионов (см. распределительную диаграмму на рис. 2.2). Концентрация HCO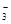 - ионов в таких водоемах, а, следовательно, и щелочность будут равны примерно 1 ммоль/л.
- ионов в таких водоемах, а, следовательно, и щелочность будут равны примерно 1 ммоль/л.
|
|
|
Следует отметить, что при отсутствии процессов растворения или осаждения щелочность воды остается неизменной. При изменении рН средьх происходят лишь взаимные трансформации компонентов карбонатной системы. Поэтому щелочность часто называют «консервативной величиной».
|
|
|
|
Дата добавления: 2013-12-14; Просмотров: 3081; Нарушение авторских прав?; Мы поможем в написании вашей работы!