
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Разбавленные растворы
|
|
|
|
Ввиду очень сложного характера взаимодействия компонентов в растворах, предсказать свойства растворов, исходя из свойств чистых компонентов, невозможно. Поэтому целесообразно сначала рассмотреть идеализированные случаи, в которых можно отделить главные черты явления от второстепенных. В связи с этим в теории растворов рассматриваются два основных типа идеальных растворов: бесконечно разбавленные растворы и совершенные растворы.
Если обозначить индексом 1 растворитель, а индексом i (i = 2, 3, 4 …) растворенное вещество, то разбавленный раствор можно определить как такой, в котором 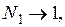 а
а  Особенностью такого раствора является то, что молекулы растворенного вещества отделены друг от друга большим числом молекул растворителя. Поэтому в таком растворе имеет место только взаимодействие между растворенным веществом и растворителем, но не между молекулами растворенного вещества. Вследствие этого, если к разбавленному раствору при постоянной температуре добавлять растворитель, то при происходящем разбавлении раствора с увеличением его объема не будет изменяться ни энергия (U), ни энтальпия (H) системы раствор – растворитель:
Особенностью такого раствора является то, что молекулы растворенного вещества отделены друг от друга большим числом молекул растворителя. Поэтому в таком растворе имеет место только взаимодействие между растворенным веществом и растворителем, но не между молекулами растворенного вещества. Вследствие этого, если к разбавленному раствору при постоянной температуре добавлять растворитель, то при происходящем разбавлении раствора с увеличением его объема не будет изменяться ни энергия (U), ни энтальпия (H) системы раствор – растворитель:

подобно тому, как это имеет место в идеальном газе.
Вообще между веществами в состоянии бесконечно разбавленного раствора и в состоянии идеального газа существует аналогия. Растворенное вещество имеет тенденцию самопроизвольно распространяться в объеме растворителя подобно тому, как газ расширяется в пустоту. Тенденция газа к расширению, мерой которого является давление, описываемой уравнением Клапейрона, т. е. 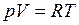 , определяется только увеличением энтропии при расширении, так как внутренняя энергия газа при этом остается постоянной. Подобно этому тенденция растворенного вещества распространяться в объеме раствора также обуславливается лишь увеличением энтропии, поскольку в разбавленном растворе молекулы растворенного вещества не взаимодействуют друг с другом.
, определяется только увеличением энтропии при расширении, так как внутренняя энергия газа при этом остается постоянной. Подобно этому тенденция растворенного вещества распространяться в объеме раствора также обуславливается лишь увеличением энтропии, поскольку в разбавленном растворе молекулы растворенного вещества не взаимодействуют друг с другом.
|
|
|
Процесс разбавления разбавленного раствора аналогичен процессу расширения идеального газа. Эта аналогия заключается в том, что в обоих случаях внутренняя энергия остается постоянной, а вероятность пребывания молекулы в данном объеме пропорциональна объему. Такая аналогия между идеальным газом и разбавленным раствором позволяет найти выражение для химического потенциала растворенного вещества.
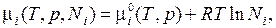
где 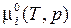 – химический потенциал чистой жидкости при рассматриваемых температуре и давлении.
– химический потенциал чистой жидкости при рассматриваемых температуре и давлении.
Если речь идет об идеальной газовой смеси, тои для химического потенциала i -го компонента используется соотношение
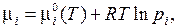
где 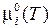 – химический потенциал, равный химическому потенциалу чистого идеального газа i при единичном давлении.
– химический потенциал, равный химическому потенциалу чистого идеального газа i при единичном давлении.
При добавлении молекул растворенного вещества в разбавленный раствор, как отмечалось выше, происходит взаимодействие только между молекулами растворенного вещества и растворителя. Отсюда следует, что добавление каждой новой молекулы растворенного вещества в раствор сопровождается таким же приращением внутренней энергии (или энтальпии), как при введении ее в чистый растворитель.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 921; Нарушение авторских прав?; Мы поможем в написании вашей работы!