
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Интервал перехода окраски индикатора
Запишем схему реакции образования комплексов определяемых катионов М с индикатором (без указания зарядов для общности рассмотрения):
M + Ind = MInd.
Концентрационная константа устойчивости комплекса равна:
β(MInd) = [MInd]/[M][Ind].
В дальнейшем β(MInd) будем записывать просто β.
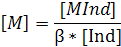

-lg[M]=pM – показатель концентрации катионов металла

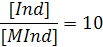
- раствор имеет окраску свободного индикатора
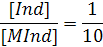
- раствор имеет окраску комплекса MInd
pM = lgβ ± 1
- интервал изменения окраски индикатора.
pM = lgβ
– самый резкий переход окраски
Примеры металлохромных индикаторов.
Известны многие десятки металлохромных индикаторов. Из них при комплексонометрическом анализе фармацевтических препаратов чаще других применяют следующие: кальконкарбоновую кислоту (кальцес), хромовый темно-синий (кислотный хром темно-синий), эриохром черный Т (протравной черный II), ксиленоловый оранжевый, мурексид, пирокатехиновый фиолетовый и некоторые другие.
1) Эриохром черный Т(кислотный хромовый черный специальный) - 1-(1-окси-2-нафтилазо)-6-нитро-2-нафтол-4-сульфокислота. В водном растворе диссоциирует по схеме:

Относится к группе азокрасителей. Является слабой трехосновной
кислотой H3Ind; Ind3-: рК1 = 4; рК2 = 6,4; рК3 = 11,5. В водных растворах, в зависимости от рН, могут доминировать разные формы.
Наиболее контрастным и удобным для фиксации КТТ является переход синий – красный, поэтому титрование ведут при рН ≈ 10 в аммиачном буфере (рН ≈ 9,5—10,0). В этих условиях индикатор образует с катионом металла М2+ комплекс Mind- красного цвета:
HInd2- + M2+ = MInd- + H+
синий красный
Вблизи ТЭ при прибавлении титранта HY3- происходит разрушение этого комплекса под действием титранта:
MInd- + HY3- = HInd2- + MY2-
красный синий
При прямом титрований наблюдается изменение окраски титруемого
раствора из красной (или красно-фиолетовой) на синюю.
Индикатор применяют для определения Mg2+, Sr2+, Ba2+, Zn2+, Cd2+,Pb2+,Mn2+ в аммиачном буфере.
Свободный индикатор — темно-коричневый порошок, малорастворимый в воде.
2) Ксиленоловый оранжевый - 3,3'-бис-[N,N-ди(карбоксиметил)- аминометил]-о-крезосуьфофталеин. Относится к группе трифенилметановых красителей:

Представляет собой шестиосновную кислоту, показатели констант кислотной диссоциации которой равны: рК1 = -1,2; рК2 = 2,6; рК3 = 3,2; рК4 = 6,4; рК5 = 10,4; рК6 = 12,3. Окраска индикатора при 2,0 < рН < 6,4 — желтая, при рН > 6,4 — красно-фиолетовая. С катионами металлов образует комплексы красного цвета. При прямом титровании вблизи ТЭ цвет раствора изменяется из красного на желтый.
Индикатор применяют при определении Cu2+, Mg2+, Ca2+, Zn2+, Cd2+,Hg2+, РЬ2+, Cо2+, Ni2+, Fe3+, Вi3+ и др. катионов металлов.
Свободный индикатор — блестящий красно-коричневый кристаллический порошок хорошо растворяется в воде и в кислых растворах; нерастворим в спирте, эфире.
3) Мурексид - однозамещенная аммонийная соль пурпурной (5,5'-ни-трилодибарбитуровой) кислоты:

Пурпурная кислота — пятиосновная кислота. Показатели констант последовательной ступенчатой кислотной диссоциации равны: рК1 ≈ 1,6; рК2 = 8,7 – 9,2; рК3 = 10,3 – 10,9; рК4 = 13,5; рК5 = 14 – 14,5.
Цвет раствора индикатора зависит от кислотности среды: красно- фиолетовый при рН < 9; фиолетовый при рН = 9,2—10,3; сине-фиолетовый при рН > 10,3. Комплексы катионов металлов с мурексидом окрашены в различный цвет. Например, комплексы Ni2+ — желтого, Сu2+ - желто-оранжевого, Ca2+ — красного, Мn2+ — оранжевого цвета.
Мурексид применяется при комплексонометрическом определении Ag+, Cu2+, Ca2+, Sr2+,Zn2+, Sc2+, Mn2+, Co2+, Ni2+ и др. катионов металлов.
Свободный индикатор — моногидрат C8H8N6O6 • Н2O — пурпурно-красный или красно-коричневый порошок с зеленоватым металлическим блеском малорастворим в воде.
|
Дата добавления: 2014-01-04; Просмотров: 4116; Нарушение авторских прав?; Мы поможем в написании вашей работы!