
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция № 16
|
|
|
|
Техническая биоэнергетика
План:
Введение
1. Получение биогаза биотехнологическими методами:
1.1. Свойства метанобразующих бактерий;
1.2. Технология получения метана.
2. Получение низкомолекулярных спиртов.
3. Получение тепловой энергии при бактериальном окислении.
4. Получение молекулярного водорода.
5. Биотопливные элементы
Введение
Современная энергетика является топливной. Около 98 % производимой в мире и потребляемой энергии дают уголь, нефть и природный газ, и только 2 % — гидроэнергетика и атомная энергетика. Постоянно растущие темпы добычи и потребления ископаемых органических топлив приводят, с одной стороны, к резкому сокращению их запасов и, с другой стороны, к тепловому и углекислотному загрязнению биосферы благодаря выведению в атмосферу дополнительных количеств тепла и СО2. С проблемами современной энергетики тесно смыкается решение задач по проблеме охраны окружающей среды. Необходимо разработать научные методы и технологии получения энергии при одновременном решении вопросов, связанных с защитой окружающей среды от непрерывно поступающих в биосферу загрязнений.
1. Получение биогаза биотехнологическими методами
Получение биогаза, основным компонентом которого (до 80—85 %) является метан - сложный бактериальный процесс, протекающий в анаэробных условиях. В нем участвуют разнообразные по физиолого-биохимическим свойствам микроорганизмы. Венцом таких ассоциаций являются метаногены - древнейшие представители так называемых архебактерий.
1.1. Свойства метанобразующих бактерий
Полагают, что метанобразующие бактерии, или метаногены, возникли около 3,0—3,5 млрд. лет тому назад и достигли своего расцвета в архее.
|
|
|
Сейчас эти микроорганизмы имеют достаточно широкое распространение, приуроченное к анаэробным условиям. Вместе с другими бактериями они активно участвуют в деструкции органических веществ в различных экологических нишах: в болотном, речном и озерном иле, в осадках морей и океанов, в искусственных технических сооружениях — метантенках, в рубце жвачных и пищеварительном тракте ряда других животных.
К настоящему времени удалось выделить в виде чистых культур более двадцати метанобразующих бактерий, причем обнаруживаются все новые виды. Среди этих бактерий есть организмы, клетки которых близки к сферическим, образующие агрегаты, похожие на сарцин, ланцетовидные, палочковидные и нитевидные формы. Большинство неподвижны, но отдельные виды проявляют способность к движению в результате наличия жгутиков.
Как и другие архебактерии, метаногены отличаются от остальных прокариот (эубактерий) составом ряда компонентов клеток, в том числе клеточной стенкой, не содержащей муреина, а также характером липидов, в которые не входят жирные кислоты. Большую часть нейтральных липидов составляют простые эфиры глицерина и длинноцепочечного спирта фитанола.
Все метанобразующие бактерии - строгие анаэробы. Некоторые из них мезофилы, другие, растущие при 60-80°С и более высокой температуре, термофилы. К числу термофилов относится, например, M. thermoautotrophicum. Оптимальное значение рН для роста разных видов 6,5—8,0. Некоторые штаммы способны расти при наличии в среде до 5—7 % и более NaCI.
Как источник серы бактерии чаще всего используют сульфид, а как источник азота — аммоний. Некоторые виды нуждаются для роста в наличии дрожжевого автолизата или смеси витаминов. Известны также метанобразующие бактерии, для роста которых необходимо присутствие ацетата и (или) других органических веществ.
|
|
|
Но довольно многие из этих микроорганизмов могут расти в автотрофных условиях (при наличии в качестве единственного источника углерода углекислоты).
Важная особенность метаногенов — способность активно развиваться в анаэробных условиях в тесном симбиозе с другими группами бактерий, создающими для них благоприятные условия и обеспечивающих необходимыми субстратами для роста и синтеза метана.
1.2. Технология получения метана
Технологически метановое брожение подразделяют на два этапа: созревание метанового биоценоза и ферментацию. В течение первого этапа развиваются бактерии, участвующие в анаэробном разложении исходных органических веществ и продуктов их распада. В результате деятельности этих микроорганизмов создаются оптимальные условия для активного биосинтеза метана.
Несмотря на сложность и далеко неполную изученность, такая биологическая система достаточно надежна и проста для получения биогаза в промышленных масштабах.
Метановое брожение жидких органических веществ осуществляется в строго анаэробных условиях при 30—40 °С (мезофильный процесс) или 52—60 °С (термофильный процесс). Ферментацию проводят в реакторах (метантенках) объемом от одного до нескольких тысяч кубических метров. Метантенки выполняются из железобетона или металла. Они могут иметь разную форму и конструкцию, от кубической до цилиндрической, расположены горизонтально или вертикально. Лучшей признается яйцеобразная конструкция. Ферментация протекает непрерывно, полупериодически и периодически. Схема биогазовых установок для переработки жидких субстратов представлена на рис 1.
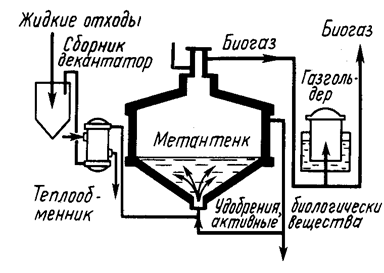 Сырье, содержащее 2—12 % органических веществ, подается в метантенк через теплообменник, где оно подогревается или охлаждается до температуры ферментации в метантенке. Место введения сырья в реактор и отбора сброженной массы зависит от конструкции метантенка.
Сырье, содержащее 2—12 % органических веществ, подается в метантенк через теплообменник, где оно подогревается или охлаждается до температуры ферментации в метантенке. Место введения сырья в реактор и отбора сброженной массы зависит от конструкции метантенка.
Реакторы снабжаются мешалками для перемешивания бродящей массы с целью ускорения процессов и теплообменниками для поддержания необходимой температуры внутри реактора. Образующиеся газы удаляются через газовый колпак, расположенный в верхней части метантенка. Газ, содержащий 50—85 % метана и 15—50 % С02, по газопроводу поступает в газохранилище — газгольдер, откуда подается в газовую сеть.
|
|
|
В последние годы в практику внедряются технологии, основанные на разделении процесса метанового брожения на стадии — фазы: кислотную и метановую. Двухфазный процесс осуществляется в двух реакторах, соединенных последовательно. Скорость поступления сырья и объемы реакторов рассчитываются так, чтобы в первом протекала только стадия образования кислот, значение рН среды не должно быть выше 6,5. Такая бражка подается во второй реактор, в котором с большой скоростью протекает непосредственно образование метана. Двухфазный процесс позволяет увеличить его общую скорость в два-три раза. Иногда в практике при использовании двухфазного процесса с целью дополнительного получения товарного биогаза процесс брожения в первом ферментере проводят при 35—37 °С, во втором — при 55 °С. При нормальных условиях ферментации на каждую тонну сброженного органического вещества образуется до 300—600 м3 биогаза. Процент разложения органических веществ до метана зависит от скорости процесса и времени выдерживания сырья в реакторе, обычно эта величина равна 30—60 %.
Концентрация метана в образующемся биогазе зависит от химического состава субстрата: углеводы дают больше углекислого газа, жиры—больше метана (до 85 %). Чем больше восстановлен субстрат, тем выше концентрация метана.
Метановое брожение — процесс эндотермический, требует постоянного подогрева для поддержания необходимой температуры ферментации. Как правило, метантенки и сырье подогреваются за счет сжигания образующегося биогаза. В среднем на поддержание требуемой температуры ферментации расходуется от 15— 20 % (мезофильный процесс) до 30—50 % (термофильный процесс) биогаза. Поэтому одним из важных моментов эксплуатации метантенков является их хорошая теплоизоляция.
Рассмотренный выше процесс метанового брожения касался использования только жидких субстратов. В последние годы широкое развитие имеет технология твердофазной метангенерации, или получение биогаза, при деструкции органических веществ с влажностью 30—40 %. Такие процессы уже имеют практическое применение в США и некоторых странах Западной Европы, например, при переработке городского твердого мусора. Основное условие такого процесса — анаэробиоз и необходимая влажность.
|
|
|
Биогаз кроме метана и углекислого газа может содержать примеси сероводорода (до 2%), что требует его соответствующей очистки.
Теплотворная способность биогаза составляет 5—7 ккал/м3 и зависит от концентрации в нем СОг. Один кубический метр биогаза эквивалентен 4 кВт/ч электроэнергии, 0,62 л керосина, 1,5 кг угля, 3,5 кг дров, 0,43 кг бутана. Он может быть использован для получения тепловой энергии, электроэнергии, заменить моторное топливо. Из биогаза можно получить «синтез-газ» (смесь угарного газа и молекулярного водорода), из которого синтезируют метанол, или искусственный бензин.
Образующийся в процессе метанового брожения шлам (жидкий или твердый) является хорошим органо-минеральным удобрением. Он может также использоваться для производства ценных биологически активных соединений, применяемых в медицине и сельском хозяйстве.
Перечисленные выше физические особенности биогаза и относительная простота его получения, возможность использования в качестве сырья для его производства разнообразных отходов положительным образом отразились на создании и развитии биогазовой промышленности в ряде стран. Китайская Народная Республика в 1983 г. имела до 7 млн. биогазовых установок семейного типа с общим объемом реакторов около 60 млн. м3. Эти установки позволяют производить в год до 110 млрд. м3 биогаза, заменить до 60—80 млн. т сырой нефти и обеспечить топливом до 30 млн. крестьян КНР.
В странах Европейского экономического сообщества действовало 570 установок, использующих жидкие отходы, и 17 установок, перерабатывающих в биогаз твердый мусор. В США широкое развитие получает производство биогаза при переработке городского твердого мусора. Например, в пригородах Нью-Йорка действует станция, производящая в год 100 млн. м3 биогаза. В нашей стране метановое брожение широко применяется в системе биологической очистки городских сточных вод на станциях аэрации. В метантенках сбраживают осадки сточных вод и активный ил, образующийся в аэротенках. Две станции, обслуживающие город с населением 8 млн. человек, дают в год 110 млн. м3 биогаза. Термофильное метановое брожение отходов микробиологической промышленности используют в нашей стране для производства биогаза и кормового препарата витамина В12. Два цеха, перерабатывающие жидкие стоки ацетоно-бутиловой промышленности, производят в год до 7 млн. м3 биогаза и до 1 т витамина В12.
2. Получение низкомолекулярных спиртов
Возможность широкого использования низших спиртов: метанола, этанола, бутанола, бутандиола, а также ацетона и других растворителей — в качестве моторного топлива для двигателей внутреннего сгорания и дизельных двигателей вновь вызвала большой интерес к получению перечисленных соединений биоконверсией из растительной биомассы.
Смесь этилового или метилового спиртов с бензином в отношении 10:90 или 20:80 под коммерческим названием «газохол» уже широко применяется в ряде стран для автомобильного транспорта.
В свете вышесказанного стоит конкретная задача по разработке конкурентоспособной промышленной технологии производства этанола для технических целей методами биоконверсии. Метиловый спирт предполагается производить из биомассы методом термохимической конверсии. Бутанол и бутандиол — хорошие заменители мазута, их также необходимо добавлять в качестве присадок к спиртово-бензиновым смесям для лучшего смешивания спиртов и углеводородов.
Микробиологическое получение этилового, бутилового спиртов и бутандиола из углеводов достаточно хорошо изучено и имеет многолетний промышленный опыт.
Этиловый спирт обычно получают из гексоз с помощью брожения, вызываемого дрожжами:
С6Н12О6à2CH3CH2OH+2CO2
В качестве сырья используются меласса (отходы сахарного производства), зерновой, картофельный, кукурузный крахмал, который предварительно осахаривается.
Этиловый спирт образуют также в большом количестве бактерии, например из рода Zymomonas (Z. mobilis, Z. anaerobica), Sarcina ventriculi и Erwinia amylovora.. Среди продуцентов этанола имеются и клостридии, к их числу относятся Clostridium thermocellum и Cl. thermohydrosulphuricum. В последнее время эти микроорганизмы интенсивно изучают, так как некоторые из них способны использовать в качестве сбраживаемого субстрата не только крахмал, но такой непищевой и дешевый продукт, как целлюлоза. Бутиловый спирт и ацетон в промышленности также получают с помощью клостридии.
Использование этанола и бутанола как моторных топлив требует их промышленного производства в объеме десятков миллионов тонн. Первая задача, которую необходимо решать в связи с поставленной целью, — это выбор непищевого, дешевого, массового и легко конвертируемого сырья.
В некоторых странах (например, в Бразилии) для производства технического этанола используют отходы сахарного тростника — багассу, в других странах — маниок, батат, сладкое сорго, топинамбур (земляная груша). Указанные культуры являются представителями южных растений. Для стран с умеренным климатом и.обладающими большими лесными массивами дешевым сырьем для крупнотоннажного производства спиртов служит древесина.
Древесина может использоваться как сырье при условии разрушения структурных связей лигнина с целлюлозой и гидролизом последней до гексоз, т. е. требуется определенная химическая или биохимическая предобработка. Это сдерживает широкое использование древесины для получения спиртов, хотя в ряде стран, в первую очередь в Советском Союзе, в течение многих лет существует промышленное производство этилового спирта путем брожения гидролизатов древесины. Такой способ основан на кислотном или щелочном гидролизе древесины до гексоз, которые далее сбраживаются дрожжами до этанола. Но такая технология достаточно энергоемкая и требует использования коррозионно-устойчивого оборудования (основное препятствие ее широкого использования в практике).
Для возможного применения древесины в целях получения биопродуктов в настоящее время интенсивно разрабатываются различные технологии деструкции лигноцеллюлоз: механические (размалывание), физические (гамма-облучение), физико-химические (паровой взрыв, или парокрекинг), химические (гидролиз), биологические (ферментативный гидролиз) и различные комбинации перечисленных методов. К наиболее перспективным следует отнести сочетание «парокрекинга» с ферментативным гидролизом — это предварительная обработка лигноцеллюлоз или гемицеллюлоз паром при высокой температуре и высоком давлении, при котором происходит взрыв кристаллических структур указанных субстратов и отделение лигнина от целлюлозы с последующим гидролизом клетчатки целлюлозолитическими ферментами. К растительным материалам, используемым для гидролитического получения сахара с последующей их биоконверсией в спирты, относят различные виды отходов лесопиления и деревообработки, сельскохозяйственного производства (солома, хлопчатник, кукурузная кочерыжка, подсолнечная лузга, костра льна, конопли, кенафа), тростник, малоразложившийся торф.
Из одной тонны древесины можно получить до 170—180 л этанола и 40 кг биомассы дрожжей, из тонны картофеля — 100 л этанола, из тонны зерна ржи—до 270 л этилового спирта. Большие перспективы для использования целлюлозы в качестве сырья для получения самых разных продуктов открывает ферментативный гидролиз, осуществляемый комплексами целлюлаз и гемицеллюлаз, продуцируемых некоторыми грибами и бактериями. Гидролиз протекает при 40—60 °С и рН 4,0—7,0, не требует больших энергозатрат и коррозионностойкого оборудования. Перспективы использования лигноцеллюлозы для получения этанола и других спиртов, а также иных органических соединений открывают широкие возможности не только для производства моторных топлив, но и для создания важной сырьевой базы для промышленного органо-химического синтеза, например для получения искусственного каучука по методу Лебедева.
3. Получение тепловой энергии при бактериальном окислении
Несколько в стороне от вышеописанных методов анаэробной биоконверсии биомассы в топливе стоит еще один микробиологический процесс получения энергии — аэробное окисление твердой биомассы (отходов) с выделением больших количеств тепла.
Твердое органическое сырье погружается в шахту, снизу подается воздух. В результате окислительных процессов, осуществляемых микроорганизмами, происходит интенсивное выделение тепловой энергии и проходящие газы нагреваются до 80 °С. С помощью компрессии температуру газов можно увеличить до 100—110 °С и получаемую энергию аккумулировать в виде горячей воды или пара. Коэффициент полезного действия установок с учетом затрат электроэнергии на эксплуатацию воздуходувок составляет 95 %. Такие установки промышленного типа работают в Японии. Образующийся шлам используется в качестве высокоэффективного органо-минерального удобрения.
4. Получение молекулярного водорода
Молекулярный водород считается наиболее перспективным видом топлива. По энергоемкости (в расчете на единицу массы) он превосходит все другие соединения, которые можно использовать в этих целях. Сжигание молекулярного водорода не сопровождается загрязнением среды большим количеством вредных веществ и, более того, ведет к регенерации воды. Водород может храниться, транспортироваться и легко преобразуется в электроэнергию с помощью топливных элементов.
К числу хемотрофов, образующих в значительном количестве молекулярный водород, относится, прежде всего, ряд облигатных и факультативных анаэробных бактерий. Кроме того, Н2 выделяют некоторые простейшие (главным образом из числа трипанозом), растущие в анаэробных условиях. Показана также возможность образования молекулярного водорода азотфиксирующими аэробами, например азотобактером.
В наибольшем количестве молекулярный водород выделяют бактерии, осуществляющие брожение разных органических веществ, но чаще всего углеводов.
К числу наиболее активных продуцентов Н2 относятся отдельные виды клостридий (например, Clostridium butyricum, C. рerfringens), энергобактерий (Escherichia coli, Citrobacter freundii), Ruminococcus и некоторых других родов.
Из фототрофных организмов способность к выделению Н2 проявляют многие пурпурные бактерии, цианобактерии и ряд водорослей. Среди последних есть не только микро-, но и макроформы. Есть данные о выделении в небольшом количестве Н2 и высшими растениями.
Пурпурные бактерии осуществляют так называемый аноксигенный фотосинтез (фотосинтез без выделения молекулярного кислорода). Объясняется это тем, что они не могут использовать воду при фотоассимиляции СО2 и в других конструктивных процессах в качестве исходного донора электронов; такую функцию у них выполняют сульфид, сера, тиосульфат, органические вещества или Н2.
Анаэробное окисление многими пурпурными бактериями органических веществ и неорганических соединений серы в определенных условиях ведет к образованию ими Н2. Особенно в большом количестве эти микроорганизмы выделяют молекулярный водород в присутствии света. Поэтому данный процесс часто называют фотовыделением водорода. В отличие от образования Н2 при брожении фотовыделение Н2 пурпурными бактериями катализирует обычно не гидрогеназа, а нитрогеназа — фермент, главная функция которого заключается в превращении N2 в аммиак. Но даже при наличии N2 часть электронов, поступающих к нитрогеназе, расходуется на восстановление протонов, что ведет к выделению Н2.
Среди цианобактерий также обнаружены штаммы, выделяющие при наличии света Н2 в довольно большом количестве и со значительной скоростью (30—40 мл ч-1*г-1 сухой биомассы). К таким организмам относятся в основном нитчатые формы, образующие особые клетки — гетероцисты (например, Anabaena cylindrica, A. variabilis, Mastigocladus thermophilus, M. laminosus).
Выделение Н2 чаще всего отмечается у суспензий клеток, причем может продолжаться 30 сут и более. Такую же способность проявляют иммобилизованные клетки микроорганизмов. В отличие от пурпурных бактерий для образования Н2 цианобактериями не требуется каких-либо экзогенных доноров электронов, кроме воды. Важно также, что нитчатые формы бактерий, образующие гетероцисты, и некоторые одноклеточные виды способны выделять Н2 не только в анаэробных, но и в аэробных условиях.
Более перспективны в данном отношении цианобактерии, поскольку выделение ими Н2 связано с биофотолизом воды, которая пока остается наиболее дешевым и доступным субстратом. Не прекращаются работы и с водорослями, так как они также способны выделять Н2 при разложении воды. Предлагается, кроме того, использовать комплексные системы, образующие Н2, в которые входят разные фототрофы или фототрофы и хемотрофы.
Показана также принципиальная возможность получения Н2 из воды с помощью хлоропластов при добавлении к ним гидрогеназы и некоторых других компонентов, хотя скорость выделения водорода и стабильность такой системы невелики. Но исследование образования Н2 подобными модельными системами может помочь созданию аналогичных искусственных катализаторов для преобразования солнечной энергии в молекулярный водород.
Таким образом, хотя микробиологический способ получения молекулярного водорода еще не реализован, но работы в данном направлении развиваются и аспекты исследований водородобразующих видов микроорганизмов достаточно широки.
5. Биотопливные элементы
На уровне поисковых разработок находятся биотопливные элементы, превращающие химическую энергию субстрата в электрическую. Примерами могут служить топливные элементы на основе окисления метанола в муравьиную кислоту с участием алкогольдегидрогеназы, муравьиной кислоты в СО2 с участием формиатдегидрогеназы, глюкозы в глюконовую кислоту с участием глюкозооксидазы. Используют также каталитическую активность целых клеток, например Е. coli, Bac. subtilis, Ps. aeruginosa, в реакции окисления глюкозы.
Окисление субстрата происходит на электроде (аноде). Посредником между субстратом и анодом является биокатализатор. Существуют два пути дальнейшей передачи электронов на электрод: 1) с участием медиатора и 2) непосредственный транспорт электронов на электрод. Конструкция биотопливного элемента позволяет генерировать не только электрический ток, но и осуществлять важные химические превращения. Например, топливный элемент с глюкозооксидазой и ß-D-фруктофуранидазой переводит сахарозу в смесь фруктозы и глюконовой кислоты.
Ферментные электроды применяются не только в топливных элементах. Они представляют собой основной компонент биологических датчиков — биосенсоров, широко применяемых в химической промышленности, медицине, при контроле за биотехнологическими процессами, в аналитических целях и т. д. Обычно используют системы с биокатализатором, иммобилизованным на поверхности мембранного электрода. Например, иммобилизацией пенициллиназы на обычном рН-электроде получают чувствительный биосенсор, регистрирующий концентрацию пенициллина (S.O. Enfors, N. Cleand, 1983). Иммобилизация клеток Е. coli на кислородном электроде дает биосенсор для измерения концентрации глутаминовой кислоты, а иммобилизация клеток Nitrosomonas sp. и Nitrobacter sp.. на том же электроде — биосенсор на NH4. На биосенсоре протекают следующие превращения:
NН4+ Nitrosomonas NO2- Nitrobacter NO3-
Разработаны биосенсоры для быстрой регистрации концентрации глюкозы в крови больного, что особенно важно при диагностике диабета.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2263; Нарушение авторских прав?; Мы поможем в написании вашей работы!