
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кс и Кр -константа равновесия
|
|
|
|

Связь между Кр и Кс:
p v = n RT 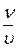 =c p= cRT
=c p= cRT
Кр = 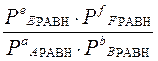 =
= 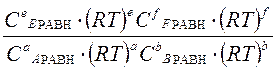
=
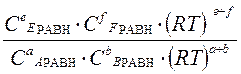
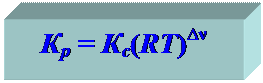 |
∆ν =(e+f) – (a + b) – изменение числа молей газов в результате реакции,
R = 0,082 атм.л.моль-1.К-1
Выражение Кр - через равновесные количества молей газообразных компонентов ni( равн) и общее давление P 0:
Парциальное давление - pi = 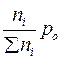
Кр =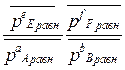 =
=
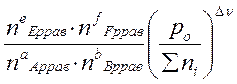
Σni = nE равн + nF равн + nA равн + nB равн
● ∆ rG0Т = - RT ln Кр - для реакций в газовых системах
● ∆ rG0Т =- RT ln Кс - для реакций в конденсированных системах.
Кр и Кс - характеризуют выход продуктов реакции.
Кр и Кс не зависят от:
● парциальных давлений
· концентраций компонентов
· общего давления в системе
но зависят от Т.

∆ rG0Т = - RT ln Кр = ∆ rH0 - T ∆ rS0
ln Kp = -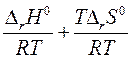 =
=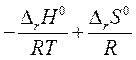
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 7662; Нарушение авторских прав?; Мы поможем в написании вашей работы!