
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Коррозионные свойства тория
|
|
|
|
В сухой и даже влажной атмосфере воздуха при комнатной температуре торий ведет себя как устойчивый к коррозии металл. Коррозия металла становится заметной с повышением температуры (табл. 3).
Окисление кислородом до 3500С идет медленно. По–видимому на поверхности образуется плотная пленка оксида. При повышении температуры наблюдается растрескивание пленки, а выше 4500С происходит саморазогрев металла. При 11000С скорость окисления вновь падает – повидимому из - за спекания оксида на поверхности металла. До 14000С не наблюдается растворимости кислорода в тории.
Таблица 3. Скорость коррозии холоднокатанного тория на воздухе
| Температура, 0С | ||||||||
| Привес, мг/ см2ч | 0,0026 | 0,016 | 0,10 | 0,17 | 0,36 | 4,0 | 15,1 | 33,1 |
При взаимодействии с азотом (табл. 5)в интервале 670 – 14900С образуются нитриды: ThN, Th2N3, (Th3N4). Не исключается образование и при более низкой температуре (450 – 5000С).
Таблица 4. Коррозия тория в газах при 800 0С в течение 0.5 часа
| Газ | Привес, мг/см2 |
| Воздух Технический азот Очищенный азот Технический аргон Очищенный аргон | 6,0 4,4 2,0 1,0 0,75 |
Сильную коррозию вызывает водород. При 4000С убыль веса образца составляла 80 мг/см2·ч, а при 5000С – 129 мг/см2·ч. При длительной выдержке металл рассыпается в порошок.
Считают, что в различных интервалах температур образуется и разлагается различные гидриды и твердые растворы тория и водорода. Так в интервале 170 – 3600С образуется и разлагается ТhН3. При 350 – 3600С образуются ТhН1,9Н2, при 4000 идет медленное разложение дигидрида, в интервале 400 – 8000 образуются твердые растворы состава aТh – ТhН2. Температуре 6000С соответствует фаза ТhН1,5. Максимальная скорость разложения ТhН1,5 до свободного aТh – около 8000С, а полностью процесс заканчивается при 9000С. При 12000С газовыделения нет.
|
|
|
Коррозия тория в воде зависит от чистоты последней и температуры. В очищенной воде при повышенных температурах – до 3500С идет взаимодействие по реакции Тh + 2Н2О = ТhО2 + 2Н2.. При 24-х часовой выдержке при 1780С на поверхности металла образуется темный порошок – смесь оксида и металла. При 48 часовой выдержке цвет порошка серый – в нем больше оксида. При пониженных температурах - до 1000С на поверхности тория образуется пленка, а коррозия составляет около 10 мг/см2·ч, повышение температуры до 2600С ведет к незначительному увеличению коррозии – до 11 мг/см2·ч, а при 3150C коррозия возрастает до 55 мг/см2·ч. Значительно ниже коррозия в дистиллированной воде: при 1000С привес образца металла составлял 0,1 мг/см2·мес.
Коррозионную стойкость тория повышает легирование цирконием и титаном, а добавки кремния, алюминия, железа, ванадия, хрома, ниобия, молибдена, марганца, бериллия – понижают.
Взаимодействие с кислотами. Плавиковая кислота не действует – образуется пленка фторида. Крепкие соляная и серная кислоты действуют медленно. Пи нагревании металл быстро растворяется в соляной и разбавленной серной кислотах. Только при нагревании и незначительно реагирует азотная кислота. Царская водка реагирует бурно.
Щелочи с торием не взаимодействуют.
Взаимодействие с металлами. Правильный выбор и обоснование любой пирометаллургической технологии получения, рафинирования и разделения металлов и сплавов возможен лишь на основании особенностей взаимодействия металлов.
Металлы могут образовывать простые эвтектики, твердые растворы замещения, твердые растворы внедрения, ограниченные твердые растворы, интерметаллические соединения (табл. 5).
В соответствие с эмпирическим правилом Юм Розери образование твердых растворов внедрения возможно, если разница радиусов металлов не более 59 %. А для твердых растворов замещения она не должна превышать 15 %.
|
|
|
Интерметаллические соединения образуются г.о. при взаимодействии элементов заметно отличающихся как по их химической природе, так и по активности. Металлы значительно различаются по электроотрицательности. (в металлохимии электроотрицательность определяется энергией отрыва электрона от одного атома и присоединения его к другому и имеет размерность 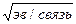 ).
).
По металлохимическим свойствам торий относится к числу электроположительных металлов. Его элетроотрицательность составляет 1,3. Он имеет сравнительно большой атомный радиус. Торий практически не взаимодействует с щелочными металлами. Потери в весе тория в эвтектическом сплаве K – Na при 6000С составляют всего 0,006 мг/см2·год. Он также стоек в жидких натрии (5000С) и литии (6000С). Можно предполагать на отсутствие взаимодействия тория с щелочноземельными металлами. С углеродом при высоких температурах образует карбиды ТhС и ТhС2. Тh и ТhС взаиморастворимы в твердом и жидком состояниях. При низких температурах происходит распад твердых растворов. Карбиды тория разлагаются водой с образованием углеводородов.
Представляет интерес взаимодействие тория с конструкционными материалами. В таблице 6 приведены данные о взаимодействии тория с некоторыми металлами.
Таблица 5. Свойства некоторых металлов и характер их взаимодействия с торием
| Металл | Температура плавления, 0С | Атомный радиус | Электро-отрица-тельность | Характер взаимодействия |
| K Na Li Mg Sr Cu Al Ni Rh La Pu Si Ce U Zr Y Th Cr Nb Ru Fe Be | 63,5 97,9 1695 (1750) | 1,35 1,90 1,55 1,60 1,15 1,28 1,43 1,24 1,34 1,87 1,34 1,82 1,52 1,60 1,8 1,8 1,26 1,46 1,34 1,26 1,12 | 0,80 0,90 0,95 1,20 1,0 1,9 1,5 1,8 2,2 1,17 1,3 1,82 1,2 1,7 1,48 1,21 1,3 2,20 1,76 2,2 1,8 1,5 | Не взаимодействуют Не взаимодействуют Не взаимодействуют Соединения, огр. тв. р. ? соединения, огр. Т. р. соединения соединения соединенияя, огр. т. р. непрер. ряд тв. р. соедин., эвт., тв. р. соединения полная растворимость огр. тв. р.,эвт. Огр. т. р., непр.ряд (b) Непер. ряд тв. р. - эвтектика эвтект., огр. т. р. соед. огр. т. р. соединения, эвтект. соединения |
Таблица 6. Взаимодействие тория с конструкционными материалами
|
|
|
| Металл | Температура начала взаимодействия |
| Al Mg Zr Ta W Nb V Mo Ni Нилюк 90 Нержав. Сталь | 500 (месяца) 600 (2 месяца) 900 (3 месяца) 900(3 месяца 900 (3мес),!300 (1 час) 800 (2мес), 900 (1 неделя) 900(1 неделя) 900 (3 месяца) 1350 (1 час) 800(24 часа) 700(1 неделя) 600 (2 месяца) |
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 347; Нарушение авторских прав?; Мы поможем в написании вашей работы!