
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вещества, сопутствующие ацилглицеринам
1. Вещества, обуславливающие окраску жиров
1.1 Каротиноиды – относят к высоконепредельным соединениям. Их подразделяют на углеводородные соединения – каротины и кислородсодержащие производные (спирты, альдегиды, кетоны, карбоновые кислоты, гидроксикетоны), которые часто объединяют под общим названием ксантофиллы.
Наличие в жирах каротиноидов, обуславливает их окраску от желтой до красной. Каротиноиды всегда содержатся в зеленых и желтых частях растений, а также в небольших количествах во многих масличных семенах.
В животных жирах содержание каротиноидов зависит от состава корма животных и чаще всего незначительно по величине.
Одним из таких углеводородов является ликопин С40Н56, обуславливающий окраску томатов, шиповника:
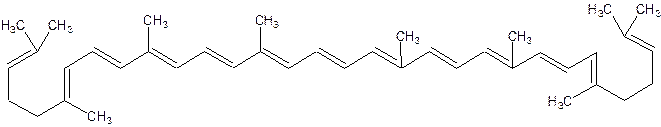
Ликопин
Наиболее часто в жирах обнаруживается каротин С40Н56, который представлен тремя изомерами: α, β, γ. Из них, например в моркови, наиболее распространен β – каротин, на долю которого приходится 85% масс. от всего содержании каротинов, α – каротин – около 15%мас., γ – каротин примерно 0,1%мас.
α – и β – каротин содержатся в растительных жирах. Каротины играют важную роль в физиологии животных организмов, поскольку в печени из них образуется витамина роста – витамина А.
При окислении β – каротина получают две моле6кулы витамина А, а при окислении α – и γ – каротинов получают по одной молекуле этого витамина.
В молекулах каротиноидов находится цепь атомов углерода с длинной системой сопряженных двойных связей и рядом ответвлений в виде метильных групп. Эту часть молекулы каротиноидов рассматривают как продукт полимеризации радикалов С5Н6, образующихся при дегидрировании изопрена:
СН2 = С – СН = СН2→ = СН – С = СН – СН =
СН3 СН3
Поскольку ликопин и каротины содержат по 40 углеродных атомов, они могут рассматриваться как образованные восемью остатками изопрена.
Молекула β – каротина имеет симметричное строение:
|
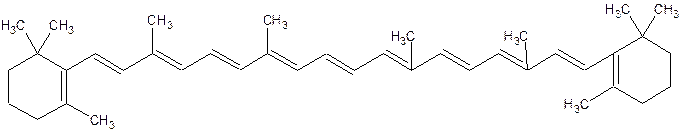
β – каротин
β – каротин представляет собой кристаллическое соединение с tпл 182 - 184°С. На концах алифатической цепи молекулы β – каротина находится два β– иононовых кольца, содержащих по шесть атомов углерода.
α – каротин отличается от β – каротина тем, что в одном из иононовых колец двойная связь перемещена:
|
|
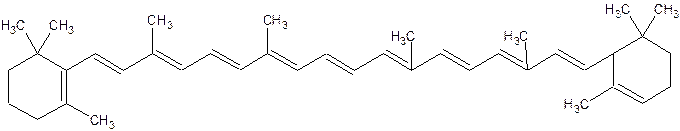
α – каротин
γ – каротин имеет одно β– иононовое кольцо, а второе развернуто в виде алифатической цепи атомов углерода:
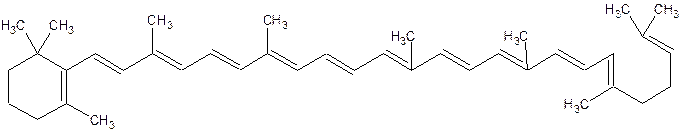
γ – каротин
Хромофорной группой, обуславливающей окраску каротиноидов, является длинная система сопряженных двойных связей. Поэтому при значительном нарушении этой системы Каротиноиды обесцвечиваются. Это происходит, например, при гидрировании их с активным катализатором.
Каротиноиды являются сильно ненасыщенными веществами, поэтому как в кристаллах, так и растворенные в масле, они легко окисляются кислородом воздуха. При окислении каротиноиды постепенно обесцвечиваются. Каротиноиды легко окисляются такими сильными окислителями, как хромовая кислота. Длительное воздействие на растворы каротина в жирах УФ – и γ – излучения приводит к их обесцвечиванию.
При нагревании до 50 - 70°С каротиноиды практически не изменяются. В жире при высоко температуре они могут полиризоваться.
Молекулы α – и β – каротина имеют по 11 сопряженных двойных связей; γ – каротин имеет 12 сопряженных связей.
Каротины растворимы в хлороформе, бензоле, диэтиловом эфире, нерастворимы в этаноле и воде.
Все без исключения другие природные каротиноиды являются производными четырех указанных выше углеводородов – ликопина и каротинов. Они образуются их эти углеводородов путем введения гидроксильных, карбонильных или метоксильных групп, или же путем частичной гидрогенизации или окисления.
Витамин А, получаемый из β – каротина имеет формулу:
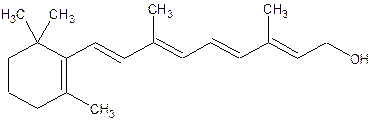
Это первичны спирт – ретинол ( С20Н30О).
Ксантофилл лутеин является производным α – каротина – это желтый каратиноид желтка куриного яйца:
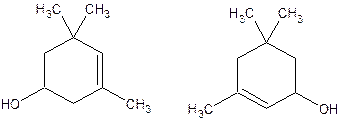
Лутеин
Так, например, в результате введения в молекулу β – каротина двух оксигрупп образуется каротиноид, содержащийся в зерне кукурузы и называемый цеаксантином С40Н55О2:
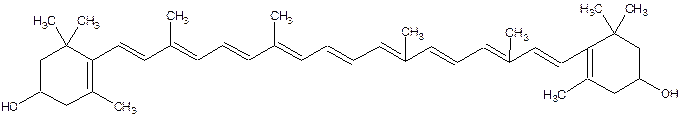
Цеаксантин
В результате присоединения к молекуле β – каротина одного атома кислорода с образованием фураноидной структуры получается каротиноид цитроксантин С40Н56О, содержащийся в кожуре цитрусовых плодов:
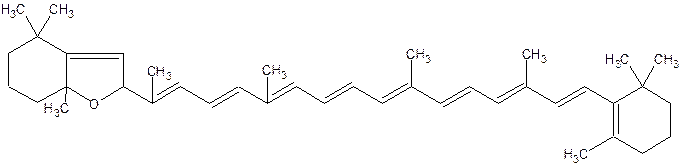 Цитроксантин
Цитроксантин
В бурых водорослях содержится каротиноид фукоксантол С40Н60О6, который принимает участие в процессе фотосинтеза в качестве так называемого вспомогательного пигмента:
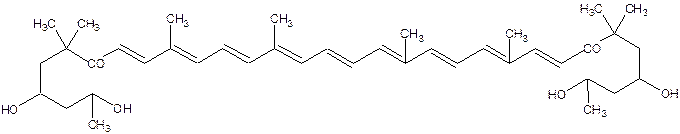 Фукоксантол
Фукоксантол
Исходя из химического строения каротиноидов, содержащих значительное количество двойных связей, можно предполагать, что они являются в растении переносчиками активного кислорода и принимают участие в окислительно-восстановительных процессах. На это указывает факт широкого распространения в растениях кислородных производных каротиноидов, называемых эпоксидами, чрезвычайно легко отдающих свой кислород. Примером такого кислородного производного может служить диэпоксид β – каротина:
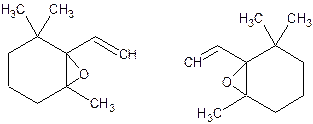
Диэпоксид β – каротина
Важным средством для идентификации каротиноидов являются спектры поглощения их растворов. Почти все каротиноидные пигменты имеют три четких максимума поглощения в видимой части спектра. Положение этих максимумов определяется главным образом количеством двойных связей в соответствующем пигменте. Каждая новая двойная связь в системе сопряженных двойных связей смещает максимум поглощения в сторону больших длин волн примерно на одну и ту же величину, а именно на 200 - 220Ǻ.
1.2 Хлорофиллы
Наличие хлорофиллов является причиной зеленых оттенков в цвете некоторых жиров, например масел: конопляного, рапсового, соевого.
Пигмент листьев растений – хлорофилл представляет собой смесь двух твердых веществ. Одно из них – хлорофилл α – окрашено в сине-зеленый цвет (температура плавления 117°С), другое – хлорофилл b – в светло-зеленый (температура плавления 120°С). Хлорофилла α обычно содержится в листьях в 3 раза больше, чем хлорофилла b.
Общая формула хлорофилла α – С55Н72О5N4Mg, хлорофилла b – С55Н70О6N4Mg.
Оба хлорофилла – производные сложных по составу и структуре дикарбоновых кислот, один карбоксил которых этерифицирован метанолом, другой высшим алканолом – фитолом – С20Н40О.
Основу указанных дикарбоновых кисло составляет порфириновое кольцо, по структуре аналогичное основе гемоглобина крови.
В чистом виде оба хлорофилла представляют собой кристаллические вещества.
Содержание хлорофиллов в жирах невелико. Оно зависит от условий извлечения масел из масличного сырья. В соевом масле, например, содержится от 1×10-4 до 1,5×10-4 % мас. хлорофиллов.
Хлорофиллы хорошо растворяются в жирах и жировых растворителях.
При обработке минеральной кислотой хлорофиллов отщепляется магний. Осторожное действие кислоты приводит к образованию феофитина а - [С32Н32ОN4][СООСН3] и феофитина b - [С32Н30О2N4][СООСН3][СООС20Н39].
При действии на хлорофилл раствора гидроксида калия в метаноле образуются изохлорофиллины. При этом отщепляются метанол и фитол и происходит изомеризация остатка.
При отщеплении от хлорофиллинов магния образуются хлорин и родин.
В растениях часто встречаются сложные эфиры оксикоричных кислот и гидроароматических кислот (хинной и шикимовой). Характерным примером таких эфиров может служить хлорогеновая кислота (кофеил-3-хинная) кислота:
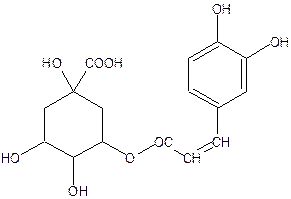
Оксикоричные кислоты – n-оксикоричная (n-кумаровая), кофейная, феруловая и синаповая - присутствуют в растениях как в свободном, так и в связанном виде.
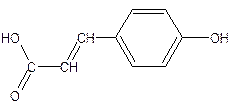
n-оксикоричная (n-кумаровая) кислота
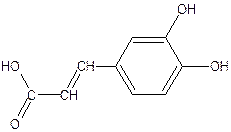
Кофейная кислота
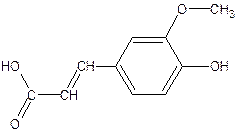
Феруловая кислота

Синаповая кислота
Характерной особенностью оксикоричных кислот является цис-транс-изомерия.
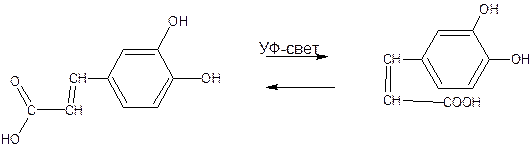
Транс-кофейная кислота Цис-кофейная кислота
Существующее в растворах подвижное равновесие этих двух форм при облучении УФ-светом резко сдвигается в сторону образования цис-формы. Эта особенность оксикоричных кислот имеет, по-видимому, важное физиологическое значение, поскольку установлено, что цис-формы являются активаторами ростовых процессов растений. Транс-формы оксикоричных кислот этой способностью не обладают.
Хлорогеновая кислота чрезвычайно широко распространена в растениях. Особенно в больших количествах она содержится в прорастающих семенах подсолнечника и необжаренных зернах кофе, где сопровождается неохлорогеновой (кофеил-5-хинной) кислотой.
1.3 Госсипол, его производные и аналоги
Это пигмент характерный для хлопкового масла С30Н30О8, находящийся в железках ядра семян хлопчатника, окрашенных от желтого до темно-синего цвета.
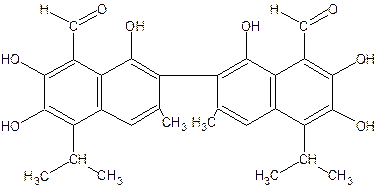
Госсипол
На основании изучения состава, структуры и свойств госсипола его считают полифенолом, содержащим в молекуле две карбонильные группы. Возможно, что Госсипол встречается в трех таутомерных формах:
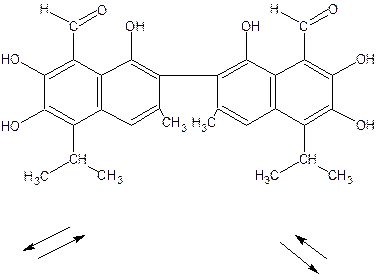
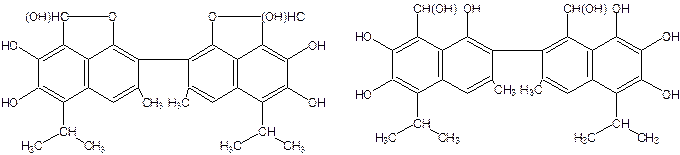
Госсипол представляет собой твердые кристаллическое вещество. В зависимости от полиморфной модификации плавится при температуре 184, 199 и 214ºС.
Госсипол растворим в метаноле, этаноле, диэтиловом эфире, ацетоне, хлороформе, пиридине. Он плохо растворим в глицерине, бензоле, петролейном эфире, кипящем в пределах 60 - 110°С, нерастворим в низкокипящем петролейном эфире (30 - 60ºС) и в воде.
Госсипол ведет себя как сильная дикарбоновая кислота, давая с гидроксидами щелочных металлов соответствующие феноляты, называемые госсиполатами.
С гидроксидами щелочных металлов в молекуле госсипола реагируют два гидроксила, находящихся в орто-положении по отношению к карбонильным группам. Образующиеся госсиполаты щелочных металлов растворимы в воде.
Растворы госсиполатов калия и натрия, содержащие избыток гидроксида щелочного металла, очень легко окисляются кислородом воздуха. При этом они приобретают темную окраску.
При нагревании госсипол реагирует со многими соединениями, содержащими аминную группу. Например, госсипол реагирует с анилином (используется для количественного определения госсипола). Реакция идет по карбонильной группе.
Госсипол образует с антраниловой кислотой нерастворимые в масле соединения по реакции: 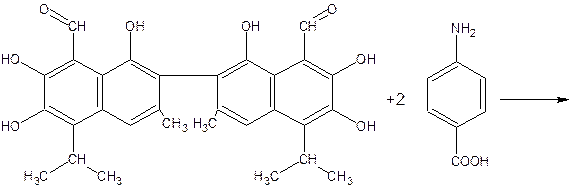
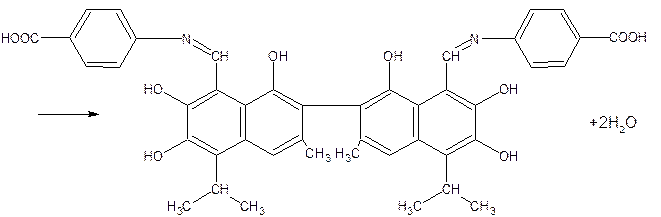 Эта реакция используется для выделения госсипола из хлопкового масла.
Эта реакция используется для выделения госсипола из хлопкового масла.
При нагревании раствора госсипола в масле, содержащем фосфолипиды, протекает реакция, сопровождающаяся образованием темноокрашенного продукта (темно-коричневого или синего цвета) – госсифосфатиды, образующиеся за счет реакции одной или обеих альдегидных групп молекулы госсипола с аминогруппами кефалинов и фосфосеринов, но не с лецитинами.
В случае возникновения азометиновых связей (─N=CH─) образовавшиеся госсифосфатиды при кислом или щелочном гидролизе распадаются.
Госсифосфатиды хорошо растворимы в нагретом масле, бензиновых растворителях его, в ряде жирорастворителей, но не растворимы в ацетоне.
К аналогам госсипола относят госсипурин, госсикаэрулин и госсифульвин. Госсипурин выделяется из хлопкового масла вместе с госсиполом. Он придает этой смеси красноватый оттенок.
Состав госсипурина точно не установлен. Ему приписывается формула С30Н32О7. по некоторым данным, можно предположить, что госсипурин состоит из молекул госсипола и диаминогоссипола, соединенных двумя кислородными мостиками подобно дисалициловому альдегиду.


2. Вещества, обуславливающие вкус и запах жиров
2.1 Гликозиды. Глюкозиды представляют собой сложные вещества, состоящие из углеродной части и неуглеродной, называемой аглюконом.
Природные глюкозиды чаще всего классифицируют по характеру агликонов, например: цианглюкозиды, тиогликозиды, стеролглюкозиды, сапонинглюкозиды.
Глюкозиды – твердые, кристаллические или аморфные вещества, растворимые в воде и спирте. При кислотном и ферментативном гидролизе они распадаются на углеводную и аглюконовую часть.
Глюкозиды широко распространены как в животном, так и особенно в растительном сырье. Сами глюкозиды плохо растворяются в органических гидрофобных растворителях и в растительных маслах, но отщепляющаяся при ферментативном гидролизе агликоновая часть может переходить в масло при экстракции или прессовании. Значительная часть гликозодов и продуктов их распада остается в жмыхах и шротах.
Цианглюкозиды. В аглюконовом компоненте цианглюкозидов содержится остаток синильной кислоты. Наиболее важным их представителями являются амигдалин и линамарин.
Амигдалин С20Н27О11N ·3 Н2О представляет собой соединение дисахарида генциобиозы и бензальдегидциангидрина и имеет следующее строение:
|
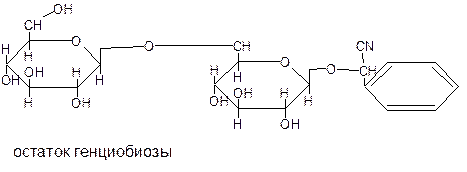
Амигадлин образует кристаллы горького вкуса, легко растворимы при нагревании в воде и спирте. При кислотном гидролизе амигдалин образует две молекулы глюкозы, молекулу бензальдегида и молекулу синильной кислоты.
Амигдалин в значительных количествах содержится в семенах горького миндаля (2,0 – 3,5%), в косточках персиков (1,8 – 3,6%), абрикосов (1,0 – 1,8%), вишен (0,8 – 1,0%), слив (до 1,8%). Сам амигдалин не ядовит, но при ферментативном и кислотном гидролизе выделяет ядовитую синильную кислоту.
При извлечении масла из косточковых прессованием или экстракцией может образовываться свободная летучая очень ядовитая синильная кислота. Поэтому при переработке косточковых необходимо принимать соответствующие меры предосторожности. Небольшое количество синильной кислоты попадает в масло, откуда она может быть удалена при рафинации.
Линамарин С10Н17NО6 состоит из остатков глюкозы и ацетонциангидрина и имеет следующее строение:
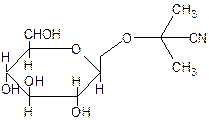
 |
Линамарин представляет собой бесцветные игольчатые кристаллы, легко растворяющиеся в воде, значительно более горького вкуса, чем амигдалин. При кислотном гидролизе линамарин расщепляется на глюкозу, синильную кислоту и ацетон.
Гликозид линамарин содержится в семенах льна, причем количество его по мере созревания семян уменьшается.
При определенных температурах и влажности материала лиманарин под действием находящихся льняных семенах фермента линамарозы (линазы) расщепляется с образованием свободной синильой кислоты.
Тиоглюкозиды. Тиоглюкозиды соржатся в семенах крестоцветных. Важными представителями тиоглюкозидов являются синигрин,синальбин и глюконапин.
Синигрин С20Н27О9NS2 имеет следующее строение:
НОСН2—СН—(СНОН)3—СН—S—С=N—СН2—СН=СН2
О ОSO3H
Глюкозид синигрин содержится в значительных количествах в семенах сарептской и черной горчицы в виде калиевой соли, которая представляет собой легко растворимые в воде кристаллы.
Синигрин мало устойчив, поэтому в ходе переработки семян горчицы он может гидролизоваться с выделением аллилгочичного масла, хорошо растворимого в жирном масле.
Синальбин С30Н44N2S2О16 имеет следующую строение:
OSO2OC16H24O5N
НОСН2—СН—(СНОН)3—СН—S—C
O N—CH2—C6H4OH
Синальбин содержится в семенах белой горчицы.
Стеролглюкозиды. Аглюконовой частью стеролглюкозидов являются стеролы, а углеводной частью d-глюкоза. Стеролглюкозиды найдены в соевых семенах и в небольших количествах (0,01%) в соевом масле, а также в фосфатидных концентратах, выделяемых из соевых масел.
Сапонинглюкозиды (сапонины). Сапонинглюкозиды относятся к группе стероидных глюкозидов. Углеводной частью сапонинов могут быть гексозы и пентозы, а Аглюконовой – сапогенины.
В сапогенинах стероидное ядро соединено с циклической спирановой кетальной группировкой:
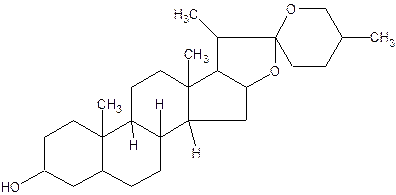
Сапонины способны понижать поверхностное натяжение воды и подобно мылам образовывать пену. Они имеют горький вкус. Некоторое сапонины обладают сильными гемолитическими действиями и, следовательно, ядовиты. Сапонины найдены в семенах сои.
Аглюконовая часть сапонинглюкозидов после их распада может переходить в соевое масло.
Фенолглюкозиды. К группе фенолглюкозидов относят вещества, содержащие в качестве аглюконов фенолы и фенолоспирты.
В семенах кунжута содержится фенолглюкозид сезамолин:
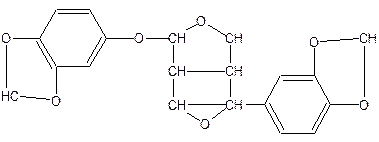
Сезамолин – твердое вещество с температурой плавления 93,6ºС. Он растворим во многих органических растворителях и в масле, устойчив к действию щелочей (при омылении кунжутного масла локализуется в его неомыляемой части), но распадается при нагревании в присутствии соляной кислоты.
При кислотном гидролизе сезамолина получается сезамол и самин:
|
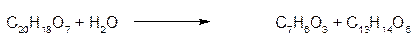
Сезамол (3,4 – метилендиоксифенол) кипит при 105 - 110ºС имеет следующее строение.
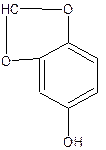
Сезамол является ингибитором окисления жиров. В кунжутном масле может содержаться до 0,41% сезамолина и до 0,1% свободного сезамола.
При дезодорации кунжутного масла содержание сезамола в них несколько уменьшается вследствие частичной отгонки.
Самин – кристаллическое вещество, ему приписывают следующее строение:
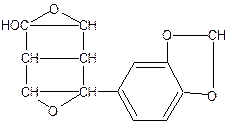
Чем больше содержится в масле сезамола, тем больше накапливается в нем и самина, так как оба э эти вещества являются продуктами распада сезамолина.
Кукурбитацин. Горечь плодов – наследственное свойство, присуще тому или иному сорту, вследствие присутствия глюкозида кукурбитацина.
Высокая температура воздуха, яркое солнечное освещение при недостатке влаги в почве и особенно в воздухе способствует усилению горечи.
Более того, кукурбитацин обладают целебными свойствами: они сдерживают рост злокачественных опухолей.
Накопление кукурбитацинов – естественная ответная реакция растении на ухудшение условий роста: сокращение длины светового дня и интенсивности освещения, недостаточность или переизбыток минерального питания и снабжения водой.
Близки к стеринам витанолиды (ненасыщенные лактоны) и кукурбитацины (ненасыщенные горькие вещества из тыквенных растений).
Кукурбитацины, относящиеся к классу тетрациклических тритерпеноидов. В растениях присутствуют кукурбитацины и свободные, и связанные с молекулой сахара в виде глюкозидов. Горечью овощи обязаны свободным кукурбитацинам. Даже в темноте горечь появляется. На свету процесс идет значительно быстрее.

Кукурбитацин В
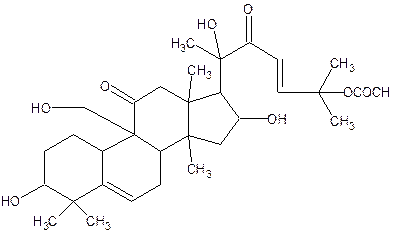
Кукрбитацин С
Кукурбитацин есть и в горьких и в сладких овощах, все дело лишь в количестве, в овощаз безгоречи кукурбитацинов очень мало.
Один из ферментов – эластаза вызывает ферментативный распад глюкозидов на кукурбитацины и сахара. Когда плод созревает горечь уменьшается, а в семенах и мякоти семенника накапливаются глюкозиды.
|
Дата добавления: 2014-01-20; Просмотров: 1986; Нарушение авторских прав?; Мы поможем в написании вашей работы!