
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Адиабатический процесс
|
|
|
|
Большой практический интерес представляет адиабатный процесс — термодинамический процесс, в котором система не обменивается теплотой с окружающей средой.
Адиабатическим (адиабатным ) называется процесс, происходящий без теплообмена с внешней средой.
Из этого определения следует, что в адиабатном процессе δQ=0. Следует отметить, что условие отсутствия теплообмена нельзя формулировать в виде Q = 0. Это равенств говорит лишь о том, что в целом за вес процесс алгебраическая сумма теплот, подведенных к системе и отведенных от нее равна нулю.
Условие Q = 0 вовсе не исключает теплообмена между системой и внешней средой на отдельных участках рассматриваемого процесса. Практически адиабатный процесс осуществляется при достаточно быстром расширении или сжатии газа.
Из первого закона термодинамики имеем для адиабатного процесса δА=-dU, т.е. в адиабатном процессе систем совершает работу за счет убыли внутренне энергии системы.
Для адиабатного процесса идеального газа из следует, что 
Рассмотрим поведение идеального газа при адиабатическом процессе.
Из первого начали термодинамики имеем 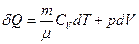 , для адиабатического процесса
, для адиабатического процесса 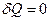 ,
,
Поэтому

Из уравнения состояния идеального газа выразим давление  ,
,
Поэтому
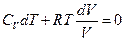 ,
,
или

Проинтегрируем, получим:
 ,
,
Но  ,
,
поэтому  – уравнение адиабаты в переменных T и V.
– уравнение адиабаты в переменных T и V.
Если подставить Т из уравнения Менделеева - Клапейрона, 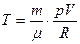 ,
,
то получим:
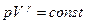 (29)
(29)
– уравнение адиабатного процесса или уравнение адиабаты в переменных р и V (Уравнение Пуассона) .
Уравнение изотермы в тех же переменных pV=const.
Постоянная g называется коэффициентом Пуассона.
 Покажем, что адиабата идет круче изотермы.
Покажем, что адиабата идет круче изотермы.
Для этого сравним производные dp/dV для обоих процессов.
|
|
|
 Для изотермического процесса
Для изотермического процесса  ,
,
Откуда  .
.
Для адиабатного процесса  ,
,
откуда  .
.
Поскольку  , то адиабаты действительно идут круче изотерм.
, то адиабаты действительно идут круче изотерм.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1430; Нарушение авторских прав?; Мы поможем в написании вашей работы!